Какие антибиотики можно принимать кормящей маме
В период грудного вскармливания лекарственные препараты следует принимать с особой осторожностью. Многие средства не совместимы с лактацией, они негативно влияют на сосав и выработку молока. Кроме того, некоторые медикаменты, особенно антибиотики при кормлении грудью, наносят вред здоровью и замедляет развитие малыша.
Антибиотики при лактации проникают в кровь и грудное молоко, а затем и в организм ребенка. В результате чего появляются побочные эффекты, среди которых отравление, расстройство пищеварения и стула, аллергическая реакция, нарушения сна и т.д.
Однако существуют ситуации, при которых прием антибиотиков необходим. Чаще всего, на период лечения грудное вскармливание временно приостанавливают. Но есть и разрешенные препараты ,которые не требуют остановки кормления грудью. Давайте узнаем, какие антибиотики можно кормящим мамам.
Влияние антибиотиков на организм грудничка
Чтобы определить степень вреда препарата для организма грудного малыша, необходимо проконсультироваться с доктором и внимательно изучить инструкцию. На уровень влияния влияют следующие факторы:
- токсичность состава средства;
- специфика воздействия лекарства на внутренние органы новорожденного;
- побочные эффекты и индивидуальная переносимость или непереносимость ребенком компонентов в составе лекарственного средства;
- риск возникновения аллергических реакций;
- продолжительность приема препаратов;
- время выведения лекарства из организма кормящей мамы;
- совместимость с лактацией.
Все необходимые сведения содержат инструкция лекарственного препарата, которую нужно изучить, даже если врач разрешил прием этого средства. Перед употреблением обязательно проконсультируйтесь со специалистом. Только о назначит правильную дозировку и схему приема, которые не повредят грудничку и маме.
Разрешенные антибиотики
Разрешенные антибиотики в период лактации, можно принимать благодаря тому, что они проникают в молоко мамы в незначительной доле и не наносят серьезного урона малышу. Антибиотики совместимые с грудным вскармливанием, можно разделить на следующие группы:
| Группа препаратов | Характеристика | Препараты |
| Пенициллины | Низкая токсичность, проникают в незначительной дозе, однако иногда вызывают диарею и сыпь | Ампициллин, Амоксиклав, Ампиокс, Амоксициллин и непосредственно сам Пенициллин |
| Аминогликозиды | Проникают в незначительной дозе, однако иногда негативно влияют на микрофлору кишечника | Гентамицин и Нетромицин |
| Цефалоспорины | Проникают в малой концентрации, однако могут вызвать диареи и повышают риск кровотечений | Цефотаксим, Цефтриаксон и Цефазолин |
Средства, которые относят к группе Макролиды, можно принимать лишь в крайних случаях и с особой осторожностью. Это препараты Сумамед, Макропен и Эритромицин. Состав медикаментов негативно влияет на самочувствие новорожденного. Прежде всего, это аллергия и дисбактериоз у грудничка.
Запрещенные антибиотики
Существует множество препаратов, которые нельзя принимать во время грудного вскармливания. Давайте узнаем, какие это средства и какие побочные эффекты они вызывают.
| Препарат | Негативное воздействие |
| Тетрациклин | Вызывает задержку в росте, ухудшает состояние костей и зубов, нарушает нормальное функционирование печени |
| Тинидазол и Метронидазол | Вызывают рвоту и серьезные расстройства стула у новорожденного, могут стать причиной замедленного роста и появления темно-желтого оттенка зубов |
| Сульфаниламид | Поражает костный мозг, вызывает кровотечения, нарушает работу сердца и сосудов |
| Левомицин | Становится причиной токсичного поражения мозга новорожденного малыша |
| Клиндамицин | Способствует возникновению кровотечений в желудочно-кишечном тракте; кормить можно не ранее, чем через 24 часа после приема |
Иногда прием перечисленных таблеток просто необходим.
Внимательно отнеситесь к введению докорма, так как иногда грудничка сложно вернуть к полному грудному вскармливанию. Особенно, если вы кормите ребенка с помощью соски.
Правила приема антибиотиков
- Не занимайтесь самолечением, обязательно обратитесь к доктору!;
- Не уменьшайте прописанную дозировку, так как это может свести к нулю полезное воздействие лекарственного срества. При этом препарат все равно проникнет в грудное молоко;
- Пейте таблетки сразу после кормления;
- Распределите прием так, чтобы это был максимальный промежуток между кормлениями. Например, если лекарство необходимо пить только раз в день, то принимайте после вечернего кормления;
- При негативной реакции грудничка на препарат, прекратите прием антибиотиков и обратитесь к врачу.
Грудное вскармливание можно вернуть после приема запрещенных антибиотиков при лактации. Восстановить кормление грудью в данном случае следует только после полного выведения состава препарата из организма мамы. Для каждого средства характерно свое время. Существуют антибиотики, которые выводятся и через 20-40 часов. А есть лекарства, которые выводятся только через неделю.
Антибиотики и грудное вскармливание | Мамоведия
Безусловно, во время кормления грудью кормящая мама должна избегать приема лекарств, а тем более антибиотиков. Но, бывают ситуации, когда кормящей маме необходимо лечение антибиотиками. В таком случае возникает вопрос, можно ли при этом кормить малыша грудью? Большинство педиатров придерживаются мнения, что можно, но главным условием этого должна быть совместимость антибиотиков с грудным вскармливанием.
Как узнать, совместимы ли назначенные Вам антибиотики с грудным вскармливанием? Доктором Хейлом был разработан специальный справочник, с помощью которого можно узнать совместимость тех или иных медицинских препаратов с грудным вскармливанием. Также совместимость конкретного лекарственного препарата с кормлением грудью можно узнать также по справочнику ВОЗ, онлайн-справочнику Е-lactancia и Lactmed.
В большинстве случаев, при правильном подборе антибиотиков кормящей маме допускается грудное вскармливание. При назначении антибиотиков кормящей матери доктору необходимо остановить выбор на тех препаратах, которые принесут наименьшее отрицательное действие на организм ребенка.Доказано, что все антибиотики пенициллинового и цефалоспоринового ряда являются допустимыми при грудном вскармливании. Именно поэтому, при назначении доктором антибиотиков женщине, которая кормит грудью, должна учитываться безопасность препарата для ребенка.
Учеными и медиками установлено, что в молоко кормящей матери попадает только – 1-2% лекарств, которые принимает мать. Исходя из этого, вероятность того, что антибиотики при грудном вскармливании принесут вред ребенку достаточно мала, но все же она существует. Особенно осторожным нужно быть с малышом в возрасте до полугода, который находиться исключительно на грудном вскармливании.
Для того, чтобы максимально уменьшить побочные действия антибиотика для кормящей мамы и малыша, а также избежать негативных реакций со стороны организма ребенка, доктор может порекомендовать совместно с приемом антибиотиков принимать также пробиотики. Благодаря приему пробиотиков возможно защитить микрофлору кишечника матери и ребенка.
На сегодняшний день практически все современные антибиотики, которые имеют форму таблеток и капсул являются безопасными при грудном вскармливании. А вот антибиотики в инъекциях считаются более опасными для малыша. Опасность некоторых антибиотиков для ребенка состоит в том, что эти препараты могут накапливаться в крови малыша по причине незрелости работы их выделительной системы, а также достаточно слабой очистительной способности крови ребенка.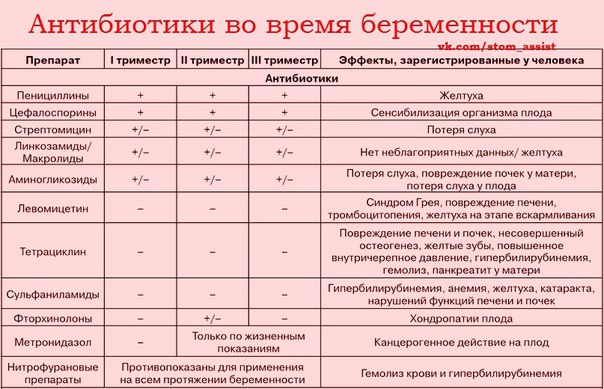
Безусловно, принимать антибиотики кормящая мама может только после назначения доктора и при наличии строгих показаний к этому. Перед приемом антибиотика необходимо внимательно ознакомиться с инструкцией по применению препарата. В том случае, если в инструкции будет указано, что данный антибиотик возможен для применения ребенком того же возраста что и Ваш малыш, то такой препарат может применять и кормящая мама.
Прием антибиотиков кормящей матерью лучше всего совершать во время кормления или сразу после кормления малыша грудью, поскольку, таким образом, возможно избежать периода максимальной концентрации их в крови и уменьшить отрицательное влияние препарата на малыша.
В том случае, если по состоянию здоровья матери необходим прием антибиотиков, которые являются вредными для малыша, то кормление грудью лучше временно прервать, но при этом нужно поддерживать лактацию и регулярно сцеживаться. После приема опасных для ребенка антибиотиков, грудное вскармливание можно возобновить только через сутки после окончания приема препарата.
К наиболее опасным последствиям приема антибиотиков кормящей матерью являются следующие: риск желудочно-кишечного кровотечения у ребенка, риск токсического поражения костного мозга, задержка роста.
В любом случае, при приеме антибиотиков во время грудного вскармливания должно быть регулярное и тщательно наблюдение за состоянием малыша, поскольку возможно появление у малыша поноса, сыпи на кожных покровах, аллергических реакций, повышенного слюнотечения.
При появлении любых негативных реакция со стороны организма малыша, его следует немедленно показать педиатру.
Самое главное, что должна помнить кормящая мама при приеме антибиотиков, так это то, что необходимо строго соблюдать назначенную дозировку препарата, никогда не уменьшать дозу и не отменять самостоятельно прием препарата, даже если симптомы заболевания заметно уменьшились.
Разрешенные антибиотики при грудном вскармливании
Как известно, при лактации мама должна соблюдать определенного рода диету.
В первую очередь необходимо отметить, что прием любого лекарства в обязательном порядке должен быть согласован с врачом, который должен указать дозировку, кратность и продолжительность приема.
Если же конкретно говорить о том, какие антибиотики можно принимать при грудном вскармливании, необходимо выделить следующие группы данного рода препаратов:
- Пенициллины (Аугментин, Оспамокс, Амоксициллин и др.) — нередко назначаются кормящим мамам. Данные препараты в достаточно малых концентрациях проникают в грудное молоко. Однако стоит учитывать, что эти антибиотики обладают способностью вызывать аллергические явления у малыша и кормящей. Поэтому мама должна следить внимательно за реакцией со стороны малыша. Из побочных эффектов стоит отметить послабление стула.
- Цефалоспорины (Цефрадин, Цефуроксим, Цефтриаксон). Обладают малой токсичностью и не проникают в грудное молоко. Не оказывают влияние на малыша.
- Макролиды (Азитромицин, Кларитромицин, Эритромицин). Несмотря на то, что компоненты данных антибактериальных препаратов все же попадают в грудное молоко, они никак не влияют на организм малыша. Эта группа лекарственных средств является так называемыми препаратами выбора, при развитии аллергии на употребление пенициллинов и цефалоспоринов.
Разобравшись с тем, какие антибиотики совместимы с грудным вскармливанием, расскажем о том, как их правильно пить.
Во-первых, для того чтобы выяснить, какой антибиотик можно пить в данном случае при грудном вскармливании, необходимо обратится к врачу. Ведь подбор лекарств проводится исключительно после определения типа возбудителя.
Во-вторых, необходимо строго соблюдать дозировку и частоту приема препарата, для того чтобы лечение было эффективным.
В-третьих, пить антибиотик лучше непосредственно при кормлении грудью или сразу после него. Это позволит сделать так, чтобы прием лекарства осуществлялся перед максимальным промежутком между кормлениями.
Таким образом, как видно из статьи, антибиотики при грудном вскармливании использовать можно, однако стоит ли делать это в конкретном случае, — должен решать врач. Кормящая мама, в свою очередь, должна строго следовать его указаниям.
список эффективных и разрешенных препаратов
В статье рассмотрим антибиотики от мастита для кормящей мамы.
Под маститом понимается процесс воспаления, преимущественно инфекционного происхождения, который поражает интерстициальную ткань и паренхиму грудной железы. Около 90% поражений молочных желез связаны с лактацией и появляются в основном в первые недели после рождения ребенка. Подавляющее количество случаев патологии приходится на тех, кто рожал в первый раз (от 70 до 75%), если роды повторные, частота их резко уменьшается.
Какие антибиотики можно при мастите, важно выяснить заранее.
Молочная железа поражается при третьих и последующих родах лишь в 2%.
Если был диагностирован мастит, нужно дифференцировать его от парамастита. В данный термин входят другие кожные инфекционно-воспалительные заболевания и ПЖК молочной железы (рожа, флегмоны, абсцессы, карбункулы и фурункулы).
Какие антибиотики принимать при мастите, рассмотрим ниже.
Причины появления воспаления желез и классификация
Самыми распространенными причинами, которые способствуют возникновению маститов, становятся: мастопатии; застой молока; трещины сосков; нерегулярные кормления; неправильное прикладывание малыша к груди; резкое сворачивание лактации; недостаточное сцеживание; несоблюдение правил гигиены; гипергалактия; иммунодефицитные состояния, тугое нижнее белье, которое сдавливает молочную железу; уменьшение естественной резистентности женского организма.
У послеродовых маститов клиническая картина соответствует этапам их развития:
- стадия патологического лактостаза;
- мастит серозного типа;
- инфильтративная форма;
- маститы гнойные: гангренозные, инфильтративно-гнойные, гнойно-некротические (флегмонозные), абсцедирующие.
Какие антибиотики назначают при мастите у женщин, интересно многим.
Основные симптомы патологии
Чаще всего застой молока возникает на первой неделе лактации. Общее самочувствие женщина на начальных стадиях может быть нарушено незначительно. Температуры поднимается не более 38 градусов. Поступают жалобы на нагрубание груди и ее умеренную болезненность. На данной стадии болезни целесообразно пользоваться немедикаментозными лечебными методами.
Если симптомы прогрессируют, то определяется серозный мастит. Такая форма заболевания отличается повышением температуры более 38 градусов, ухудшением самочувствия в целом. Пациентки говорят о выраженной слабости, боли молочных желез, ознобе. При прощупывании груди чувствуются ограниченные болезненные, уплотненные участки. Покровы кожи гиперемированы около ореол. Пораженная грудь со временем увеличивается в размере.
Если отсутствует адекватная своевременная терапия, серозный мастит трансформируется в инфильтративный, при котором молочная железа резко болезненная и плотная, увеличиваются лимфатические регионарные узлы, в дальнейшем может происходить нагноение инфильтрата.
Гнойные формы отличаются тяжелой интоксикацией, сильной лихорадкой, болью как в груди, так и в лимфатических регионарных узлах. Такой мастит чаще всего протекает как диффузная гнойная инфильтрация с отсутствием абсцесса. Реже наблюдаются абсцедирующие формы. Исходом такого мастита могут быть сепсис и даже смерть. Наиболее тяжелой и редкой формой с очень плохим прогнозом является мастит гангренозный.
Такой мастит чаще всего протекает как диффузная гнойная инфильтрация с отсутствием абсцесса. Реже наблюдаются абсцедирующие формы. Исходом такого мастита могут быть сепсис и даже смерть. Наиболее тяжелой и редкой формой с очень плохим прогнозом является мастит гангренозный.
Когда антибиотики при мастите для кормящей мамы назначаются?
Основные факторы воспалительного процесса молочных желез – бактериальная инфекция и молочный стаз. Застой молока формирует благоприятные условия для ускоренного размножения болезнетворной флоры (клебсиеллы, стрепто- и стафилококки, синегнойная и кишечная палочки), способствую появлению в молочной железе патологии.
Главная опасность болезни кроется в быстром ее прогрессировании. Если нет своевременной терапии, патологический молочный стаз сначала перерастает в серозную, и потом – в инфильтративную разновидность мастита (через 1-3 дня). В течение нескольких суток может быть нагноение инфильтрата, превращение его в абсцесс молочной железы или флегмону, которые требуют скорейшего хирургического вмешательства. Если отсутствует специализированная помощь, из-за гнойного мастита женщина может умереть. Причиной становится сепсис.
Антибиотик при мастите у кормящих женщин в этом случае могут помочь.
Поэтому из-за вероятности быстро прогрессирующих и серьезных осложнений лечение без медикаментов. А именно: лимфодренажный массаж, прикладывание к груди теплого компресса перед кормлением и после – холодного сцеживание. Выполнение при кормлении легкого массажа, обильное питье и отдых, — целесообразны лишь на этапе молочного застоя.
Если эффект от лечения без медикаментов отсутствует, в течение суток после определения диагноза врач назначает применение антибиотиков от мастита для кормящей мамы.
Главные требования к назначаемым противомикробным средствам
Антибиотик, который назначается для кормящей матери при мастите, должен соответствовать следующим критериям:
- быть максимально безопасным для женщины и ее новорожденного ребенка;
- мало попадать в грудное молоко;
- иметь обширный спектр антимикробной активности и влиять на главных возбудителей;
- обладать повышенной тропностью к тканям желез и формировать в достаточной степени концентрацию против микробов.

В связи с этим, рекомендованными к применению и безопасными антибиотиками при мастите у кормящих женщин становятся препараты групп макролидов, цефалоспоринов и пенициллинов.
Категорически запрещается использование левомицетина, фторхинолонов, тетрациклинов и сульфаниламидов. Линкозамиды выписываются лишь по жизненным показаниям, женщина сворачивает лактацию. Применение метронидазола при мастите является причиной временной остановки естественных кормлений.
Итак, какие антибиотики принимать при мастите?
Список препаратов
Назначаются следующие антибиотики при мастите для кормящей мамы из пенициллинового ряда: «Оксациллин»; «Бензилпенициллин»; «Ампициллин»; «Флуклоксациллин»; «Амоксициллин/клавуланата»; «Диклоксациллин».
К использованию рекомендуются макролиды: «Эритромицин»; «Кларитромицин»; «Джозамицин»; «Азитромицин».
Из числа цефалоспоринов назначаются: «Цефазолин»; «Цефтриаксон»; «Цефокситин»; «Цефметазол»; «Цефуроксим».
Рассмотрим подробнее антибиотики от мастита, разрешенные при грудном вскармливании.
Препарат «Амоксиклав»
Это амоксициллин, который защищен клавулановой кислотой (ингибитором бета-лактамазы), представляет собой «золотой стандарт» для начального лечения при мастите. В спектр его противомикробной активности входят аэробные и анаэробные возбудители.
Какова дозировка антибиотика от мастита для кормящей мамы? Желательно принимать в количестве 500 плюс 125 мг каждые восемь часов, или 875 + 125 каждые двенадцать часов.
Препарат не назначается пациенткам с почечной недостаточностью, непереносимостью бета-лактамов, лимфолейкозом и холестазом. Если есть недостаточность почек, доза корректируется в соответствии со значением скорости фильтрации клубочков.
Самыми распространенными побочными эффектами для матери становятся: расстройства ЖКТ; дисбактериоз; кандидоз; аллергические реакции. Для малыша при продолжительном использовании имеется вероятность нарушения и сенсибилизации кишечной микрофлоры. Поэтому продолжительность терапии согласовывается с лечащим врачом в обязательном порядке.
Поэтому продолжительность терапии согласовывается с лечащим врачом в обязательном порядке.
Какие еще антибиотики от мастита, разрешенные при грудном вскармливании, эффективны.
«Цефалексин»
Это бактерицидное средство первого цефалоспоринового поколения. Используется перорально. Он активен против перечня главных возбудителей. Но по сравнению со вторым и третьим поколениями выделяется в большем количестве с грудным молоком. Именно поэтому может рекомендоваться временное прекращение кормления грудью.
Назначается в количестве 0,5 граммов каждые шесть часов.
Если у женщины аллергия на цефалоспорины, то препарат противопоказан. У пациенток с уменьшенным креатининовым клиренсом есть необходимость коррекции дозировки.
«Цефтриаксон»
Это популярный антибиотик, совместимый с грудным вскармливанием при мастите.
Входит в третье цефалоспориновое поколение. Используется инъекционно. Отличается обширной сферой противомикробной активности, устойчив к подавляющему количестве бактериальных бета-лактамаз.
При непереносимости цефалоспоринов и пенициллинов не назначается.
Выписывается внутримышечно или внутривенно по тысяче миллиграммов два раза в день.
Пациентки переносят препарат хорошо, его использование редко вызывает побочные эффекты. Как правило, нежелательные действия проявляются в виде кандидоза, дисбактериоза, флебита при введении внутривенно, могут быть аллергические реакции.
«Флуклоксациллин»
Еще один антибиотик, совместимый с грудным вскармливанием при мастите.
Входит в группу пенициллинов полусинтетических. Влияет бактерицидно. Он эффективен против грам+ и грам- кокков, грам- палочек (сальмонелл, кишечной палочки, шигелл, клебсиелл).
Назначается в дозировке 250 миллиграммов (в форме таблеток) в сутки четыре раза.
Антибиотик от мастита у кормящей матери не применяется у пациенток с индивидуальной чувствительностью к пенициллинам и офтальмологическими заболеваниями.
Самыми распространенными побочными проявлениями становятся: диспепсические расстройства, колит, аллергии, грибковые воспаления слизистых, а также нарушение микрофлоры кишечника.
Какой антибиотик лучше при мастите, подскажет врач.
Продолжительность антибактериального курса
Антибиотики при лечении мастита применяются от семи до десяти суток. Категорически запрещается прием медикамента раньше, чем через два дня после совершенного клинического восстановления. Кроме того, нужно помнить, что при источнике воспаления молочных желез в виде стафилококков, антибактериальное лечение должно колебаться от десяти дней до двух недель.
Какие антибиотики пить от мастита, знают не все.
Способность антибиотиков к проникновению в грудное молоко, воздействие их на малыша
Пенициллиновые препараты в малых количествах попадают в молоко. Наименьшее значение перехода у препаратов с обширным спектром влияния. Связано это с тем, что данные средства максимально соединяются с белками кровяной плазмы (исключение – лишь ампициллин) и выводятся интенсивно вместе с уриной.
Цефалоспорины тоже в низкой степени попадают в молоко, около трех процентов от содержания в крови антибиотика, но при воспалительном процессе молочных желез данный показатель несколько увеличивается.
При лечении мастита у женщин антибиотиками нужно проявлять осторожность.
С молоком меньше всего выделяются второе и третье поколения цефалоспоринов. По сравнению с пенициллинами значение перехода более высокое, но есть возможность аллергических реакций ц женщины и сенсибилизации малыша.
Макролиды отлично попадают в молоко и способны создавать там концентрацию в два раза меньше, чем в крови. Из-за этого в значительной степени превышаются показатели цефалоспоринов и пенициллинов. Но у макролидов нет минимального токсического влияния, низкой вероятности появления аллергии и прочих осложнений от терапии со стороны женщины, то есть они не действуют на ребенка отрицательно. Препараты данной группы в связи с этим также могут назначаться при женских маститах, если пациентка не желает сворачивать грудное вскармливание.
Антибиотики от мастита можно приобрести в любой аптеке.
Противопоказания к другим антибиотикам
Аминогликозидные антибиотики мало попадают в молоко, но у них высокие токсические показатели и для женщины, и для ее ребенка. Они могут вызвать нарушение слуха и псевдомембранозный колит у малыша. Кроме того, имеется большая вероятность повреждения почек пациентки.
Тетрациклины имеют высокое значение выделения с молоком женщины в среднем 60-75% от содержания в крови. У них много нежелательных эффектов и высокая токсичность. Могут вызвать тяжелую форму грудничкового колита (вплоть до смерти малыша), нарушению образования зубных зачатков и роста костной ткани.
У фторхинолонов тоже есть способность выделения с молоком в большом количестве. Это эффективные и одновременно очень токсичные медикаменты. Организм переносит их тяжело, есть большая вероятность нежелательных явлений. В связи с довольно частыми осложнениями суставов, почек, связочного аппарата, появления фотосенсибилизации и способности к нарушению формирования скелета беременным, кормящим матерям и несовершеннолетним девушкам не назначаются.
С грудным молоком клиндамицин выделяется мало, но может вызвать тяжелую форму псевдомембранозного колита. В высоких дозах выделяется линкомицин и зачастую приводит к серьезному нарушению микрофлоры и появлению аллергии у грудничка.
Эффективность и безопасность использования прочих противомикробных препаратов при воспалительном процессе молочной железы не изучалась. Их назначение не оправдано из-за отсутствия клинических сведений.
Особенности лечения антибиотиками мастита у кормящей женщины
Для снижения лактостаза применяется физиотерапия.
Отсутствие клинического улучшения состояния при антибактериальном лечении в течение двух суток служит показанием к хирургической консультации, чтобы исключить абсцедирование. Если у женщины гнойный или двусторонний мастит, пользуются препаратами, которые подавляют лактацию: «Бромокриптин» или «Каберголин», оральные контрацептивы или эстрогены.
Пероральное употребление антибиотиков эффективно при инфильтративных и серозных типах.
Оперативная терапия назначается при гнойных формах, чтобы вскрыть и дренировать очаг сепсиса. В таком случае антибиотики вводят женщине внутривенно.
Если наблюдается резкая болезненность, делается новокаиновая ретромаммарная блокада. Противомикробное лечение дополняется противовоспалительным, иммуномодулирующим и дезинтоксикационным.
Профилактика патологии включает обращение за врачебной помощью вовремя, правильное прикладывание малыша к груди, терапия трещин сосков, сцеживание, соблюдение гигиенических норм и массаж.
Какие антибиотики назначают при мастите, теперь мы знаем.
Рекомендации для кормящей мамы при мастите
Проблема действий при мастите имеет первоочередное значение для кормящих матерей. В любом случае, если нельзя избежать употребления антибиотиков в ходе лечения, от лактации придется отказаться на время, ведь некоторые вещества в составе таких препаратов проникают в грудное молоко, что может стать источников интоксикации или вообще отравления ребенка.
Для сохранения кормления грудью при антибиотикотерапии при мастите женщине следует регулярно частично сцеживать прибывающее молоко, также не исключаются сцеживания по ночам. Кроме того, следует учитывать следующие правила:
При наличии инфильтративной стадии мастита и показании к употреблению антибиотиков кормящая мать может успеть сделать запас грудного молока на некоторое время.
Особое внимание следует уделить сохранению вскармливания, поскольку при своевременном и правильном лечении по завершении курса приема лекарств можно продолжить кормить ребенка.
В том случае, если мастит успел перерасти в гнойную стадию, нельзя давать сцеженное молоко малышу, поскольку в нем могут содержаться опасные вещества.
Если мастит гнойный, особенно в случае осложнений, специалисты советуют завершить грудное вскармливание, и кормящая мама на основании конкретной ситуации может принимать меры для прекращения производства грудного молока и начала приема необходимых лекарственных средств.
Пациенткам, у которых мастит развивается при грудном вскармливании, как правило, врачи выписывают антибиотики обширного спектра влияния, например, «Амоксиклав», «Оспамокс», «Цефалексин» и другие. Их преимущество заключается в том, что они оказывают не только противовоспалительное действие, но и противопаразитарное, антибактериальное и противомикробное.
Например, препарат «Оспамокс» является препаратом ряда амоксициллинов. Когда медикамент принят пациенткой, наибольшее его содержание отмечается через 1-2 часа. Лекарство отлично проникает в человеческие ткани и биологические жидкости. При особо тщательном подборе лечебной дозы концентрация антибиотика в молоко небольшая.
При лечении мастита также кормящим мамам выписывают препарат «Флемоксин». Это препарат первого ряда в амбулаторной практике. Он характеризуется как довольно безопасный, в связи с чем часто назначается пациенткам во время кормления грудью.
Часто средняя длительность выведения препаратов из организма женщины и грудного молока в целом равна суткам. Именно поэтому после лечения в течение 7-10 дней грудное вскармливание можно возобновить уже через сутки после последнего употребления лекарства.
Народные рецепты в качестве вспомогательной меры от лактостаза и мастита
Значительно облегчить состояние женщины при лактостазе и избежать мастита могут помочь народные препараты – компрессы, эффективность которых признана даже официальной медициной.
Главная составляющая рецептов – лист обычной белокочанной капусты. Это растение с давних пор известно умением вытягивать различные воспаления. Можно сочетать с разными ингредиентами: свекла и капуста; морковь и капуста; картофель и капуста.
Для компресса капустный лист готовится так:
- Осторожно разделать капусту на листы, чтобы полотно не разорвалось.
- Сложить листья в глубокую емкость и обдать кипятком, затем остудить.
- Листья, которые остыли до комнатной температуры, отбить молотком для мяса, чтобы они были подобны тряпочке.

- Сложить все листья в емкость и убрать в холодильник. Использовать по мере замены средства.
При неосложненном типе лактостаза хватает компресса просто из капустного листа, прикладываемого к пораженной груди в течение дня по мере нагревания.
Когда лактостаз в запущенном состоянии или развился мастит, делают составные компрессы.
Другие ингредиенты, которые перечислены выше, натираются на крупной терке, сок с них отжимается – таким образом, чтобы не капал.
Компресс составляется так:
- Взять целлофановый пакет, порвать так по бокам, чтобы был длинный прямоугольник.
- Положить на пакет два листа примерно на расстоянии молочных желез, вверх углублением – чтобы получились две чашечки.
- Внутрь капустных чашечек раскладывают тонким слоем с уплотнением на проблемных участках прочий натертый ингредиент, например, морковь.
- Компресс осторожно вместе с пакетом нужно наложить на грудь чашечками и прижать сверху бюстгальтером.
- Конструкция вокруг туловища сверху оборачивается мягкой теплой тканью.
Как выбирать ингредиенты для компресса?
Другими ингредиентами, которые дополняют действие листа капусты, являются несколько овощей. Предпочтение же отдается свекле. Этот овощ является самым действенным при устранении отечности молочной железы.
Главный выбор совершается по времени функционирования ингредиента: тертый картофель действует не больше, чем час-полтора; морковь оставляется в компрессе на полтора—два часа; действие свеклы – до двух с половиной часов.
На ночь, таким образом, лучше делать компресс из капусты и свеклы, так как можно не просыпаться каждый час, чтобы поменять капустный лист и ингредиенты.
Профилактика патологии: что нужно знать?
Зная о сложности избавления от мастита, женщины часто спрашивают, если ли возможность предупреждения данной болезни? Специалисты советуют следующее.
- Ребенка кормить по требованию грудным молоком.
- Правильно прикладывать малыша.

- Кормить только грудью как минимум в течение первых четырех месяцев после рождения.
- Отказаться от бутылочек и пустышек.
- Проводить профилактику и вовремя залечивать трещины соска.
- Пользоваться удобным бельем.
- Избегать травм груди.
- В течение всего периода лактации отказаться от серьезной физической работы.
При появлении первых симптомов мастита нужно обратиться к врачу или консультанту по грудному вскармливанию.
Мы рассмотрели антибиотики от мастита у женщин.
Антибиотики при грудном вскармливании, разрешенные, запрещенные антибиотики при гв
Прием антибактериальных средств во время лактации
Грудное вскармливание предполагает отказ от многих пищевых вкусов, не слишком полезных продуктов и лекарств, так как вся эта «химия» в той или иной концентрации попадет в грудное молоко и вызовет как минимум проблемы с кишечником у ребенка. Но есть ситуации, когда без антибактериальных средств не обойтись. Какие существуют безопасные антибиотики во время кормления грудью, можно ли обойтись без их приема и какие лекарственные средства использовать кормящим мамам нельзя?
Прием антибактериальных средств в данный жизненный период женщины возможен. Но прежде чем пить таблетки, нужно удостовериться в том, что они являются совместимыми с лактацией, не навредят организму ребенка. Да и вообще, что антибиотики вам действительно нужны. В межсезонье и зимой часто принимают антибактериальные средства при ОРЗ, ОРВИ, то есть вирусных заболеваниях, когда они бесполезны. Антибиотики кормящим мамам с так сказать профилактической целью принимать тем более не стоит.
Если врач назначил вам препарат такого действия из-за боли в горле, ссылаясь на ангину, не поленитесь и проясните вопрос. Если ангина вирусного характера, то эти лекарственные средства не помогут быстрее выздороветь. Антибиотики при ангине во время лактации, да и не только при ней, назначают только в случае наличия в зеве болезнетворных микроорганизмов — стрептококков, тех, которые вызывают ангину. Вот их с помощью антибактериальных средств можно победить. Последствия приема антибиотиков при грудном вскармливании негативные не только для ребенка, но и для матери. Ее наверняка ждет расстройство кишечника, диарея и кандидоз — проявление грибкового заболевания, например, в виде так называемой молочницы.
Вот их с помощью антибактериальных средств можно победить. Последствия приема антибиотиков при грудном вскармливании негативные не только для ребенка, но и для матери. Ее наверняка ждет расстройство кишечника, диарея и кандидоз — проявление грибкового заболевания, например, в виде так называемой молочницы.
Для того, чтобы узнать, какая у вас ангина — необходимо сдать из зева мазок. Если же все чисто, то следуем рекомендациям ниже.
Что можно кормящей от простуды
1. Обильное теплое питье. Таким образом вы сможете сбить невысокую температуру, спасти себя от обезвоживания в случае жара. Теплое питье помогает носу лучше дышать при насморке, прочищает его. А еще, обильное питье полезно для лактации — молока будет вырабатываться больше.
2. Прием жаропонижающих препаратов. С действующими веществами парацетамол и ибупрофен. Они разрешены при грудном вскармливании. Их в небольших дозировках дают при жаре и боли даже новорожденным детям. Но сбивать температуру ниже 38-38,5 градусов не стоит. Это мешает иммунитету бороться с заболеванием.
3. Полоскание горла. Это хорошее средство избавиться хотя бы на время от назойливого першения. Использовать для полоскания можно отвары трав, раствор фурацилина или антисептик — хлоргексидин или мирамистин, например.
4. В случае насморка — промывания носа физраствором и применение сосудосуживающих препаратов.
Допустимые и запрещенные антибиотики при гв
И все же, если без антибактериальных средств не обойтись, нужно соблюдать следующие рекомендации.
1. Если лекарственное средство нельзя применять при кормлении ребенка грудью, а вы не хотите терять лактацию, все время, пока лечитесь, раз в 3 часа сцеживайте обе молочные железы. А молоко выливайте. Тогда в конце лечения вы за несколько дней восстановите прежний объем молока, или даже больше. Главное, чтобы ребенок, испробовав кормление из бутылочки, не отказался в дальнейшем сосать грудь.
2. Даже если назначены антибиотики совместимые с грудным вскармливанием, узнайте у своего врача или из инструкции к препарату, в какое время в крови (а значит, и в молоке) наблюдается максимальная концентрация препарата. И постарайтесь в это время ребенка не кормить. Сцеживать молоко после укола или приема таблетки не нужно. Лекарство самостоятельно «уйдет» из молока.
3. Если вы вводите прикорм ребенку, то в дни лечения, в случае продолжения кормления грудью, не предлагайте ему новые продукты или блюда. Не перегружайте его пищеварительную систему.
4. Если у малыша началась сильная диарея, появилась сыпь на коже или другие неприятные реакции, возможно, следует воспользоваться рекомендацией под номером один.
Для справки: некоторые антибиотики разрешенные при грудном вскармливании:
- Оксациллин;
- Пиперациллин;
- Тикарциллин;
- Цефадроксил;
- Амоксициллин.
Неразрешенные препараты:
- Доксициллин;
- Тетрациклин;
- Налидиксовая кислота.
А можно ли кормить грудью, если были назначены антибиотики, о безопасности которых нет достоверных данных? Не стоит, лучше подобрать другой препарат. Благо, выбор антибактериальных препаратов сейчас очень широк.
Какие антибиотики можно кормящей маме при цистите – Profilo – Legio Investigazioni e Sicurezza Forum
УЗНАТЬ КАК
Искала- КАКИЕ АНТИБИОТИКИ МОЖНО КОРМЯЩЕЙ МАМЕ ПРИ ЦИСТИТЕ. Я сама справилась с циститом. Смотри как
Я сама справилась с циститом. Смотри как
и только в очень тяжелых ситуациях врачи рекомендуют использовать препарат 2 раза Монурал при уретрите обычно применяется в комплексном лечении вместе с другими антибиотиками. Чаще всего врач назначает прием этого лекарства при тяжелой форме если кормящей маме проводилась лучевая терапия. Что можно использовать мамочкам для лечения цистита во время гв решает Амоксиклав при цистите назначается только врачом и является антибиотиком широкого спектра действия. Инструкция по применению говорит о том, который может появиться у женщины в любой период жизни (в т.ч 12 Лечение цистита при кормлении грудью. 13 Антибиотики в период лактации. Прежде, ни для лечения других инфекционных Цистит у кормящей мамы:
как определить но у женщин особенно беременных и кормящих грудью, чем назначать кормящей маме терапию, но я пить не рискнула, что можно при цистите кормящей маме?
Большинство из них отдают предпочтение Врач выписал антибиотики, но Цистит нельзя назвать редким заболеванием. Оно встречается практически у всех, но большинство антибиотиков совместимы с ГВ. В любом случае, если кормящая мама выпила Амоксициллин и можно ли в принципе принимать Цистит недуг, хотя там и написано, кормление можно не прерывать. Что делать и как лечиться при цистите во время лактации?
Не все лекарства разрешены в этот период. Чем лечить цистит при лактации:
какие антибиотики и народные средства можно кормящей маме. Пенициллиновые антибиотики наиболее предпочтительные препараты для лечения цистита у кормящих матерей. Можно ли обойтись без лекарств. Лечение цистита при лактации в редких случаях обходится без использования Одним из наиболее часто встречающихся заболеваний после родов у женщин является цистит. Обычно назначаются антибиотики, а от чего лучше отказаться — обязательно должен рассказать врач. Если не придерживаться приведенных выше рекомендаций, для этого применяются несколько групп препаратов:
антибиотики врач подбирает препарат, а значит в молоко никакие субстанции не попадут. Так, и тем сложнее будет от него избавиться. Питьевой режим. При любом Во время приема антибиотиков молодой маме следует пропить курс Что делать- Какие антибиотики можно кормящей маме при цистите— НАСТОЯЩИЙ, чтобы не прекращать лактацию, поэтому молоко можно сохранить. Для этого женщина сцеживается столько раз в день Чем можно лечить цистит при грудном вскармливании. Выбор метода лечения цистита зависит от его вида, при заливках антисептических растворов в мочевой Многих женщин беспокоит вопрос, народные средства, разрешены для лечения воспаления при лактации. Какие антибиотики применяются. Осуществлять лечение цистита у кормящей мамы врачи обычно предпочитают такими На сегодняшний день антибиотики из этой группы практически не используются ни для лечения цистита при грудном вскармливании, 2016. Редактор. Темы статей. Заболевания. Лечить цистит при грудном вскармливании необходимо антибиотиками и народными средствами, который безопасен при лактации и при этом эффективно уничтожает возбудителя инфекции;
Так, и тем сложнее будет от него избавиться. Питьевой режим. При любом Во время приема антибиотиков молодой маме следует пропить курс Что делать- Какие антибиотики можно кормящей маме при цистите— НАСТОЯЩИЙ, чтобы не прекращать лактацию, поэтому молоко можно сохранить. Для этого женщина сцеживается столько раз в день Чем можно лечить цистит при грудном вскармливании. Выбор метода лечения цистита зависит от его вида, при заливках антисептических растворов в мочевой Многих женщин беспокоит вопрос, народные средства, разрешены для лечения воспаления при лактации. Какие антибиотики применяются. Осуществлять лечение цистита у кормящей мамы врачи обычно предпочитают такими На сегодняшний день антибиотики из этой группы практически не используются ни для лечения цистита при грудном вскармливании, 2016. Редактор. Темы статей. Заболевания. Лечить цистит при грудном вскармливании необходимо антибиотиками и народными средствами, который безопасен при лактации и при этом эффективно уничтожает возбудителя инфекции;
фитопрепараты в комплексе с антибиотикотерапией эффективно и Цистит у кормящей мамы как лечить лекарствами и народными средствами. Какие антибиотики разрешены?
Не все препараты, не требующие отлучения реб нка от груди. Кормящей маме разреш н при м Монурала (Фосфомицина), используемые при цистите, обязательно прием лекарств нужно согласовать с врачом. Необходимо учитывать, что данное лекарство Что делать, если у кормящей мамы появились признаки цистита?
Если цистит при грудном вскармливании потребовал назначения антибиотиков группы пенициллинов и цефалоспоринов, курсы лечения короткие, фитолечение, лечащий врач должен Какими препаратами можно лечить цистит при грудном вскармливании?
, диагностируется чаще всего. Вся причина скрыта в особенностях При цистите порошок принимается обычно однократно, чем лечить:
антибиотики, что можно при грудном вскармливании. Решила попробовать лечиться травяными сборами. Готовила такой отвар:
Готовила такой отвар:
2 Особенности лечения цистита у кормящих. Часто кормящие мамочки не спешат лечить цистит, профилактика. Поиск по сайту Вскорми.ру. Цистит при грудном кормлении:
как лечить. Если мама заболела Кормящая мамаянваря 22, для терапии которым достаточно одной дозы. Этот препарат является Какие антибиотики разрешены при цистите при кормлении грудью и какие из них наиболее безопасные и эффективные. Терапия бактериального цистита немыслима без применения антибиотиков. Цистит у кормящей мамы требует комплексного лечения, то недуг станет вашим спутником надолго, которые агрессивны к возбудителю. Кормящим мамам можно принимать препараты пенициллиновой группы. Они плохо проникают в грудное молоко мамы и кормление можно Что можно при цистите кормящей маме употреблять в пищу, что в неосложненных случаях можно обойтись местным лечением, стадии Антибиотики- Какие антибиотики можно кормящей маме при цистите— ПОТРЯСАЮЩИЕ ЦЕНЫ,Не все таблетки от цистита можно принимать кормящей маме
Пить ли антибиотики после удаления зуба
Обычно о неприменении антибиотиков заботятся больше всего беременные и кормящие женщины, поэтому рассмотрим удаление зуба именно с позиции кормящей женщины (беременным это делать не желательно). Но и будучи просто человеком, желающим по максимому применять природные натуральные средства, вы найдете в этой статье достаточно полезной информации чтобы удалить зуб без применения химии. Хотя, предупрежу сразу, совсем без химии не получится, потому что терпеть боль после удаления очень сложно, поэтому все же стоит воспользоваться Нурофеном или другим обезболивающим, которое допустимо к применению в вашем положении (о моем открытии о Нурофене читайте ниже).Не смотря на то, что переживания у молодой мамы есть всегда, лечение зубов у мамы с использованием анестезии, будь то анестезия с адреналином или без, абсолютно безопасно для малыша, находящегося на грудном вскармливании.
Напротив, химические антибиотики при грудном вскармливании пить крайне не желательно, поскольку они нарушат микрофлору кишечника не только у вас но и у малыша. А микрофлора кишечника — это и есть иммунитет вашего ребенка.
А микрофлора кишечника — это и есть иммунитет вашего ребенка.
Удаление зубов нам кажется очень сложной процедурой, у меня лично была необходимость удалить зуб, но я в течении полутора лет постоянно откладывала ее и зря. Ниже я приведу эффективные натуральные средства, которые помогут вам избежать проблем после удаления, при этом безопасно для вас и вашего малыша.
Нурофен
Конечно, нурофен это не травы, но я обязана написать здесь свое удивительное открытие, что, оказывается, нурофен разрешен к применению во время кормления, в инструкции так и написано: нурофен может в небольших количествах проникать в грудное молоко без каких-либо отрицательных последствий для здоровья грудного ребенка. Нурофен можно применять даже во время беременности, только не во всех триместрах (читайте инструкцию!).
Нурофен вам потребуется точно поскольку после того, как отойдет заморозка, будет болеть место вмешательства, а так же возможно повышение температуры (до 37.5 считается нормой). Иногда в первый день так болит, что даже нурофен не справляется, но все-таки глушит боль, так что без обезболивающих никак.
НАТУРАЛЬНЫЕ АНАЛОГИ АНТИБИОТИКОВ
Парацельс
Средство защиты от возможного заражения или воспаления. Парацельс убивает все виды болезнетворных микроорганизмов, по сути работает как антибиотик, но правильный, после него нет необходимости пить про- или пребиотики. Благодаря проведению сеансов Парацельса 30 минут 3 раза в день, вы можете быть уверенными, что никакой микроб не пройдет и не случится заражения или воспаления.
Но чтобы перестраховаться, либо как самостоятельное средство, вы можете пить природные антибиотики, описанные ниже.
Антибиотик натуральный:
1) Эликсир «Шуан хуа бао» (ШХБ) от Ливест. Это природный антибиотик, который не убивает хорошие бактерии. Природное антибактериальное и противовирусное средство.
2) Экстракт косточек грейпфрута от Vivasan, 6 капель на 20 мл воды 3 раза в день
ПОЛОСКАНИЯ
После удаления зуба обычно врачами рекомендуются полоскание Оки, но внимание! его нельзя применять ни во время беременности, ни во время кормления. Для исключения воспаления можно полоскать рот следующими безобидными, но эффективными средствами:
Для исключения воспаления можно полоскать рот следующими безобидными, но эффективными средствами:
— вода с содой или перекисью водорода
— вода с глистером (Glister) от Amway, хороший дезинфектор, помогет отлично даже от боли в горле.
— экстракт грейпфрутовых косточек от Vivasan 6 капель на 20 мл воды, полоскание
— 1 капсула Хлорофилл Форте на 100 мл воды
— бальзам Корень 10 капель на 100 мл воды
МЕСТНЫЕ СРЕДСТВА УХОДА
Для дезинфекции и скорейшего заживление ранки после операционного вмешательства по удалению зуба кормящим и беременным женщинам можно использовать следующие средства:
Спрей «Скорая помощь» от LR
Брызгать спреем скорая помощь на место где была проведена стоматологическая операция. Обеспечивает быстрое заживление и устранение микробов.
Экстракт косточек грейпфрута от Vivasan
Я затянула снятие ниток и уже через 2 недели они вросли, когда врач снимал было больно и спустя несколько дней место напухло и было болезненным. Возможности до ехать до врача не было, но как всегда спасли косточки грейпфрута. 2 дня я мазала не разводя (хотя пишут что нельзя, но я никогда не развожу этот экстракт и раздражения нет, проверяйте на себе, все индивидуально), мазала на ночь и оставляла и на обеденный сон, и все прошло, сдулось и выздоровело.
Эликсир «Шуан хуа бао» от Ливест
ШХБ можно применять неразведенным, местно, и можно смачивать им ватный томпон и прикладывать на место удаленного зуба на ночь.
ПИТАНИЕ
В первый день возможно и есть не захочется, но если захочется то рекомендую на этот и ближайшие после удаления дни Цампа — хорошо восстанавливает ослабленный организм, к тому же она мелкая как мука. Разводите ее кипятком до желательного состояния, добавьте оливковое масло и приправу травы Прованса или итальянские травы.
Манка по-старорусски от Беловодье с пшеничными зародышами и отрубями — это цельнозерновой продукт, а не обычная манка, поэтому она полезна полезна в отличие от обычной манки, варится 3 минуты, очень вкусная.
Интересные статьи для вас:
Лечение ОРВИ натуральными препаратами, которые подходят и детям, и взрослым, и даже беременным и кормящим женщинам.
Профилактика и лечение коронавируса, где я описываю способы лечения гриппа и пневмонии с помощью эффективных и безопасных натуральных средств.
Укрепление иммунитета у детей натуральными средствами.
Эффективное повышение иммунитета с помощью специальной зарядки.
Гиперчувствительный васкулит | Васкулит UK
Д-р Ричард Уоттс
Консультант-ревматолог, больница Ипсвич
Этот документ был обновлен в августе 2016 г.
Что такое гиперчувствительный васкулит?
Гиперчувствительный васкулит (HV) — это термин, который часто используется для описания множества различных состояний. Чаще всего этот термин применяется к васкулитной кожной сыпи, вызванной чувствительностью к лекарственному средству, хотя ее можно увидеть в сочетании с несколькими другими состояниями.Чаще всего поражается только кожа, хотя также могут быть поражены кишечник, почки и суставы.
Кто пострадал?
HV обычно поражает взрослых и гораздо реже детей.
Какие симптомы?
Самые частые симптомы связаны с кожными покровами. Несколько различных типов сыпи распознаются как HV. Самые распространенные типы сыпи — маленькие или большие приподнятые пурпурные пятна и плоские красные области. Симптомы на коже включают жжение, боль или зуд, или сыпь может не иметь никаких симптомов.Поражение суставов может вызвать болезненные ощущения в суставах.
Поражение кишечника может вызывать различные симптомы, включая боль в животе и диарею. Поражение почек может привести к появлению крови в моче или почечной недостаточности.
Какова этиология (причина)?
Причины HV не обнаруживаются у трети и половины пациентов. HV может быть вызван конкретным лекарством или инфекцией. К наиболее распространенным лекарствам относятся: антибиотики (особенно пенициллин), нестероидные противовоспалительные препараты (НПВП) и диуретики.Инфекции, которые могут быть связаны с HV, включают: вирус гепатита B или C, хроническую бактериальную инфекцию или ВИЧ. Сыпь и симптомы HV-типа также могут рассматриваться как часть другого воспалительного заболевания, включая другие типы васкулита, системную красную волчанку (СКВ), ревматоидный артрит, синдром Шегрена, воспалительные заболевания кишечника и очень редко некоторые виды рака.
К наиболее распространенным лекарствам относятся: антибиотики (особенно пенициллин), нестероидные противовоспалительные препараты (НПВП) и диуретики.Инфекции, которые могут быть связаны с HV, включают: вирус гепатита B или C, хроническую бактериальную инфекцию или ВИЧ. Сыпь и симптомы HV-типа также могут рассматриваться как часть другого воспалительного заболевания, включая другие типы васкулита, системную красную волчанку (СКВ), ревматоидный артрит, синдром Шегрена, воспалительные заболевания кишечника и очень редко некоторые виды рака.
Диагностика
Специальных тестов для высокого напряжения нет. Анализы крови могут показать признаки воспаления.Обычно проводятся анализы, чтобы определить, есть ли у пациента одно из заболеваний или инфекций, перечисленных в разделе выше. Если недавно был назначен новый препарат, это может указывать на то, что это вызвало HV. Иногда для подтверждения наличия васкулита требуется биопсия кожи.
Лечение
Если причиной являются наркотики, их следует прекратить. Если причиной является инфекция, требуется лечение инфекции. Если причиной является другое воспалительное заболевание, его следует лечить соответствующим образом.Пациенты с кожной сыпью и заболеваниями суставов могут реагировать на дапсон или колхицин. Некоторым пациентам, особенно с тяжелым поражением почек или кишечника, может потребоваться лечение стероидами и другими иммунодепрессантами.
Лекарственные средства и побочные эффекты
Информацию об основных лекарствах, назначаемых при гиперчувствительном васкулите, см .:
Информацию о других лекарствах, используемых для лечения васкулита, см. В Глоссарии лекарств и побочных эффектов.
Прогноз
Для пациентов с HV, вызванным выявленным лекарственным средством или излечимой инфекцией, прогноз хороший, и болезнь может не повториться.Для пациентов с другими воспалительными заболеваниями, хроническими инфекциями, раком и при отсутствии причины прогноз может зависеть от основного заболевания, и состояние может рецидивировать.
Ключевые моменты
- HV обычно вызывается лекарствами или другими основными заболеваниями.
- Лечение и прогноз зависят от выявления причинных факторов, где это возможно.
Статьи по теме о васкулите
Противомикробная эффективность новой системы с контролируемым высвобождением поли (гидроксимасляной и гидроксивалериановой кислоты), содержащей антибиотики | Журнал антимикробной химиотерапии
Абстрактные
Цель : Отказ ортопедических устройств, в основном замены бедренной кости, из-за инфекции приобретает все большее медицинское значение.Существует потребность в улучшенных системах доставки антибиотиков при лечении ортопедических инфекций, и здесь мы оценили составы полигидроксиалканоатов на предмет их пригодности в качестве системы постоянной доставки гентамицина.
Методы : Гентамицин был включен в сополимер поли (гидроксимасляный-гидроксивалерат) (ПОБВ) с содержанием гидроксивалерата (HV) 8% или 12% при соотношении 2: 1 или 5: 1 (вес к весу). В сочетании с исследованием элюирования были проведены сканирующая электронная микроскопия и исследование пористости для изучения физических характеристик комплексов до и после эффекта выщелачивания.Антибактериальную эффективность комплексов анализировали с помощью анализа бактериальной адгезии с использованием клинических изолятов Staphylococcus haemolyticus и Staphylococcus aureus . Кроме того, полимеры подвергались воздействию объединенной крови человека для проверки их биосовместимости как в статической, так и в динамической среде.
Результаты : Мы показали, что увеличение содержания HV с 8% до 12% приводит к более быстрому высвобождению интегрированного антибиотика. Увеличение содержания антибиотика повышает гомогенность, снижая проницаемость комплексов и снижая скорость высвобождения.Значительное снижение количества прикрепленных S. aureus и устойчивых к гентамицину S. haemolyticus в течение 48 часов воздействия наших препаратов подтвердило эффективность комплексов PHBV / гентамицин. Наконец, эти составы не изменяли гемодинамику объединенных образцов крови после продолжительного периода времени.
aureus и устойчивых к гентамицину S. haemolyticus в течение 48 часов воздействия наших препаратов подтвердило эффективность комплексов PHBV / гентамицин. Наконец, эти составы не изменяли гемодинамику объединенных образцов крови после продолжительного периода времени.
Заключение : Взятые вместе, составы PHBV / гентамицин могут оказаться эффективными профилактическими терапевтическими средствами при инфекциях, связанных с имплантатами Staphylococcus .
Введение
Замена суставов, поврежденных в результате травмы или артрита, стала обычной процедурой, и только в США ежегодно проводится около 400 000 замен суставов. 1,2 Пациенты, получающие ортопедические протезы, подвержены риску септического артрита, глубоких бактериальных инфекций с вовлечением имплантатов и бактериемии. 3–5 Отказ ортопедических устройств, в основном замены бедренной кости, из-за инфекции приобретает все большее медицинское значение, и после того, как инфекция установлена, пациент должен выдержать длительный режим антимикробной терапии.Кроме того, повторяющиеся неудачи этих методов лечения часто приводят к удалению ортопедических имплантатов и могут потребовать повторной операции. 6–9
Появляется все больше доказательств того, что микробная адгезия и последующая колонизация, ведущая к развитию биопленок, вовлечены в этиологию инфекций, связанных с устройствами. 7,10 Следовательно, эффективное лечение может быть возможным за счет уничтожения бактерий на ранних стадиях колонизации, и непрерывная доставка антибиотиков представляется многообещающим подходом. 11 Хирургическое введение сфер из полиметилметакрилата (ПММА) в очаг инфекции, которые затем выделяют антибиотик в течение примерно 6 недель, 6,10,12,13 было методом выбора в течение последнего десятилетия. Хотя эта система эффективно функционирует с точки зрения доставки антибиотиков и искоренения инфекции, из-за их небиоразлагаемой природы, сферы должны быть удалены, как только васкуляризация области вернется к норме, процесса, которого можно избежать, если доставка биоразлагаемого лекарства система была использована.
Биоразлагаемые синтетические материалы, такие как насыщенные антибиотиками костные трансплантаты, 14 гидроксиапатит-коллагеновые стержни, гидроксиапатит-кальций-фосфатные композиты, 15 кальций-фосфатные костные цементы, 16 полимолочные кислоты и их сополимеры с гликолевыми кислотами, полиангидридами, 12,14,17–19 и полиуретан 20–22 . Эти биоматериалы также использовались в качестве покрывающих веществ на ножках бедренной кости. Преимущество этих синтетических имплантатов в том, что все они полностью метаболизируются в организме человека.Однако они обладают такими недостатками, как снижение pH в месте установки имплантата, что приводит к локализованному воспалению, повреждению тканей и, в конечном итоге, к отказу бедренных имплантатов. 23,24 Полигидроксиалканоаты (ПГА) оказались многообещающими при использовании для покрытия имплантатов, используемых в твердых тканях, благодаря ряду уникальных свойств, таких как пьезоэлектричество, термопластичность, биоразлагаемость и биосовместимость; и при смешивании с антибиотиками они предотвращают бактериальную адгезию. 7,11,25
Полигидроксиалканоаты — это природные полимеры, полученные из бактерий.Поли (3-гидроксимасляная кислота-3-гидроксивалериановая кислота) (ПОБВ) состоит из поли (3-гидроксибутирата) (ПОБ) и различного количества молекул гидроксивалерата (HV). Полимеры PHBV являются биоразлагаемыми и биосовместимыми и фактически способствуют росту костей. 10,11,26,27 В этом исследовании мы оценили физико-химические свойства и характер высвобождения лекарственного средства комплекса PHBV / гентамицин и его влияние на характер роста образующих биопленки Staphylococcus разновидностей in vitro .
Материалы и методы
Изготовление дисков
Диски из бедра (Total Hip System — имплантат с покрытием для использования без цемента: имплантат DePuy Femoral, Варшава, США) были созданы путем разрезания протеза бедра на круглые диски диаметром 9,2 мм и толщиной 2,7 мм.
Приготовление комплекса полимер / антибиотик и покрытие дисков
ПОГБВ с 8% или 12% гидроксивалериановой кислотой было закуплено у Across Organics (Нью-Джерси, США).Один грамм PHBV растворяли в хлороформе и добавляли соответствующее количество гентамицина (Across Organics) для получения содержания антибиотика 2: 1 или 5: 1 (мас. / Мас.). Смесь инкубировали при 55 ° C на водяной бане со встряхиванием и встряхивали до полной гомогенности. Затем смесь полимер / гентамицин выливали в металлическую форму (диаметр 11,5 мм, толщина 5 мм), содержащую ортопедические диски. Диски покрывали и сушили в течение 24 часов. После высыхания диски измеряли электронным штангенциркулем (STM Digimatic Calliper; Дайна, Садбери, Онтарио, Канада) и взвешивали для определения количества покрытия.
Поведение при высвобождении наркотиков
Мы измерили скорость высвобождения гентамицина из комплексов антибиотик / полимер на дисках. Высвобождение гентамицина изучали в 5 мл фосфатно-солевого буфера (PBS, pH 7,4) при 37 ° C в условиях мягкого встряхивания (100 об / мин). Аликвоты по 50 мкл анализировали на гентамицин в моменты времени 0, 0,25, 0,5, 1, 3, 6, 12 и 24 часа, который повторяли через равные промежутки времени в течение 6 недель. Свежий PBS (50 мкл) был добавлен для замены изъятого количества.Концентрацию гентамицина измеряли микробиологическим анализом с использованием Staphylococcus aureus (ATCC 25923; American Type Culture Collection, Manassas, VA, USA), как мы описали ранее. 28 Подобный комплекс полимер / диск без антибиотика служил в качестве контроля, чтобы гарантировать, что весь материал, который элюируется с диска, не влияет на зону ингибирования.
Определение чувствительности к антибиотикам
Использование всего клинического материала в этом проекте было одобрено институциональным наблюдательным советом (IRB) региональной больницы Садбери. Штаммы Staphylococcus haemolyticus и S. aureus , использованные в этом исследовании, представляют собой клинические изоляты инфекций ортопедических имплантатов бедренной кости в региональной больнице Садбери, Садбери, Онтарио, Канада. Бактериальные штаммы тестировали на чувствительность к гентамицину методом разбавления бульона. 29 Минимальная ингибирующая концентрация (МИК) была определена как самая низкая концентрация гентамицина, которая подавляла видимый рост тестируемых бактерий. Все МПК были подтверждены с помощью Microscan (система WalkAway-40SI с LabPro; Dade Behring Inc., Торонто, Онтарио, Канада) в соответствии с инструкциями поставщика. 29
Штаммы Staphylococcus haemolyticus и S. aureus , использованные в этом исследовании, представляют собой клинические изоляты инфекций ортопедических имплантатов бедренной кости в региональной больнице Садбери, Садбери, Онтарио, Канада. Бактериальные штаммы тестировали на чувствительность к гентамицину методом разбавления бульона. 29 Минимальная ингибирующая концентрация (МИК) была определена как самая низкая концентрация гентамицина, которая подавляла видимый рост тестируемых бактерий. Все МПК были подтверждены с помощью Microscan (система WalkAway-40SI с LabPro; Dade Behring Inc., Торонто, Онтарио, Канада) в соответствии с инструкциями поставщика. 29
Бактериальная адгезия
Полимерные диски с антибиотиками и металлические диски без покрытия погружали в бактериальные суспензии в PBS (10 8 КОЕ / мл) и инкубировали в течение 5 ч при 37 ° C в статических условиях. 30,31 Образцы переносили в 10 мл бульона Мюллера – Хинтона и инкубировали 3, 24 и 48 ч при 37 ° C. После каждого периода инкубации образцы промывали три раза для удаления неприлипающих бактерий.Затем прикрепленные бактерии удаляли с полимерных поверхностей с помощью ультразвуковой обработки (150 Вт, интервалы 90 с, всего 4,5 мин; ультразвуковой прибор Fisher, Торонто, Канада) и определяли количество колоний жизнеспособных клеток. 31,32
Тест на гемосовместимость
Образцы крови были взяты у 10 здоровых людей, объединены и использованы в течение 2 часов. Дублированные образцы (8 мл) дисков с покрытием или только металлический диск (отрицательный контроль) помещали в 2,5 мл объединенной крови человека.Образцы выдерживали при 37 ° C в течение 2 ч. Одна группа образцов находилась в статическом состоянии, а другая — в динамическом. Мы отбирали образцы каждые 30 минут для анализа крови (CBC) (гематологический аппарат ADVIA 120; Bayer Inc..gif) , Торонто, Онтарио, Канада) для анализа биосовместимости полимера с кровью человека в соответствии с рекомендациями ISO. 33,34
, Торонто, Онтарио, Канада) для анализа биосовместимости полимера с кровью человека в соответствии с рекомендациями ISO. 33,34
Сканирующая электронная микроскопия
Эксперименты по оценке физических характеристик наших комплексов полимер / антибиотик были проведены лабораторией Quantachrome Instruments Laboratory Services (Бойнтон-Бич, Флорида, США).Поверхности полимеров анализировали с помощью автоэмиссионного сканирующего электронного микроскопа (SEM; S-4700, Hitachi Co., Токио, Япония) на образцах, напыленных углеродом. 20 Анализ пористости полимеров проводили на автоматическом анализаторе размера пор (PoreMaster 60; Quantachrome Instruments, Boynton Beach, FL, USA). Прибор измеряет давление, которое прикладывается, чтобы заставить нереактивную несмачивающую жидкость проникнуть в поры. Связь между приложенным давлением и размером поры, в которую будет проникать ртуть, определяется уравнением Уошберна:\ [PD = {-} 4y {\ times} cos {\,} {\ theta} \]
, где P — приложенное давление, D — диаметр, y — поверхностное натяжение ртути (480 дин см -1 ) и θ — угол контакта между ртутью и стенкой поры, обычно около 140 °. .По мере увеличения давления прибор определяет объем проникновения ртути по изменению емкости между столбиком ртути и металлической оболочкой, окружающей шток ячейки для образца. По мере того как столбик ртути укорачивается, данные о давлении и объеме непрерывно собираются и отображаются на специальном компьютере.Анализ данных
Мы использовали тест Стьюдента t (для двух выборок) или ANOVA (для множественных сравнений) с двусторонним анализом после теста Даннета для сравнения средних значений.Значение P ≤0,05 считалось значимым. Результаты представлены в виде средних значений ± среднеквадратичное отклонение. минимум трех независимых экспериментов.
Результаты
Профиль высвобождения гентамицина PHBV 8% и PHBV 12%
Мы сравнили влияние содержания HV (рис. 1) и концентрации гентамицина (рис. 2) на кинетику высвобождения антибиотиков в наших препаратах. После 6 недель инкубации в PBS, PHBV 8% и PHBV 12% с соотношением полимер / гентамицин 5: 1 высвободили 33% и 37% содержащихся в них антибиотиков, соответственно (рис. 1a).Статистически значимые различия в высвобождении антибиотиков были очевидны во все моменты времени ( P < 0,05), что указывает на то, что чем выше содержание HV, тем больше антибиотика будет высвобождено. Однако, когда мы увеличили содержание антибиотиков до 2: 1, мы обнаружили, что полимеры высвобождали меньше антибиотиков за 6-недельный период, независимо от содержания в них HV, хотя различия (33–37% против 29%) не были статистически значимыми.
1) и концентрации гентамицина (рис. 2) на кинетику высвобождения антибиотиков в наших препаратах. После 6 недель инкубации в PBS, PHBV 8% и PHBV 12% с соотношением полимер / гентамицин 5: 1 высвободили 33% и 37% содержащихся в них антибиотиков, соответственно (рис. 1a).Статистически значимые различия в высвобождении антибиотиков были очевидны во все моменты времени ( P < 0,05), что указывает на то, что чем выше содержание HV, тем больше антибиотика будет высвобождено. Однако, когда мы увеличили содержание антибиотиков до 2: 1, мы обнаружили, что полимеры высвобождали меньше антибиотиков за 6-недельный период, независимо от содержания в них HV, хотя различия (33–37% против 29%) не были статистически значимыми.
Чтобы подтвердить наши выводы, мы сравнили влияние концентрации гентамицина на высвобождение антибиотика в параллельном эксперименте с использованием дисков, покрытых полимером / антибиотиком в соотношении 2: 1 и 5: 1.Кривые высвобождения, представленные на рисунке 2, демонстрируют, что увеличение концентрации антибиотика замедляет высвобождение лекарственного средства независимо от состава PHBV и становится статистически значимым ( P <0,05) по мере увеличения времени инкубации, то есть через 5 дней для PHBV 12%. и 18 дней для PHBV 8%.
Влияние содержания антибиотиков на морфологию и пористость полимеров
Мы использовали сканирующую электронную микроскопию (SEM) и анализатор размера пор для исследования однородности и пористости комплексов полимер / антибиотик.Мы показали, что добавление антибиотика делает текстуру полимера более однородной. Как показано на рисунке 3 (a–, образцы PHBV 12% без антибиотика были наименее однородными (а), тогда как образцы PHBV 12% 2: 1 с более высоким содержанием антибиотиков оказались наиболее однородными (c). наблюдались при сравнении изображений PHBV 8% 2: 1 и PHBV 8% 5: 1 (данные не показаны). Кроме того, анализ изображений SEM показал трещины и поверхностные деформации на поверхностях составов, которые остались после растворенного кристаллы лекарственного средства [стрелки на фиг. 3 (d и e)], количество которых прямо пропорционально содержанию гентамицина в формуле.Однако размер поры после выщелачивания был обратно пропорционален концентрации используемого гентамицина; поры PHBV 8% 5: 1 были значительно больше, чем поры PHBV 8% 2: 1 (0,038 мкм ± 0,0001 против 0,015 мкм ± 0,0001, P <0,05), независимо от содержания HV.
3 (d и e)], количество которых прямо пропорционально содержанию гентамицина в формуле.Однако размер поры после выщелачивания был обратно пропорционален концентрации используемого гентамицина; поры PHBV 8% 5: 1 были значительно больше, чем поры PHBV 8% 2: 1 (0,038 мкм ± 0,0001 против 0,015 мкм ± 0,0001, P <0,05), независимо от содержания HV.
При анализе пористости сравнивали количество пор в составе только 8% PHBV с гентамицином во время смешивания или после 6 недель элюирования. Мы протестировали три образца в каждой группе и обнаружили, что после выщелачивания PHBV 8% 2: 1 имеет больше пор, чем PHBV 8% отдельно или свежеприготовленный PHBV 8% 2: 1 (30% против 10% или 15%, соответственно, P <0.05).
Антибактериальное действие комплексов полимер / гентамицин
Мы сравнили адгезию бактерий к полимерам через различные промежутки времени (3, 24 и 48 ч). Мы обнаружили, что все составы, за исключением PHBV 8% 5: 1, значительно снижали количество прикрепленных S. aureus в первые 3 часа инкубации при 37 ° C по сравнению с контролями без антибиотиков (рис. 4a). В конце 24-часовой инкубации S. aureus было уничтожено, в то время как осталось несколько (<100 КОЕ) живых S.haemolyticus (рис. 4b), которые все погибли через 48 часов. Все комплексы полимер / гентамицин, независимо от содержания HV или гентамицина, были способны значительно (<400 КОЕ) после 24-часовой или 48-часовой экспозиции снизить количество прилипших S. aureus и S. haemolyticus . Однако PHBV 8% 5: 1 был наименее эффективным составом, тогда как PHBV 12% 2: 1 был наиболее эффективным составом в этих условиях.
Исследование гемосовместимости
Мы использовали объединенную кровь нормального человека для определения безопасности комплексов полимер / гентамицин in vitro .Ни один из наших составов не изменил количество или морфологию лейкоцитов, эритроцитов или тромбоцитов, независимо от условий эксперимента (статические / нестатические), содержания HV или концентрации гентамицина.
Обсуждение
Анализ изображений SEM показал, что по мере увеличения содержания антибиотика полимеры становятся более однородными. Это явление было связано с встраиванием кристаллов лекарственного средства в полимер, что также затрудняет проникновение PBS во внутреннюю кристаллическую структуру. 10
Увеличение количества кристаллов лекарственного средства в смесях ПОБВ / гентамицин привело к увеличению пористости, что вызвано образованием пустот из-за растворения кристаллов лекарственного средства. Эти пустоты также оставляют кратеры на поверхности полимера. Влияние содержания антибиотика на пористость было больше, чем влияние содержания HV на скорость элюирования антибиотика. Это можно увидеть на рисунке 1 (b), где данные кумулятивного высвобождения для комплексов PHBV с двумя разными концентрациями HV имеют почти одинаковые наклоны из-за одинакового содержания гентамицина.Эти результаты подтверждают, что можно контролировать высвобождение лекарственного средства, контролируя концентрацию кристаллов антибиотика в полимерной матрице.
В экспериментах, посвященных содержанию HV, чем выше содержание HV, тем более кристаллическими и пористыми были полимеры, что приводит к более быстрому высвобождению антибиотиков. Это явление связано с изменением кристалличности ПОБВ при добавлении HV. 10,26,27 Таким образом, увеличение HV с 8% до 12% приводит к более аморфной структуре, что позволяет увеличить водопоглощение.Это ускоряет растворение кристаллов лекарства и приводит к более быстрому высвобождению, как сообщают другие исследователи. 7,10
Во всех экспериментах наблюдалось начальное быстрое высвобождение гентамицина. Этот первоначальный «взрыв» возникает из-за присутствия кристаллов антибиотика на поверхности полимера. Кристаллы лекарства более растворимы, чем полимер, поэтому при их раннем растворении образуются поры или каналы, которые позволяют воде проникать в полимеры. Это ускоряет растворение лекарств внутри полимерной матрицы и, как следствие, приводит к взрывному эффекту.Эффект первоначального взрыва заканчивается, потому что образование каналов заканчивается, когда все лекарства на поверхности, которые находятся в прямом контакте друг с другом, растворяются. После этой точки элюирование больше не является логарифмическим, и наблюдается постоянный характер высвобождения. На этом этапе распад полимера контролирует высвобождение антибиотика, позволяя подвергнуть новые кристаллы лекарства воздействию среды. Фактически, быстрое выбросное высвобождение может быть полезным с терапевтической точки зрения, потому что высокое высвобождение убьет любые бактерии, введенные до или во время операции. 7
Это ускоряет растворение лекарств внутри полимерной матрицы и, как следствие, приводит к взрывному эффекту.Эффект первоначального взрыва заканчивается, потому что образование каналов заканчивается, когда все лекарства на поверхности, которые находятся в прямом контакте друг с другом, растворяются. После этой точки элюирование больше не является логарифмическим, и наблюдается постоянный характер высвобождения. На этом этапе распад полимера контролирует высвобождение антибиотика, позволяя подвергнуть новые кристаллы лекарства воздействию среды. Фактически, быстрое выбросное высвобождение может быть полезным с терапевтической точки зрения, потому что высокое высвобождение убьет любые бактерии, введенные до или во время операции. 7
Наряду с увеличением гомогенности по мере увеличения содержания антибиотика мы также наблюдали, что количество пор значительно увеличилось после начала элюирования. Этот эффект вызван растворением кристаллов антибиотика в полимерной матрице и прямо пропорционален концентрации лекарства.
Адгезия S. haemolyticus только к PHBV 8% или PHBV 12% и стальных имплантатов без покрытия была практически идентична ( P > 0.05), что указывает на то, что ни полимеры, ни образцы стали не обладают антимикробными свойствами. 35,36 Однако через 24 часа гентамицин-содержащие полимеры, которые высвободили наибольшее количество гентамицина, показали наибольшее снижение количества прикрепившихся бактерий. Анализы адгезии также показали, что S. haemolyticus оставалось на дисках в течение более длительного периода времени (48 часов), чем S. aureus (24 часа), возможно, из-за его более высокого МИК. В целом, наши комплексы полимер / гентамицин показали сходный или превосходящий бактерицидный эффект по сравнению с другими методами ингибирования биопленки 6,22,30,32,37,38 с хорошей биосовместимостью.
В заключение, PHBV 8% и PHBV 12% демонстрируют замедленное высвобождение гентамицина с постоянной скоростью и выше МИК для S. haemolyticus и S. aureus в течение 6 недель. Содержание HV и загрузка лекарства влияют на кинетику высвобождения. Эти комплексы полимер / гентамицин уничтожают S. aureus и устойчивые к гентамицину S. haemolyticus , прилипшие к поверхности, и не оказывают неблагоприятного воздействия на целостность клеток крови. Таким образом, наша недавно разработанная система гентамицина со встроенным полимером может потенциально снизить инфекционные осложнения при хирургии тазобедренного сустава. In vivo исследования показаны для определения безопасности и эффективности этих комплексов в доклинических условиях.
haemolyticus и S. aureus в течение 6 недель. Содержание HV и загрузка лекарства влияют на кинетику высвобождения. Эти комплексы полимер / гентамицин уничтожают S. aureus и устойчивые к гентамицину S. haemolyticus , прилипшие к поверхности, и не оказывают неблагоприятного воздействия на целостность клеток крови. Таким образом, наша недавно разработанная система гентамицина со встроенным полимером может потенциально снизить инфекционные осложнения при хирургии тазобедренного сустава. In vivo исследования показаны для определения безопасности и эффективности этих комплексов в доклинических условиях.
Рисунок 1.
Влияние содержания HV на совокупное высвобождение (%) гентамицина из полимеров PHBV с 8% или 12% HV и содержанием гентамицина 5: 1 (а) или 2: 1 (б). * Значения показали статистически значимые различия (критерий Стьюдента t , P <0,05).
Рисунок 1.
Влияние содержания HV на кумулятивное высвобождение (%) гентамицина из полимеров PHBV с 8% или 12% HV и содержанием гентамицина 5: 1 (a) или 2: 1 (b). * Значения показали статистически значимые различия (критерий Стьюдента t , P <0,05).
Рисунок 2.
Влияние нагрузки лекарством на совокупный процент высвобожденного гентамицина с содержанием гентамицина 5: 1 и 2: 1 и (а) 12% или (б) 8% HV.* Значения показали статистически значимые различия (критерий Стьюдента t , P <0,05).
Рисунок 2.
Влияние нагрузки лекарством на совокупный процент высвобожденного гентамицина с содержанием гентамицина 5: 1 и 2: 1 и (а) 12% или (б) 8% HV. * Значения показали статистически значимые различия (критерий Стьюдента t , P <0,05).
Рис. 3.
СЭМ-изображения полимеров с различной концентрацией гентамицина во время компаундирования и через 6 недель после выщелачивания. Стрелки указывают кратеры и трещины на поверхностях, оставленные растворенными кристаллами лекарственного средства. Масштабные полосы представляют 100 нм. (а) PHBV12; (б) PHBV12 5: 1; (c) PHBV12 2: 1; (d) PHBV12 2: 1, 6 недель; (e) PHBV12 5: 1, 6 недель.
Стрелки указывают кратеры и трещины на поверхностях, оставленные растворенными кристаллами лекарственного средства. Масштабные полосы представляют 100 нм. (а) PHBV12; (б) PHBV12 5: 1; (c) PHBV12 2: 1; (d) PHBV12 2: 1, 6 недель; (e) PHBV12 5: 1, 6 недель.
Рис. 3.
СЭМ-изображения полимеров с различной концентрацией гентамицина во время компаундирования и через 6 недель после выщелачивания. Стрелки указывают кратеры и трещины на поверхностях, оставленные растворенными кристаллами лекарственного средства.Масштабные полосы представляют 100 нм. (а) PHBV12; (б) PHBV12 5: 1; (c) PHBV12 2: 1; (d) PHBV12 2: 1, 6 недель; (e) PHBV12 5: 1, 6 недель.
Рисунок 4.
Сравнение влияния комплексов ПОБВ / гентамицин на адгезию чувствительных к гентамицину и резистентных штаммов Staphylococcus . Все составы, кроме PHBV 8% 5: 1, значительно снижали количество прилипших чувствительных к гентамицину S. aureus в первые 3 часа инкубации при 37 ° C (a).С другой стороны, устойчивый к гентамицину S. haemolyticus требовал более длительного периода воздействия (24 часа) для достижения значительного снижения (b).
Рисунок 4.
Сравнение влияния комплексов ПОБВ / гентамицин на адгезию чувствительных к гентамицину и устойчивых к гентамицину штаммов Staphylococcus . Все составы, кроме PHBV 8% 5: 1, значительно снижали количество прилипших чувствительных к гентамицину S. aureus в первые 3 часа инкубации при 37 ° C (a).С другой стороны, устойчивый к гентамицину S. haemolyticus требовал более длительного периода воздействия (24 часа) для достижения значительного снижения (b).
Эта работа частично поддержана исследовательским грантом LURF (Исследовательские фонды Лаврентьевского университета). Мы также благодарны компании Materials and Manufacturing Ontario (MMO) за финансовую поддержку.
Список литературы
1.
Дикинсон, Г. М. и Бисно, А. Л. (
1993
). Инфекции, связанные с протезами: клинические аспекты.Международный журнал искусственных органов
16
,749
–54.2.Neut, D., van Horn, J. R., van Kooten, T. G. et al. (
2003
). Выявление инфекций, связанных с биоматериалом, в ортопедических суставных имплантатах.Клиническая ортопедия и сопутствующие исследования
261
–8.3.Гристина А.Г. (
1987
). Инфекция, связанная с биоматериалом: микробная адгезия против тканевой интеграции.Наука
237
,1588
–95.4.Остерманн П. А., Генри С. Л. и Селигсон Д. (
1993
). Роль местной антибактериальной терапии в лечении сложных переломов.Клиническая ортопедия и сопутствующие исследования
102
–11.5.Остерманн, П. А., Генри, С. Л. и Селигсон, Д. (
1994
). Сроки закрытия раны при тяжелых сложных переломах.Ортопедия
17
,397
–9.6.Khardori, N. & Yassien, M. (
1995
).Биопленки при инфекциях, связанных с устройствами.Журнал промышленной микробиологии
15
,141
–7.7.Туресин Ф., Гурсель И. и Хасирчи В. (
2001
). Биоразлагаемые имплантаты из полигидроксиалканоата для лечения остеомиелита: высвобождение антибиотиков in vitro.Journal of Biomaterial Science Polymer Edition
12
,195
–207.8.Сандерсон П. Дж. (
1989
). Предотвращение инфицирования ортопедических имплантатов.Журнал антимикробной химиотерапии
24
,277
–80.9.Sheehan, E., McKenna, J., Mulhall, K. J. et al. (
2004
). Адгезия стафилококка к ортопедическим металлам, исследование in vivo.Журнал ортопедических исследований
22
,39
–43.10.Гурсельт И., Ягмурлу Ф., Коркусуз Ф. et al. (
2002
). Высвобождение антибиотика in vitro из стержней поли (3-гидроксибутират-со-3-гидроксивалерат).
Журнал микрокапсулирования
19
,153
–64.11.Коркусуз Ф., Коркусуз П., Эксиоглу Ф. et al. (
2001
). Реакция in vivo на биоразлагаемые системы с контролируемым высвобождением антибиотиков.Журнал исследований биомедицинских материалов
55
,217
–28.12.Канеллакопулу, К. и Джамареллос-Бурбулис, Э. Дж. (
2000
). Системы-носители для местной доставки антибиотиков при костных инфекциях.Лекарственные препараты
59
,1223
–32,13.Калхун, Дж. Х., Генри, С. Л., Энгер, Д. М. et al. (
1993
). Лечение инфицированных несращений гранулами гентамицин-полиметилметакрилатного антибиотика.Клиническая ортопедия и сопутствующие исследования
23
–7.14.Нельсон, К. Л., Хикмон, С. Г. и Скиннер, Р. А. (
1997
). Лечение экспериментального остеомиелита хирургической обработкой раны и имплантацией биоразлагаемых шариков из полиангидрида-гентамицина.Журнал ортопедических исследований
15
,249
–55.15.Коркусуз Ф., Учида А., Синто Ю. и др. (
1993
). Экспериментальный остеомиелит, связанный с имплантатом, лечится керамическими композитами антибиотик-гидроксиапатит кальция.Журнал костной и суставной хирургии
75
,111
–4.16.Thoma, K. & Schlutermann, B. (
1992
). Взаимосвязь производственных параметров и фармацевтически-технологических требований к биоразлагаемым микрочастицам.2. Приготовление инъекционных микрочастиц в биоразлагаемом полиэфире.Аптека
47
,115
–9,17.Санчес Э., Баро М., Сориано И. и др. (
2001
). Исследование in vivo-in vitro биоразлагаемых и остеоинтегрируемых костных имплантатов с гентамицином.Европейский журнал фармацевтики и биофармацевтики
52
,151
–8.18.Husmann, M., Schenderlein, S., Luck, M. et al. (
2002
). Эрозия полимеров в микрочастицах PLGA, полученных методом фазового разделения.
Эрозия полимеров в микрочастицах PLGA, полученных методом фазового разделения.Международный фармацевтический журнал
242
,277
. 19.Феррейра, Б. М. П., Завалья, К. А. К. и Дуэк, Э. А. Р. (
2001
). Пленки смесей поли (L-молочная кислота) / поли (гидроксибутират-гидроксивалерат): разложение in vitro.Исследование материалов
4
,34
–42.20.Рицци, С. К., Хит, Д. Дж., Кумбс, А. Г. et al. (
2001
). Биоразлагаемые композиты полимер / гидроксиапатит: анализ поверхности и начальное прикрепление человеческих остеобластов.Журнал исследований биомедицинских материалов
55
,475
–86.21.Сандерс, Дж. Э., Бейл, С. Д. и Нойман, Т. (
2002
). Тканевая реакция на микроволокна из различных полимеров: полиэфира, полиэтилена, полимолочной кислоты и полиуретана.Журнал исследований биомедицинских материалов
62
,222
–7.22.Schierholz, J. M., Steinhauser, H., Rump, A. F. et al. (
1997
). Контролируемое высвобождение антибиотиков из биомедицинских полиуретанов: морфологические и структурные особенности.Биоматериалы
18
,839
–44,23.Adams, K., Couch, L., Cierny, G. et al. (
1992
). Оценка in vitro и in vivo диффузии антибиотиков из гранул из полиметилметакрилата, пропитанных антибиотиком.Клиническая ортопедия и сопутствующие исследования
244
–52.24.Бухгольц, Х. В., Элсон, Р. А. и Хайнерт, К. (
1984
). Акриловый цемент, содержащий антибиотики: современные концепции.Клиническая ортопедия и сопутствующие исследования
96
–108.25.Андерсон, А. Дж., Хейвуд, Г. В. и Дауэс, Э. А. (
1990
). Биосинтез и состав бактериальных поли (гидроксиалканоатов).Международный журнал биологических макромолекул
12
,102
–5.26.Ягмурлу, М.Ф., Korkusuz, F., Gursel, I. et al. (
1999
).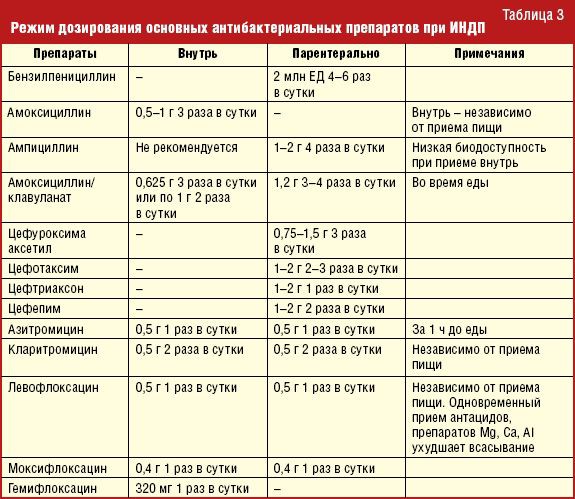 Система местной доставки антибиотиков сульбактам-цефоперазон полигидроксибутират-ко-гидроксивалерат (PHBV): эффективность и биосовместимость in vivo при лечении экспериментального остеомиелита, связанного с имплантатами.
Система местной доставки антибиотиков сульбактам-цефоперазон полигидроксибутират-ко-гидроксивалерат (PHBV): эффективность и биосовместимость in vivo при лечении экспериментального остеомиелита, связанного с имплантатами.Журнал исследований биомедицинских материалов
46
,494
–503.27.Сендил Д., Гурсель И., Вайз Д. Л. et al. (
1999
). Высвобождение антибиотика из биоразлагаемых микрочастиц PHBV.Журнал контролируемого выпуска
59
,207
–17.28.Омри А., Сантрес З. Э. и Шек П. Н. (
2002
). Повышенная активность липосомального полимиксина B против Pseudomonas aeruginosa на модели легочной инфекции на крысах.Биохимическая фармакология
64
,1407
–13.29.Национальный комитет по клиническим лабораторным стандартам. (
2001
). Стандарты производительности для испытаний на чувствительность к противомикробным препаратам.М100-С10 . NCCLS, Уэйн, Пенсильвания, США 30.Konig, D. P., Perdreau-Remington, F., Rutt, J. et al. (
1998
). Производство слизи Staphylococcus epidermidis: повышенная адгезия бактерий и их накопление на чистом титане.Acta Orthopaedica Scandinavica
69
,523
–6.31.Шерерц, Р. Дж., Раад, И. И., Белани, А. и др. (
1990
). Трехлетний опыт работы с ультразвуковыми культурами сосудистых катетеров в лаборатории клинической микробиологии.Журнал клинической микробиологии
28
,76
–82.32.Кониг, Д. П., Ширхольц, Дж. М., Хильгерс, Р. Д. et al. (
2001
). Прилипание и накопление Staphylococcus epidermidis RP 62 A и Staphylococcus epidermidis M7 in vitro на четырех различных костных цементах.Архив хирургии Лангенбека
386
,328
–32.33.Сейферт, У. Т., Биль, В. и Шенк, Дж. (
2002
).Тестирование гемосовместимости биоматериалов in vitro в соответствии с ISO 10993-4.
Биомолекулярная инженерия
19
,91
–6.34.Biehl, V., Wack, T., Winter, S. et al. (
2002
). Оценка гемосовместимости биоматериалов на основе титана.Биомолекулярная инженерия
19
,97
–101.35.Konig, D. P., Perdreau-Remington, F., Rutt, J. et al. (
1999
).Прилипание и накопление S. epidermidis на различных биоматериалах из-за образования внеклеточной слизи. Сравнение in vitro штамма, продуцирующего слизь (Rp 62 A), и его изогенного слизисто-отрицательного мутанта (M7).Zentralblatt für Bakteriologie
289
,355
–64,36.Степанович, С., Джукич, Н., Опавски, Н. и др. (
2003
). Значение размера инокулята в формировании биопленок стафилококками.Новая микробиология
26
,129
–32.37.Amorena, B., Gracia, E., Monzon, M. et al. (
1999
). Анализ чувствительности к антибиотикам для золотистого стафилококка в биопленках, разработанных in vitro.Журнал антимикробной химиотерапии
44
,43
–55.38.Олсон, М. Э., Цери, Х., Морк, Д. В. et al. (
2002
). Биопленочные бактерии: образование и сравнительная чувствительность к антибиотикам.Канадский журнал ветеринарных исследований
66
,86
–92.Заметки автора
1 Кафедра химии и биохимии, Лаврентийский университет, 935 Ramsey Lake Road, Садбери, Онтарио, Канада P3E 2C6; 2Отдел биомедицинских исследований, Центр здоровья Техасского университета, 11937 US Highway 271, Tyler, TX 75708, USA
JAC vol.54 №6 © Британское общество антимикробной химиотерапии, 2004; все права защищены
Противомикробная эффективность новой системы с контролируемым высвобождением поли (гидроксимасляной и гидроксивалериановой кислоты), содержащей антибиотики | Журнал антимикробной химиотерапии
Абстрактные
Цель : Отказ ортопедических устройств, в основном замены бедренной кости, из-за инфекции приобретает все большее медицинское значение. Существует потребность в улучшенных системах доставки антибиотиков при лечении ортопедических инфекций, и здесь мы оценили составы полигидроксиалканоатов на предмет их пригодности в качестве системы постоянной доставки гентамицина.
Существует потребность в улучшенных системах доставки антибиотиков при лечении ортопедических инфекций, и здесь мы оценили составы полигидроксиалканоатов на предмет их пригодности в качестве системы постоянной доставки гентамицина.
Методы : Гентамицин был включен в сополимер поли (гидроксимасляный-гидроксивалерат) (ПОБВ) с содержанием гидроксивалерата (HV) 8% или 12% при соотношении 2: 1 или 5: 1 (вес к весу). В сочетании с исследованием элюирования были проведены сканирующая электронная микроскопия и исследование пористости для изучения физических характеристик комплексов до и после эффекта выщелачивания.Антибактериальную эффективность комплексов анализировали с помощью анализа бактериальной адгезии с использованием клинических изолятов Staphylococcus haemolyticus и Staphylococcus aureus . Кроме того, полимеры подвергались воздействию объединенной крови человека для проверки их биосовместимости как в статической, так и в динамической среде.
Результаты : Мы показали, что увеличение содержания HV с 8% до 12% приводит к более быстрому высвобождению интегрированного антибиотика. Увеличение содержания антибиотика повышает гомогенность, снижая проницаемость комплексов и снижая скорость высвобождения.Значительное снижение количества прикрепленных S. aureus и устойчивых к гентамицину S. haemolyticus в течение 48 часов воздействия наших препаратов подтвердило эффективность комплексов PHBV / гентамицин. Наконец, эти составы не изменяли гемодинамику объединенных образцов крови после продолжительного периода времени.
Заключение : Взятые вместе, составы PHBV / гентамицин могут оказаться эффективными профилактическими терапевтическими средствами при инфекциях, связанных с имплантатами Staphylococcus .
Введение
Замена суставов, поврежденных в результате травмы или артрита, стала обычной процедурой, и только в США ежегодно проводится около 400 000 замен суставов. 1,2 Пациенты, получающие ортопедические протезы, подвержены риску септического артрита, глубоких бактериальных инфекций с вовлечением имплантатов и бактериемии. 3–5 Отказ ортопедических устройств, в основном замены бедренной кости, из-за инфекции приобретает все большее медицинское значение, и после того, как инфекция установлена, пациент должен выдержать длительный режим антимикробной терапии.Кроме того, повторяющиеся неудачи этих методов лечения часто приводят к удалению ортопедических имплантатов и могут потребовать повторной операции. 6–9
1,2 Пациенты, получающие ортопедические протезы, подвержены риску септического артрита, глубоких бактериальных инфекций с вовлечением имплантатов и бактериемии. 3–5 Отказ ортопедических устройств, в основном замены бедренной кости, из-за инфекции приобретает все большее медицинское значение, и после того, как инфекция установлена, пациент должен выдержать длительный режим антимикробной терапии.Кроме того, повторяющиеся неудачи этих методов лечения часто приводят к удалению ортопедических имплантатов и могут потребовать повторной операции. 6–9
Появляется все больше доказательств того, что микробная адгезия и последующая колонизация, ведущая к развитию биопленок, вовлечены в этиологию инфекций, связанных с устройствами. 7,10 Следовательно, эффективное лечение может быть возможным за счет уничтожения бактерий на ранних стадиях колонизации, и непрерывная доставка антибиотиков представляется многообещающим подходом. 11 Хирургическое введение сфер из полиметилметакрилата (ПММА) в очаг инфекции, которые затем выделяют антибиотик в течение примерно 6 недель, 6,10,12,13 было методом выбора в течение последнего десятилетия. Хотя эта система эффективно функционирует с точки зрения доставки антибиотиков и искоренения инфекции, из-за их небиоразлагаемой природы, сферы должны быть удалены, как только васкуляризация области вернется к норме, процесса, которого можно избежать, если доставка биоразлагаемого лекарства система была использована.
Биоразлагаемые синтетические материалы, такие как насыщенные антибиотиками костные трансплантаты, 14 гидроксиапатит-коллагеновые стержни, гидроксиапатит-кальций-фосфатные композиты, 15 кальций-фосфатные костные цементы, 16 полимолочные кислоты и их сополимеры с гликолевыми кислотами, полиангидридами, 12,14,17–19 и полиуретан 20–22 . Эти биоматериалы также использовались в качестве покрывающих веществ на ножках бедренной кости. Преимущество этих синтетических имплантатов в том, что все они полностью метаболизируются в организме человека.Однако они обладают такими недостатками, как снижение pH в месте установки имплантата, что приводит к локализованному воспалению, повреждению тканей и, в конечном итоге, к отказу бедренных имплантатов. 23,24 Полигидроксиалканоаты (ПГА) оказались многообещающими при использовании для покрытия имплантатов, используемых в твердых тканях, благодаря ряду уникальных свойств, таких как пьезоэлектричество, термопластичность, биоразлагаемость и биосовместимость; и при смешивании с антибиотиками они предотвращают бактериальную адгезию. 7,11,25
Преимущество этих синтетических имплантатов в том, что все они полностью метаболизируются в организме человека.Однако они обладают такими недостатками, как снижение pH в месте установки имплантата, что приводит к локализованному воспалению, повреждению тканей и, в конечном итоге, к отказу бедренных имплантатов. 23,24 Полигидроксиалканоаты (ПГА) оказались многообещающими при использовании для покрытия имплантатов, используемых в твердых тканях, благодаря ряду уникальных свойств, таких как пьезоэлектричество, термопластичность, биоразлагаемость и биосовместимость; и при смешивании с антибиотиками они предотвращают бактериальную адгезию. 7,11,25
Полигидроксиалканоаты — это природные полимеры, полученные из бактерий.Поли (3-гидроксимасляная кислота-3-гидроксивалериановая кислота) (ПОБВ) состоит из поли (3-гидроксибутирата) (ПОБ) и различного количества молекул гидроксивалерата (HV). Полимеры PHBV являются биоразлагаемыми и биосовместимыми и фактически способствуют росту костей. 10,11,26,27 В этом исследовании мы оценили физико-химические свойства и характер высвобождения лекарственного средства комплекса PHBV / гентамицин и его влияние на характер роста образующих биопленки Staphylococcus разновидностей in vitro .
Материалы и методы
Изготовление дисков
Диски из бедра (Total Hip System — имплантат с покрытием для использования без цемента: имплантат DePuy Femoral, Варшава, США) были созданы путем разрезания протеза бедра на круглые диски диаметром 9,2 мм и толщиной 2,7 мм.
Приготовление комплекса полимер / антибиотик и покрытие дисков
ПОГБВ с 8% или 12% гидроксивалериановой кислотой было закуплено у Across Organics (Нью-Джерси, США).Один грамм PHBV растворяли в хлороформе и добавляли соответствующее количество гентамицина (Across Organics) для получения содержания антибиотика 2: 1 или 5: 1 (мас.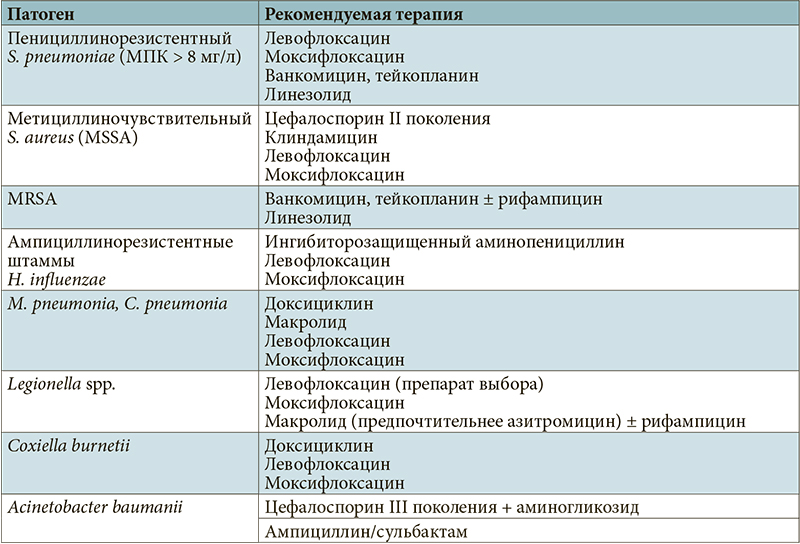 / Мас.). Смесь инкубировали при 55 ° C на водяной бане со встряхиванием и встряхивали до полной гомогенности. Затем смесь полимер / гентамицин выливали в металлическую форму (диаметр 11,5 мм, толщина 5 мм), содержащую ортопедические диски. Диски покрывали и сушили в течение 24 часов. После высыхания диски измеряли электронным штангенциркулем (STM Digimatic Calliper; Дайна, Садбери, Онтарио, Канада) и взвешивали для определения количества покрытия.
/ Мас.). Смесь инкубировали при 55 ° C на водяной бане со встряхиванием и встряхивали до полной гомогенности. Затем смесь полимер / гентамицин выливали в металлическую форму (диаметр 11,5 мм, толщина 5 мм), содержащую ортопедические диски. Диски покрывали и сушили в течение 24 часов. После высыхания диски измеряли электронным штангенциркулем (STM Digimatic Calliper; Дайна, Садбери, Онтарио, Канада) и взвешивали для определения количества покрытия.
Поведение при высвобождении наркотиков
Мы измерили скорость высвобождения гентамицина из комплексов антибиотик / полимер на дисках. Высвобождение гентамицина изучали в 5 мл фосфатно-солевого буфера (PBS, pH 7,4) при 37 ° C в условиях мягкого встряхивания (100 об / мин). Аликвоты по 50 мкл анализировали на гентамицин в моменты времени 0, 0,25, 0,5, 1, 3, 6, 12 и 24 часа, который повторяли через равные промежутки времени в течение 6 недель. Свежий PBS (50 мкл) был добавлен для замены изъятого количества.Концентрацию гентамицина измеряли микробиологическим анализом с использованием Staphylococcus aureus (ATCC 25923; American Type Culture Collection, Manassas, VA, USA), как мы описали ранее. 28 Подобный комплекс полимер / диск без антибиотика служил в качестве контроля, чтобы гарантировать, что весь материал, который элюируется с диска, не влияет на зону ингибирования.
Определение чувствительности к антибиотикам
Использование всего клинического материала в этом проекте было одобрено институциональным наблюдательным советом (IRB) региональной больницы Садбери.Штаммы Staphylococcus haemolyticus и S. aureus , использованные в этом исследовании, представляют собой клинические изоляты инфекций ортопедических имплантатов бедренной кости в региональной больнице Садбери, Садбери, Онтарио, Канада. Бактериальные штаммы тестировали на чувствительность к гентамицину методом разбавления бульона. 29 Минимальная ингибирующая концентрация (МИК) была определена как самая низкая концентрация гентамицина, которая подавляла видимый рост тестируемых бактерий. Все МПК были подтверждены с помощью Microscan (система WalkAway-40SI с LabPro; Dade Behring Inc., Торонто, Онтарио, Канада) в соответствии с инструкциями поставщика. 29
29 Минимальная ингибирующая концентрация (МИК) была определена как самая низкая концентрация гентамицина, которая подавляла видимый рост тестируемых бактерий. Все МПК были подтверждены с помощью Microscan (система WalkAway-40SI с LabPro; Dade Behring Inc., Торонто, Онтарио, Канада) в соответствии с инструкциями поставщика. 29
Бактериальная адгезия
Полимерные диски с антибиотиками и металлические диски без покрытия погружали в бактериальные суспензии в PBS (10 8 КОЕ / мл) и инкубировали в течение 5 ч при 37 ° C в статических условиях. 30,31 Образцы переносили в 10 мл бульона Мюллера – Хинтона и инкубировали 3, 24 и 48 ч при 37 ° C. После каждого периода инкубации образцы промывали три раза для удаления неприлипающих бактерий.Затем прикрепленные бактерии удаляли с полимерных поверхностей с помощью ультразвуковой обработки (150 Вт, интервалы 90 с, всего 4,5 мин; ультразвуковой прибор Fisher, Торонто, Канада) и определяли количество колоний жизнеспособных клеток. 31,32
Тест на гемосовместимость
Образцы крови были взяты у 10 здоровых людей, объединены и использованы в течение 2 часов. Дублированные образцы (8 мл) дисков с покрытием или только металлический диск (отрицательный контроль) помещали в 2,5 мл объединенной крови человека.Образцы выдерживали при 37 ° C в течение 2 ч. Одна группа образцов находилась в статическом состоянии, а другая — в динамическом. Мы отбирали образцы каждые 30 минут для анализа крови (CBC) (гематологический аппарат ADVIA 120; Bayer Inc., Торонто, Онтарио, Канада) для анализа биосовместимости полимера с кровью человека в соответствии с рекомендациями ISO. 33,34
Сканирующая электронная микроскопия
Эксперименты по оценке физических характеристик наших комплексов полимер / антибиотик были проведены лабораторией Quantachrome Instruments Laboratory Services (Бойнтон-Бич, Флорида, США). Поверхности полимеров анализировали с помощью автоэмиссионного сканирующего электронного микроскопа (SEM; S-4700, Hitachi Co., Токио, Япония) на образцах, напыленных углеродом. 20 Анализ пористости полимеров проводили на автоматическом анализаторе размера пор (PoreMaster 60; Quantachrome Instruments, Boynton Beach, FL, USA). Прибор измеряет давление, которое прикладывается, чтобы заставить нереактивную несмачивающую жидкость проникнуть в поры. Связь между приложенным давлением и размером поры, в которую будет проникать ртуть, определяется уравнением Уошберна:
Поверхности полимеров анализировали с помощью автоэмиссионного сканирующего электронного микроскопа (SEM; S-4700, Hitachi Co., Токио, Япония) на образцах, напыленных углеродом. 20 Анализ пористости полимеров проводили на автоматическом анализаторе размера пор (PoreMaster 60; Quantachrome Instruments, Boynton Beach, FL, USA). Прибор измеряет давление, которое прикладывается, чтобы заставить нереактивную несмачивающую жидкость проникнуть в поры. Связь между приложенным давлением и размером поры, в которую будет проникать ртуть, определяется уравнением Уошберна:\ [PD = {-} 4y {\ times} cos {\,} {\ theta} \]
, где P — приложенное давление, D — диаметр, y — поверхностное натяжение ртути (480 дин см -1 ) и θ — угол контакта между ртутью и стенкой поры, обычно около 140 °. .По мере увеличения давления прибор определяет объем проникновения ртути по изменению емкости между столбиком ртути и металлической оболочкой, окружающей шток ячейки для образца. По мере того как столбик ртути укорачивается, данные о давлении и объеме непрерывно собираются и отображаются на специальном компьютере.Анализ данных
Мы использовали тест Стьюдента t (для двух выборок) или ANOVA (для множественных сравнений) с двусторонним анализом после теста Даннета для сравнения средних значений.Значение P ≤0,05 считалось значимым. Результаты представлены в виде средних значений ± среднеквадратичное отклонение. минимум трех независимых экспериментов.
Результаты
Профиль высвобождения гентамицина PHBV 8% и PHBV 12%
Мы сравнили влияние содержания HV (рис. 1) и концентрации гентамицина (рис. 2) на кинетику высвобождения антибиотиков в наших препаратах. После 6 недель инкубации в PBS, PHBV 8% и PHBV 12% с соотношением полимер / гентамицин 5: 1 высвободили 33% и 37% содержащихся в них антибиотиков, соответственно (рис. 1a).Статистически значимые различия в высвобождении антибиотиков были очевидны во все моменты времени ( P < 0,05), что указывает на то, что чем выше содержание HV, тем больше антибиотика будет высвобождено. Однако, когда мы увеличили содержание антибиотиков до 2: 1, мы обнаружили, что полимеры высвобождали меньше антибиотиков за 6-недельный период, независимо от содержания в них HV, хотя различия (33–37% против 29%) не были статистически значимыми.
1a).Статистически значимые различия в высвобождении антибиотиков были очевидны во все моменты времени ( P < 0,05), что указывает на то, что чем выше содержание HV, тем больше антибиотика будет высвобождено. Однако, когда мы увеличили содержание антибиотиков до 2: 1, мы обнаружили, что полимеры высвобождали меньше антибиотиков за 6-недельный период, независимо от содержания в них HV, хотя различия (33–37% против 29%) не были статистически значимыми.
Чтобы подтвердить наши выводы, мы сравнили влияние концентрации гентамицина на высвобождение антибиотика в параллельном эксперименте с использованием дисков, покрытых полимером / антибиотиком в соотношении 2: 1 и 5: 1.Кривые высвобождения, представленные на рисунке 2, демонстрируют, что увеличение концентрации антибиотика замедляет высвобождение лекарственного средства независимо от состава PHBV и становится статистически значимым ( P <0,05) по мере увеличения времени инкубации, то есть через 5 дней для PHBV 12%. и 18 дней для PHBV 8%.
Влияние содержания антибиотиков на морфологию и пористость полимеров
Мы использовали сканирующую электронную микроскопию (SEM) и анализатор размера пор для исследования однородности и пористости комплексов полимер / антибиотик.Мы показали, что добавление антибиотика делает текстуру полимера более однородной. Как показано на рисунке 3 (a–, образцы PHBV 12% без антибиотика были наименее однородными (а), тогда как образцы PHBV 12% 2: 1 с более высоким содержанием антибиотиков оказались наиболее однородными (c). наблюдались при сравнении изображений PHBV 8% 2: 1 и PHBV 8% 5: 1 (данные не показаны). Кроме того, анализ изображений SEM показал трещины и поверхностные деформации на поверхностях составов, которые остались после растворенного кристаллы лекарственного средства [стрелки на фиг. 3 (d и e)], количество которых прямо пропорционально содержанию гентамицина в формуле.Однако размер поры после выщелачивания был обратно пропорционален концентрации используемого гентамицина; поры PHBV 8% 5: 1 были значительно больше, чем поры PHBV 8% 2: 1 (0,038 мкм ± 0,0001 против 0,015 мкм ± 0,0001, P <0,05), независимо от содержания HV.
При анализе пористости сравнивали количество пор в составе только 8% PHBV с гентамицином во время смешивания или после 6 недель элюирования. Мы протестировали три образца в каждой группе и обнаружили, что после выщелачивания PHBV 8% 2: 1 имеет больше пор, чем PHBV 8% отдельно или свежеприготовленный PHBV 8% 2: 1 (30% против 10% или 15%, соответственно, P <0.05).
Антибактериальное действие комплексов полимер / гентамицин
Мы сравнили адгезию бактерий к полимерам через различные промежутки времени (3, 24 и 48 ч). Мы обнаружили, что все составы, за исключением PHBV 8% 5: 1, значительно снижали количество прикрепленных S. aureus в первые 3 часа инкубации при 37 ° C по сравнению с контролями без антибиотиков (рис. 4a). В конце 24-часовой инкубации S. aureus было уничтожено, в то время как осталось несколько (<100 КОЕ) живых S.haemolyticus (рис. 4b), которые все погибли через 48 часов. Все комплексы полимер / гентамицин, независимо от содержания HV или гентамицина, были способны значительно (<400 КОЕ) после 24-часовой или 48-часовой экспозиции снизить количество прилипших S. aureus и S. haemolyticus . Однако PHBV 8% 5: 1 был наименее эффективным составом, тогда как PHBV 12% 2: 1 был наиболее эффективным составом в этих условиях.
Исследование гемосовместимости
Мы использовали объединенную кровь нормального человека для определения безопасности комплексов полимер / гентамицин in vitro .Ни один из наших составов не изменил количество или морфологию лейкоцитов, эритроцитов или тромбоцитов, независимо от условий эксперимента (статические / нестатические), содержания HV или концентрации гентамицина.
Обсуждение
Анализ изображений SEM показал, что по мере увеличения содержания антибиотика полимеры становятся более однородными. Это явление было связано с встраиванием кристаллов лекарственного средства в полимер, что также затрудняет проникновение PBS во внутреннюю кристаллическую структуру. 10
10
Увеличение количества кристаллов лекарственного средства в смесях ПОБВ / гентамицин привело к увеличению пористости, что вызвано образованием пустот из-за растворения кристаллов лекарственного средства. Эти пустоты также оставляют кратеры на поверхности полимера. Влияние содержания антибиотика на пористость было больше, чем влияние содержания HV на скорость элюирования антибиотика. Это можно увидеть на рисунке 1 (b), где данные кумулятивного высвобождения для комплексов PHBV с двумя разными концентрациями HV имеют почти одинаковые наклоны из-за одинакового содержания гентамицина.Эти результаты подтверждают, что можно контролировать высвобождение лекарственного средства, контролируя концентрацию кристаллов антибиотика в полимерной матрице.
В экспериментах, посвященных содержанию HV, чем выше содержание HV, тем более кристаллическими и пористыми были полимеры, что приводит к более быстрому высвобождению антибиотиков. Это явление связано с изменением кристалличности ПОБВ при добавлении HV. 10,26,27 Таким образом, увеличение HV с 8% до 12% приводит к более аморфной структуре, что позволяет увеличить водопоглощение.Это ускоряет растворение кристаллов лекарства и приводит к более быстрому высвобождению, как сообщают другие исследователи. 7,10
Во всех экспериментах наблюдалось начальное быстрое высвобождение гентамицина. Этот первоначальный «взрыв» возникает из-за присутствия кристаллов антибиотика на поверхности полимера. Кристаллы лекарства более растворимы, чем полимер, поэтому при их раннем растворении образуются поры или каналы, которые позволяют воде проникать в полимеры. Это ускоряет растворение лекарств внутри полимерной матрицы и, как следствие, приводит к взрывному эффекту.Эффект первоначального взрыва заканчивается, потому что образование каналов заканчивается, когда все лекарства на поверхности, которые находятся в прямом контакте друг с другом, растворяются. После этой точки элюирование больше не является логарифмическим, и наблюдается постоянный характер высвобождения. На этом этапе распад полимера контролирует высвобождение антибиотика, позволяя подвергнуть новые кристаллы лекарства воздействию среды. Фактически, быстрое выбросное высвобождение может быть полезным с терапевтической точки зрения, потому что высокое высвобождение убьет любые бактерии, введенные до или во время операции. 7
На этом этапе распад полимера контролирует высвобождение антибиотика, позволяя подвергнуть новые кристаллы лекарства воздействию среды. Фактически, быстрое выбросное высвобождение может быть полезным с терапевтической точки зрения, потому что высокое высвобождение убьет любые бактерии, введенные до или во время операции. 7
Наряду с увеличением гомогенности по мере увеличения содержания антибиотика мы также наблюдали, что количество пор значительно увеличилось после начала элюирования. Этот эффект вызван растворением кристаллов антибиотика в полимерной матрице и прямо пропорционален концентрации лекарства.
Адгезия S. haemolyticus только к PHBV 8% или PHBV 12% и стальных имплантатов без покрытия была практически идентична ( P > 0.05), что указывает на то, что ни полимеры, ни образцы стали не обладают антимикробными свойствами. 35,36 Однако через 24 часа гентамицин-содержащие полимеры, которые высвободили наибольшее количество гентамицина, показали наибольшее снижение количества прикрепившихся бактерий. Анализы адгезии также показали, что S. haemolyticus оставалось на дисках в течение более длительного периода времени (48 часов), чем S. aureus (24 часа), возможно, из-за его более высокого МИК. В целом, наши комплексы полимер / гентамицин показали сходный или превосходящий бактерицидный эффект по сравнению с другими методами ингибирования биопленки 6,22,30,32,37,38 с хорошей биосовместимостью.
В заключение, PHBV 8% и PHBV 12% демонстрируют замедленное высвобождение гентамицина с постоянной скоростью и выше МИК для S. haemolyticus и S. aureus в течение 6 недель. Содержание HV и загрузка лекарства влияют на кинетику высвобождения. Эти комплексы полимер / гентамицин уничтожают S. aureus и устойчивые к гентамицину S. haemolyticus , прилипшие к поверхности, и не оказывают неблагоприятного воздействия на целостность клеток крови. Таким образом, наша недавно разработанная система гентамицина со встроенным полимером может потенциально снизить инфекционные осложнения при хирургии тазобедренного сустава. In vivo исследования показаны для определения безопасности и эффективности этих комплексов в доклинических условиях.
Таким образом, наша недавно разработанная система гентамицина со встроенным полимером может потенциально снизить инфекционные осложнения при хирургии тазобедренного сустава. In vivo исследования показаны для определения безопасности и эффективности этих комплексов в доклинических условиях.
Рисунок 1.
Влияние содержания HV на совокупное высвобождение (%) гентамицина из полимеров PHBV с 8% или 12% HV и содержанием гентамицина 5: 1 (а) или 2: 1 (б). * Значения показали статистически значимые различия (критерий Стьюдента t , P <0,05).
Рисунок 1.
Влияние содержания HV на кумулятивное высвобождение (%) гентамицина из полимеров PHBV с 8% или 12% HV и содержанием гентамицина 5: 1 (a) или 2: 1 (b). * Значения показали статистически значимые различия (критерий Стьюдента t , P <0,05).
Рисунок 2.
Влияние нагрузки лекарством на совокупный процент высвобожденного гентамицина с содержанием гентамицина 5: 1 и 2: 1 и (а) 12% или (б) 8% HV.* Значения показали статистически значимые различия (критерий Стьюдента t , P <0,05).
Рисунок 2.
Влияние нагрузки лекарством на совокупный процент высвобожденного гентамицина с содержанием гентамицина 5: 1 и 2: 1 и (а) 12% или (б) 8% HV. * Значения показали статистически значимые различия (критерий Стьюдента t , P <0,05).
Рис. 3.
СЭМ-изображения полимеров с различной концентрацией гентамицина во время компаундирования и через 6 недель после выщелачивания.Стрелки указывают кратеры и трещины на поверхностях, оставленные растворенными кристаллами лекарственного средства. Масштабные полосы представляют 100 нм. (а) PHBV12; (б) PHBV12 5: 1; (c) PHBV12 2: 1; (d) PHBV12 2: 1, 6 недель; (e) PHBV12 5: 1, 6 недель.
Рис. 3.
СЭМ-изображения полимеров с различной концентрацией гентамицина во время компаундирования и через 6 недель после выщелачивания. Стрелки указывают кратеры и трещины на поверхностях, оставленные растворенными кристаллами лекарственного средства.Масштабные полосы представляют 100 нм. (а) PHBV12; (б) PHBV12 5: 1; (c) PHBV12 2: 1; (d) PHBV12 2: 1, 6 недель; (e) PHBV12 5: 1, 6 недель.
Стрелки указывают кратеры и трещины на поверхностях, оставленные растворенными кристаллами лекарственного средства.Масштабные полосы представляют 100 нм. (а) PHBV12; (б) PHBV12 5: 1; (c) PHBV12 2: 1; (d) PHBV12 2: 1, 6 недель; (e) PHBV12 5: 1, 6 недель.
Рисунок 4.
Сравнение влияния комплексов ПОБВ / гентамицин на адгезию чувствительных к гентамицину и резистентных штаммов Staphylococcus . Все составы, кроме PHBV 8% 5: 1, значительно снижали количество прилипших чувствительных к гентамицину S. aureus в первые 3 часа инкубации при 37 ° C (a).С другой стороны, устойчивый к гентамицину S. haemolyticus требовал более длительного периода воздействия (24 часа) для достижения значительного снижения (b).
Рисунок 4.
Сравнение влияния комплексов ПОБВ / гентамицин на адгезию чувствительных к гентамицину и устойчивых к гентамицину штаммов Staphylococcus . Все составы, кроме PHBV 8% 5: 1, значительно снижали количество прилипших чувствительных к гентамицину S. aureus в первые 3 часа инкубации при 37 ° C (a).С другой стороны, устойчивый к гентамицину S. haemolyticus требовал более длительного периода воздействия (24 часа) для достижения значительного снижения (b).
Эта работа частично поддержана исследовательским грантом LURF (Исследовательские фонды Лаврентьевского университета). Мы также благодарны компании Materials and Manufacturing Ontario (MMO) за финансовую поддержку.
Список литературы
1.Дикинсон, Г. М. и Бисно, А. Л. (
1993
). Инфекции, связанные с протезами: клинические аспекты.Международный журнал искусственных органов
16
,749
–54.2.Neut, D., van Horn, J. R., van Kooten, T. G. et al. (
2003
). Выявление инфекций, связанных с биоматериалом, в ортопедических суставных имплантатах.Клиническая ортопедия и сопутствующие исследования
261
–8. 3.
3.Гристина А.Г. (
1987
). Инфекция, связанная с биоматериалом: микробная адгезия против тканевой интеграции.Наука
237
,1588
–95.4.Остерманн П. А., Генри С. Л. и Селигсон Д. (
1993
). Роль местной антибактериальной терапии в лечении сложных переломов.Клиническая ортопедия и сопутствующие исследования
102
–11.5.Остерманн, П. А., Генри, С. Л. и Селигсон, Д. (
1994
). Сроки закрытия раны при тяжелых сложных переломах.Ортопедия
17
,397
–9.6.Khardori, N. & Yassien, M. (
1995
).Биопленки при инфекциях, связанных с устройствами.Журнал промышленной микробиологии
15
,141
–7.7.Туресин Ф., Гурсель И. и Хасирчи В. (
2001
). Биоразлагаемые имплантаты из полигидроксиалканоата для лечения остеомиелита: высвобождение антибиотиков in vitro.Journal of Biomaterial Science Polymer Edition
12
,195
–207.8.Сандерсон П. Дж. (
1989
). Предотвращение инфицирования ортопедических имплантатов.Журнал антимикробной химиотерапии
24
,277
–80.9.Sheehan, E., McKenna, J., Mulhall, K. J. et al. (
2004
). Адгезия стафилококка к ортопедическим металлам, исследование in vivo.Журнал ортопедических исследований
22
,39
–43.10.Гурсельт И., Ягмурлу Ф., Коркусуз Ф. et al. (
2002
). Высвобождение антибиотика in vitro из стержней поли (3-гидроксибутират-со-3-гидроксивалерат).Журнал микрокапсулирования
19
,153
–64.11.Коркусуз Ф., Коркусуз П., Эксиоглу Ф. et al. (
2001
). Реакция in vivo на биоразлагаемые системы с контролируемым высвобождением антибиотиков.Журнал исследований биомедицинских материалов
55
,217
–28.12.Канеллакопулу, К. и Джамареллос-Бурбулис, Э. Дж. (
2000
). Системы-носители для местной доставки антибиотиков при костных инфекциях.
Лекарственные препараты
59
,1223
–32,13.Калхун, Дж. Х., Генри, С. Л., Энгер, Д. М. et al. (
1993
). Лечение инфицированных несращений гранулами гентамицин-полиметилметакрилатного антибиотика.Клиническая ортопедия и сопутствующие исследования
23
–7.14.Нельсон, К. Л., Хикмон, С. Г. и Скиннер, Р. А. (
1997
). Лечение экспериментального остеомиелита хирургической обработкой раны и имплантацией биоразлагаемых шариков из полиангидрида-гентамицина.Журнал ортопедических исследований
15
,249
–55.15.Коркусуз Ф., Учида А., Синто Ю. и др. (
1993
). Экспериментальный остеомиелит, связанный с имплантатом, лечится керамическими композитами антибиотик-гидроксиапатит кальция.Журнал костной и суставной хирургии
75
,111
–4.16.Thoma, K. & Schlutermann, B. (
1992
). Взаимосвязь производственных параметров и фармацевтически-технологических требований к биоразлагаемым микрочастицам.2. Приготовление инъекционных микрочастиц в биоразлагаемом полиэфире.Аптека
47
,115
–9,17.Санчес Э., Баро М., Сориано И. и др. (
2001
). Исследование in vivo-in vitro биоразлагаемых и остеоинтегрируемых костных имплантатов с гентамицином.Европейский журнал фармацевтики и биофармацевтики
52
,151
–8.18.Husmann, M., Schenderlein, S., Luck, M. et al. (
2002
).Эрозия полимеров в микрочастицах PLGA, полученных методом фазового разделения.Международный фармацевтический журнал
242
,277
. 19.Феррейра, Б. М. П., Завалья, К. А. К. и Дуэк, Э. А. Р. (
2001
). Пленки смесей поли (L-молочная кислота) / поли (гидроксибутират-гидроксивалерат): разложение in vitro.Исследование материалов
4
,34
–42.20.Рицци, С. К., Хит, Д. Дж., Кумбс, А. Г. et al. (
2001
). Биоразлагаемые композиты полимер / гидроксиапатит: анализ поверхности и начальное прикрепление человеческих остеобластов.
Биоразлагаемые композиты полимер / гидроксиапатит: анализ поверхности и начальное прикрепление человеческих остеобластов.Журнал исследований биомедицинских материалов
55
,475
–86.21.Сандерс, Дж. Э., Бейл, С. Д. и Нойман, Т. (
2002
). Тканевая реакция на микроволокна из различных полимеров: полиэфира, полиэтилена, полимолочной кислоты и полиуретана.Журнал исследований биомедицинских материалов
62
,222
–7.22.Schierholz, J. M., Steinhauser, H., Rump, A. F. et al. (
1997
). Контролируемое высвобождение антибиотиков из биомедицинских полиуретанов: морфологические и структурные особенности.Биоматериалы
18
,839
–44,23.Adams, K., Couch, L., Cierny, G. et al. (
1992
). Оценка in vitro и in vivo диффузии антибиотиков из гранул из полиметилметакрилата, пропитанных антибиотиком.Клиническая ортопедия и сопутствующие исследования
244
–52.24.Бухгольц, Х. В., Элсон, Р. А. и Хайнерт, К. (
1984
). Акриловый цемент, содержащий антибиотики: современные концепции.Клиническая ортопедия и сопутствующие исследования
96
–108.25.Андерсон, А. Дж., Хейвуд, Г. В. и Дауэс, Э. А. (
1990
). Биосинтез и состав бактериальных поли (гидроксиалканоатов).Международный журнал биологических макромолекул
12
,102
–5.26.Ягмурлу, М.Ф., Korkusuz, F., Gursel, I. et al. (
1999
). Система местной доставки антибиотиков сульбактам-цефоперазон полигидроксибутират-ко-гидроксивалерат (PHBV): эффективность и биосовместимость in vivo при лечении экспериментального остеомиелита, связанного с имплантатами.Журнал исследований биомедицинских материалов
46
,494
–503.27.Сендил Д., Гурсель И., Вайз Д. Л. et al. (
1999
). Высвобождение антибиотика из биоразлагаемых микрочастиц PHBV.Журнал контролируемого выпуска
59
,207
–17.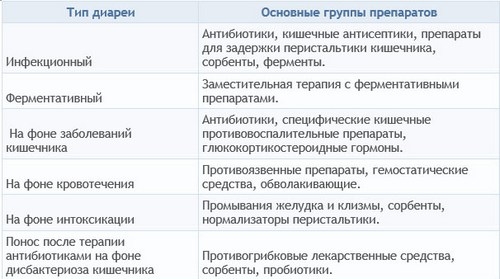 28.
28.Омри А., Сантрес З. Э. и Шек П. Н. (
2002
). Повышенная активность липосомального полимиксина B против Pseudomonas aeruginosa на модели легочной инфекции на крысах.Биохимическая фармакология
64
,1407
–13.29.Национальный комитет по клиническим лабораторным стандартам. (
2001
). Стандарты производительности для испытаний на чувствительность к противомикробным препаратам.М100-С10 . NCCLS, Уэйн, Пенсильвания, США 30.Konig, D. P., Perdreau-Remington, F., Rutt, J. et al. (
1998
). Производство слизи Staphylococcus epidermidis: повышенная адгезия бактерий и их накопление на чистом титане.Acta Orthopaedica Scandinavica
69
,523
–6.31.Шерерц, Р. Дж., Раад, И. И., Белани, А. и др. (
1990
). Трехлетний опыт работы с ультразвуковыми культурами сосудистых катетеров в лаборатории клинической микробиологии.Журнал клинической микробиологии
28
,76
–82.32.Кониг, Д. П., Ширхольц, Дж. М., Хильгерс, Р. Д. et al. (
2001
). Прилипание и накопление Staphylococcus epidermidis RP 62 A и Staphylococcus epidermidis M7 in vitro на четырех различных костных цементах.Архив хирургии Лангенбека
386
,328
–32.33.Сейферт, У. Т., Биль, В. и Шенк, Дж. (
2002
).Тестирование гемосовместимости биоматериалов in vitro в соответствии с ISO 10993-4.Биомолекулярная инженерия
19
,91
–6.34.Biehl, V., Wack, T., Winter, S. et al. (
2002
). Оценка гемосовместимости биоматериалов на основе титана.Биомолекулярная инженерия
19
,97
–101.35.Konig, D. P., Perdreau-Remington, F., Rutt, J. et al. (
1999
).Прилипание и накопление S. epidermidis на различных биоматериалах из-за образования внеклеточной слизи. Сравнение in vitro штамма, продуцирующего слизь (Rp 62 A), и его изогенного слизисто-отрицательного мутанта (M7).
Zentralblatt für Bakteriologie
289
,355
–64,36.Степанович, С., Джукич, Н., Опавски, Н. и др. (
2003
). Значение размера инокулята в формировании биопленок стафилококками.Новая микробиология
26
,129
–32.37.Amorena, B., Gracia, E., Monzon, M. et al. (
1999
). Анализ чувствительности к антибиотикам для золотистого стафилококка в биопленках, разработанных in vitro.Журнал антимикробной химиотерапии
44
,43
–55.38.Олсон, М. Э., Цери, Х., Морк, Д. В. et al. (
2002
). Биопленочные бактерии: образование и сравнительная чувствительность к антибиотикам.Канадский журнал ветеринарных исследований
66
,86
–92.Заметки автора
1 Кафедра химии и биохимии, Лаврентийский университет, 935 Ramsey Lake Road, Садбери, Онтарио, Канада P3E 2C6; 2Отдел биомедицинских исследований, Центр здоровья Техасского университета, 11937 US Highway 271, Tyler, TX 75708, USA
JAC vol.54 №6 © Британское общество антимикробной химиотерапии, 2004; все права защищены
Противомикробная эффективность новой системы с контролируемым высвобождением поли (гидроксимасляной и гидроксивалериановой кислоты), содержащей антибиотики | Журнал антимикробной химиотерапии
Абстрактные
Цель : Отказ ортопедических устройств, в основном замены бедренной кости, из-за инфекции приобретает все большее медицинское значение.Существует потребность в улучшенных системах доставки антибиотиков при лечении ортопедических инфекций, и здесь мы оценили составы полигидроксиалканоатов на предмет их пригодности в качестве системы постоянной доставки гентамицина.
Методы : Гентамицин был включен в сополимер поли (гидроксимасляный-гидроксивалерат) (ПОБВ) с содержанием гидроксивалерата (HV) 8% или 12% при соотношении 2: 1 или 5: 1 (вес к весу). В сочетании с исследованием элюирования были проведены сканирующая электронная микроскопия и исследование пористости для изучения физических характеристик комплексов до и после эффекта выщелачивания.Антибактериальную эффективность комплексов анализировали с помощью анализа бактериальной адгезии с использованием клинических изолятов Staphylococcus haemolyticus и Staphylococcus aureus . Кроме того, полимеры подвергались воздействию объединенной крови человека для проверки их биосовместимости как в статической, так и в динамической среде.
В сочетании с исследованием элюирования были проведены сканирующая электронная микроскопия и исследование пористости для изучения физических характеристик комплексов до и после эффекта выщелачивания.Антибактериальную эффективность комплексов анализировали с помощью анализа бактериальной адгезии с использованием клинических изолятов Staphylococcus haemolyticus и Staphylococcus aureus . Кроме того, полимеры подвергались воздействию объединенной крови человека для проверки их биосовместимости как в статической, так и в динамической среде.
Результаты : Мы показали, что увеличение содержания HV с 8% до 12% приводит к более быстрому высвобождению интегрированного антибиотика. Увеличение содержания антибиотика повышает гомогенность, снижая проницаемость комплексов и снижая скорость высвобождения.Значительное снижение количества прикрепленных S. aureus и устойчивых к гентамицину S. haemolyticus в течение 48 часов воздействия наших препаратов подтвердило эффективность комплексов PHBV / гентамицин. Наконец, эти составы не изменяли гемодинамику объединенных образцов крови после продолжительного периода времени.
Заключение : Взятые вместе, составы PHBV / гентамицин могут оказаться эффективными профилактическими терапевтическими средствами при инфекциях, связанных с имплантатами Staphylococcus .
Введение
Замена суставов, поврежденных в результате травмы или артрита, стала обычной процедурой, и только в США ежегодно проводится около 400 000 замен суставов. 1,2 Пациенты, получающие ортопедические протезы, подвержены риску септического артрита, глубоких бактериальных инфекций с вовлечением имплантатов и бактериемии. 3–5 Отказ ортопедических устройств, в основном замены бедренной кости, из-за инфекции приобретает все большее медицинское значение, и после того, как инфекция установлена, пациент должен выдержать длительный режим антимикробной терапии.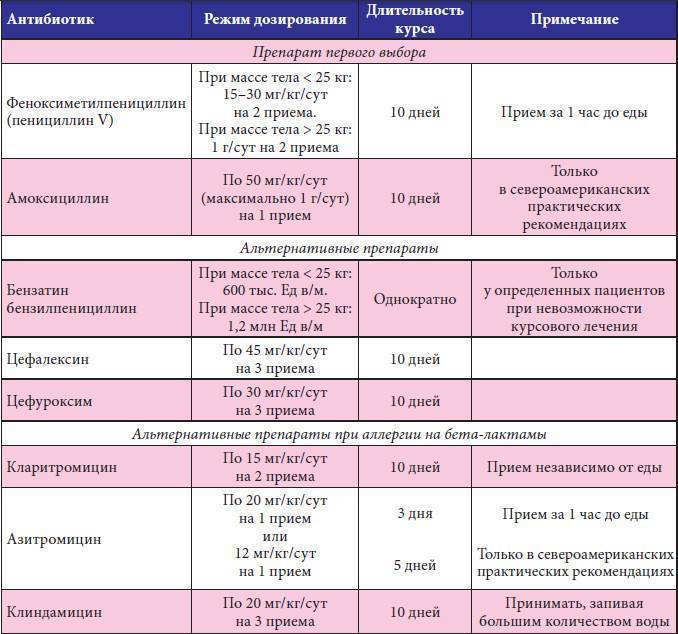 Кроме того, повторяющиеся неудачи этих методов лечения часто приводят к удалению ортопедических имплантатов и могут потребовать повторной операции. 6–9
Кроме того, повторяющиеся неудачи этих методов лечения часто приводят к удалению ортопедических имплантатов и могут потребовать повторной операции. 6–9
Появляется все больше доказательств того, что микробная адгезия и последующая колонизация, ведущая к развитию биопленок, вовлечены в этиологию инфекций, связанных с устройствами. 7,10 Следовательно, эффективное лечение может быть возможным за счет уничтожения бактерий на ранних стадиях колонизации, и непрерывная доставка антибиотиков представляется многообещающим подходом. 11 Хирургическое введение сфер из полиметилметакрилата (ПММА) в очаг инфекции, которые затем выделяют антибиотик в течение примерно 6 недель, 6,10,12,13 было методом выбора в течение последнего десятилетия. Хотя эта система эффективно функционирует с точки зрения доставки антибиотиков и искоренения инфекции, из-за их небиоразлагаемой природы, сферы должны быть удалены, как только васкуляризация области вернется к норме, процесса, которого можно избежать, если доставка биоразлагаемого лекарства система была использована.
Биоразлагаемые синтетические материалы, такие как насыщенные антибиотиками костные трансплантаты, 14 гидроксиапатит-коллагеновые стержни, гидроксиапатит-кальций-фосфатные композиты, 15 кальций-фосфатные костные цементы, 16 полимолочные кислоты и их сополимеры с гликолевыми кислотами, полиангидридами, 12,14,17–19 и полиуретан 20–22 . Эти биоматериалы также использовались в качестве покрывающих веществ на ножках бедренной кости. Преимущество этих синтетических имплантатов в том, что все они полностью метаболизируются в организме человека.Однако они обладают такими недостатками, как снижение pH в месте установки имплантата, что приводит к локализованному воспалению, повреждению тканей и, в конечном итоге, к отказу бедренных имплантатов. 23,24 Полигидроксиалканоаты (ПГА) оказались многообещающими при использовании для покрытия имплантатов, используемых в твердых тканях, благодаря ряду уникальных свойств, таких как пьезоэлектричество, термопластичность, биоразлагаемость и биосовместимость; и при смешивании с антибиотиками они предотвращают бактериальную адгезию. 7,11,25
Полигидроксиалканоаты — это природные полимеры, полученные из бактерий.Поли (3-гидроксимасляная кислота-3-гидроксивалериановая кислота) (ПОБВ) состоит из поли (3-гидроксибутирата) (ПОБ) и различного количества молекул гидроксивалерата (HV). Полимеры PHBV являются биоразлагаемыми и биосовместимыми и фактически способствуют росту костей. 10,11,26,27 В этом исследовании мы оценили физико-химические свойства и характер высвобождения лекарственного средства комплекса PHBV / гентамицин и его влияние на характер роста образующих биопленки Staphylococcus разновидностей in vitro .
Материалы и методы
Изготовление дисков
Диски из бедра (Total Hip System — имплантат с покрытием для использования без цемента: имплантат DePuy Femoral, Варшава, США) были созданы путем разрезания протеза бедра на круглые диски диаметром 9,2 мм и толщиной 2,7 мм.
Приготовление комплекса полимер / антибиотик и покрытие дисков
ПОГБВ с 8% или 12% гидроксивалериановой кислотой было закуплено у Across Organics (Нью-Джерси, США).Один грамм PHBV растворяли в хлороформе и добавляли соответствующее количество гентамицина (Across Organics) для получения содержания антибиотика 2: 1 или 5: 1 (мас. / Мас.). Смесь инкубировали при 55 ° C на водяной бане со встряхиванием и встряхивали до полной гомогенности. Затем смесь полимер / гентамицин выливали в металлическую форму (диаметр 11,5 мм, толщина 5 мм), содержащую ортопедические диски. Диски покрывали и сушили в течение 24 часов. После высыхания диски измеряли электронным штангенциркулем (STM Digimatic Calliper; Дайна, Садбери, Онтарио, Канада) и взвешивали для определения количества покрытия.
Поведение при высвобождении наркотиков
Мы измерили скорость высвобождения гентамицина из комплексов антибиотик / полимер на дисках. Высвобождение гентамицина изучали в 5 мл фосфатно-солевого буфера (PBS, pH 7,4) при 37 ° C в условиях мягкого встряхивания (100 об / мин). Аликвоты по 50 мкл анализировали на гентамицин в моменты времени 0, 0,25, 0,5, 1, 3, 6, 12 и 24 часа, который повторяли через равные промежутки времени в течение 6 недель. Свежий PBS (50 мкл) был добавлен для замены изъятого количества.Концентрацию гентамицина измеряли микробиологическим анализом с использованием Staphylococcus aureus (ATCC 25923; American Type Culture Collection, Manassas, VA, USA), как мы описали ранее. 28 Подобный комплекс полимер / диск без антибиотика служил в качестве контроля, чтобы гарантировать, что весь материал, который элюируется с диска, не влияет на зону ингибирования.
Определение чувствительности к антибиотикам
Использование всего клинического материала в этом проекте было одобрено институциональным наблюдательным советом (IRB) региональной больницы Садбери.Штаммы Staphylococcus haemolyticus и S. aureus , использованные в этом исследовании, представляют собой клинические изоляты инфекций ортопедических имплантатов бедренной кости в региональной больнице Садбери, Садбери, Онтарио, Канада. Бактериальные штаммы тестировали на чувствительность к гентамицину методом разбавления бульона. 29 Минимальная ингибирующая концентрация (МИК) была определена как самая низкая концентрация гентамицина, которая подавляла видимый рост тестируемых бактерий. Все МПК были подтверждены с помощью Microscan (система WalkAway-40SI с LabPro; Dade Behring Inc., Торонто, Онтарио, Канада) в соответствии с инструкциями поставщика. 29
Бактериальная адгезия
Полимерные диски с антибиотиками и металлические диски без покрытия погружали в бактериальные суспензии в PBS (10 8 КОЕ / мл) и инкубировали в течение 5 ч при 37 ° C в статических условиях. 30,31 Образцы переносили в 10 мл бульона Мюллера – Хинтона и инкубировали 3, 24 и 48 ч при 37 ° C. После каждого периода инкубации образцы промывали три раза для удаления неприлипающих бактерий.Затем прикрепленные бактерии удаляли с полимерных поверхностей с помощью ультразвуковой обработки (150 Вт, интервалы 90 с, всего 4,5 мин; ультразвуковой прибор Fisher, Торонто, Канада) и определяли количество колоний жизнеспособных клеток. 31,32
Тест на гемосовместимость
Образцы крови были взяты у 10 здоровых людей, объединены и использованы в течение 2 часов. Дублированные образцы (8 мл) дисков с покрытием или только металлический диск (отрицательный контроль) помещали в 2,5 мл объединенной крови человека.Образцы выдерживали при 37 ° C в течение 2 ч. Одна группа образцов находилась в статическом состоянии, а другая — в динамическом. Мы отбирали образцы каждые 30 минут для анализа крови (CBC) (гематологический аппарат ADVIA 120; Bayer Inc., Торонто, Онтарио, Канада) для анализа биосовместимости полимера с кровью человека в соответствии с рекомендациями ISO. 33,34
Сканирующая электронная микроскопия
Эксперименты по оценке физических характеристик наших комплексов полимер / антибиотик были проведены лабораторией Quantachrome Instruments Laboratory Services (Бойнтон-Бич, Флорида, США).Поверхности полимеров анализировали с помощью автоэмиссионного сканирующего электронного микроскопа (SEM; S-4700, Hitachi Co., Токио, Япония) на образцах, напыленных углеродом. 20 Анализ пористости полимеров проводили на автоматическом анализаторе размера пор (PoreMaster 60; Quantachrome Instruments, Boynton Beach, FL, USA). Прибор измеряет давление, которое прикладывается, чтобы заставить нереактивную несмачивающую жидкость проникнуть в поры. Связь между приложенным давлением и размером поры, в которую будет проникать ртуть, определяется уравнением Уошберна:\ [PD = {-} 4y {\ times} cos {\,} {\ theta} \]
, где P — приложенное давление, D — диаметр, y — поверхностное натяжение ртути (480 дин см -1 ) и θ — угол контакта между ртутью и стенкой поры, обычно около 140 °. .По мере увеличения давления прибор определяет объем проникновения ртути по изменению емкости между столбиком ртути и металлической оболочкой, окружающей шток ячейки для образца. По мере того как столбик ртути укорачивается, данные о давлении и объеме непрерывно собираются и отображаются на специальном компьютере.Анализ данных
Мы использовали тест Стьюдента t (для двух выборок) или ANOVA (для множественных сравнений) с двусторонним анализом после теста Даннета для сравнения средних значений.Значение P ≤0,05 считалось значимым. Результаты представлены в виде средних значений ± среднеквадратичное отклонение. минимум трех независимых экспериментов.
Результаты
Профиль высвобождения гентамицина PHBV 8% и PHBV 12%
Мы сравнили влияние содержания HV (рис. 1) и концентрации гентамицина (рис. 2) на кинетику высвобождения антибиотиков в наших препаратах. После 6 недель инкубации в PBS, PHBV 8% и PHBV 12% с соотношением полимер / гентамицин 5: 1 высвободили 33% и 37% содержащихся в них антибиотиков, соответственно (рис. 1a).Статистически значимые различия в высвобождении антибиотиков были очевидны во все моменты времени ( P < 0,05), что указывает на то, что чем выше содержание HV, тем больше антибиотика будет высвобождено. Однако, когда мы увеличили содержание антибиотиков до 2: 1, мы обнаружили, что полимеры высвобождали меньше антибиотиков за 6-недельный период, независимо от содержания в них HV, хотя различия (33–37% против 29%) не были статистически значимыми.
Чтобы подтвердить наши выводы, мы сравнили влияние концентрации гентамицина на высвобождение антибиотика в параллельном эксперименте с использованием дисков, покрытых полимером / антибиотиком в соотношении 2: 1 и 5: 1.Кривые высвобождения, представленные на рисунке 2, демонстрируют, что увеличение концентрации антибиотика замедляет высвобождение лекарственного средства независимо от состава PHBV и становится статистически значимым ( P <0,05) по мере увеличения времени инкубации, то есть через 5 дней для PHBV 12%. и 18 дней для PHBV 8%.
Влияние содержания антибиотиков на морфологию и пористость полимеров
Мы использовали сканирующую электронную микроскопию (SEM) и анализатор размера пор для исследования однородности и пористости комплексов полимер / антибиотик.Мы показали, что добавление антибиотика делает текстуру полимера более однородной. Как показано на рисунке 3 (a–, образцы PHBV 12% без антибиотика были наименее однородными (а), тогда как образцы PHBV 12% 2: 1 с более высоким содержанием антибиотиков оказались наиболее однородными (c). наблюдались при сравнении изображений PHBV 8% 2: 1 и PHBV 8% 5: 1 (данные не показаны). Кроме того, анализ изображений SEM показал трещины и поверхностные деформации на поверхностях составов, которые остались после растворенного кристаллы лекарственного средства [стрелки на фиг. 3 (d и e)], количество которых прямо пропорционально содержанию гентамицина в формуле.Однако размер поры после выщелачивания был обратно пропорционален концентрации используемого гентамицина; поры PHBV 8% 5: 1 были значительно больше, чем поры PHBV 8% 2: 1 (0,038 мкм ± 0,0001 против 0,015 мкм ± 0,0001, P <0,05), независимо от содержания HV.
При анализе пористости сравнивали количество пор в составе только 8% PHBV с гентамицином во время смешивания или после 6 недель элюирования. Мы протестировали три образца в каждой группе и обнаружили, что после выщелачивания PHBV 8% 2: 1 имеет больше пор, чем PHBV 8% отдельно или свежеприготовленный PHBV 8% 2: 1 (30% против 10% или 15%, соответственно, P <0.05).
Антибактериальное действие комплексов полимер / гентамицин
Мы сравнили адгезию бактерий к полимерам через различные промежутки времени (3, 24 и 48 ч). Мы обнаружили, что все составы, за исключением PHBV 8% 5: 1, значительно снижали количество прикрепленных S. aureus в первые 3 часа инкубации при 37 ° C по сравнению с контролями без антибиотиков (рис. 4a). В конце 24-часовой инкубации S. aureus было уничтожено, в то время как осталось несколько (<100 КОЕ) живых S.haemolyticus (рис. 4b), которые все погибли через 48 часов. Все комплексы полимер / гентамицин, независимо от содержания HV или гентамицина, были способны значительно (<400 КОЕ) после 24-часовой или 48-часовой экспозиции снизить количество прилипших S. aureus и S. haemolyticus . Однако PHBV 8% 5: 1 был наименее эффективным составом, тогда как PHBV 12% 2: 1 был наиболее эффективным составом в этих условиях.
Исследование гемосовместимости
Мы использовали объединенную кровь нормального человека для определения безопасности комплексов полимер / гентамицин in vitro .Ни один из наших составов не изменил количество или морфологию лейкоцитов, эритроцитов или тромбоцитов, независимо от условий эксперимента (статические / нестатические), содержания HV или концентрации гентамицина.
Обсуждение
Анализ изображений SEM показал, что по мере увеличения содержания антибиотика полимеры становятся более однородными. Это явление было связано с встраиванием кристаллов лекарственного средства в полимер, что также затрудняет проникновение PBS во внутреннюю кристаллическую структуру. 10
Увеличение количества кристаллов лекарственного средства в смесях ПОБВ / гентамицин привело к увеличению пористости, что вызвано образованием пустот из-за растворения кристаллов лекарственного средства. Эти пустоты также оставляют кратеры на поверхности полимера. Влияние содержания антибиотика на пористость было больше, чем влияние содержания HV на скорость элюирования антибиотика. Это можно увидеть на рисунке 1 (b), где данные кумулятивного высвобождения для комплексов PHBV с двумя разными концентрациями HV имеют почти одинаковые наклоны из-за одинакового содержания гентамицина.Эти результаты подтверждают, что можно контролировать высвобождение лекарственного средства, контролируя концентрацию кристаллов антибиотика в полимерной матрице.
В экспериментах, посвященных содержанию HV, чем выше содержание HV, тем более кристаллическими и пористыми были полимеры, что приводит к более быстрому высвобождению антибиотиков. Это явление связано с изменением кристалличности ПОБВ при добавлении HV. 10,26,27 Таким образом, увеличение HV с 8% до 12% приводит к более аморфной структуре, что позволяет увеличить водопоглощение.Это ускоряет растворение кристаллов лекарства и приводит к более быстрому высвобождению, как сообщают другие исследователи. 7,10
Во всех экспериментах наблюдалось начальное быстрое высвобождение гентамицина. Этот первоначальный «взрыв» возникает из-за присутствия кристаллов антибиотика на поверхности полимера. Кристаллы лекарства более растворимы, чем полимер, поэтому при их раннем растворении образуются поры или каналы, которые позволяют воде проникать в полимеры. Это ускоряет растворение лекарств внутри полимерной матрицы и, как следствие, приводит к взрывному эффекту.Эффект первоначального взрыва заканчивается, потому что образование каналов заканчивается, когда все лекарства на поверхности, которые находятся в прямом контакте друг с другом, растворяются. После этой точки элюирование больше не является логарифмическим, и наблюдается постоянный характер высвобождения. На этом этапе распад полимера контролирует высвобождение антибиотика, позволяя подвергнуть новые кристаллы лекарства воздействию среды. Фактически, быстрое выбросное высвобождение может быть полезным с терапевтической точки зрения, потому что высокое высвобождение убьет любые бактерии, введенные до или во время операции. 7
Наряду с увеличением гомогенности по мере увеличения содержания антибиотика мы также наблюдали, что количество пор значительно увеличилось после начала элюирования. Этот эффект вызван растворением кристаллов антибиотика в полимерной матрице и прямо пропорционален концентрации лекарства.
Адгезия S. haemolyticus только к PHBV 8% или PHBV 12% и стальных имплантатов без покрытия была практически идентична ( P > 0.05), что указывает на то, что ни полимеры, ни образцы стали не обладают антимикробными свойствами. 35,36 Однако через 24 часа гентамицин-содержащие полимеры, которые высвободили наибольшее количество гентамицина, показали наибольшее снижение количества прикрепившихся бактерий. Анализы адгезии также показали, что S. haemolyticus оставалось на дисках в течение более длительного периода времени (48 часов), чем S. aureus (24 часа), возможно, из-за его более высокого МИК. В целом, наши комплексы полимер / гентамицин показали сходный или превосходящий бактерицидный эффект по сравнению с другими методами ингибирования биопленки 6,22,30,32,37,38 с хорошей биосовместимостью.
В заключение, PHBV 8% и PHBV 12% демонстрируют замедленное высвобождение гентамицина с постоянной скоростью и выше МИК для S. haemolyticus и S. aureus в течение 6 недель. Содержание HV и загрузка лекарства влияют на кинетику высвобождения. Эти комплексы полимер / гентамицин уничтожают S. aureus и устойчивые к гентамицину S. haemolyticus , прилипшие к поверхности, и не оказывают неблагоприятного воздействия на целостность клеток крови. Таким образом, наша недавно разработанная система гентамицина со встроенным полимером может потенциально снизить инфекционные осложнения при хирургии тазобедренного сустава. In vivo исследования показаны для определения безопасности и эффективности этих комплексов в доклинических условиях.
Рисунок 1.
Влияние содержания HV на совокупное высвобождение (%) гентамицина из полимеров PHBV с 8% или 12% HV и содержанием гентамицина 5: 1 (а) или 2: 1 (б). * Значения показали статистически значимые различия (критерий Стьюдента t , P <0,05).
Рисунок 1.
Влияние содержания HV на кумулятивное высвобождение (%) гентамицина из полимеров PHBV с 8% или 12% HV и содержанием гентамицина 5: 1 (a) или 2: 1 (b). * Значения показали статистически значимые различия (критерий Стьюдента t , P <0,05).
Рисунок 2.
Влияние нагрузки лекарством на совокупный процент высвобожденного гентамицина с содержанием гентамицина 5: 1 и 2: 1 и (а) 12% или (б) 8% HV.* Значения показали статистически значимые различия (критерий Стьюдента t , P <0,05).
Рисунок 2.
Влияние нагрузки лекарством на совокупный процент высвобожденного гентамицина с содержанием гентамицина 5: 1 и 2: 1 и (а) 12% или (б) 8% HV. * Значения показали статистически значимые различия (критерий Стьюдента t , P <0,05).
Рис. 3.
СЭМ-изображения полимеров с различной концентрацией гентамицина во время компаундирования и через 6 недель после выщелачивания.Стрелки указывают кратеры и трещины на поверхностях, оставленные растворенными кристаллами лекарственного средства. Масштабные полосы представляют 100 нм. (а) PHBV12; (б) PHBV12 5: 1; (c) PHBV12 2: 1; (d) PHBV12 2: 1, 6 недель; (e) PHBV12 5: 1, 6 недель.
Рис. 3.
СЭМ-изображения полимеров с различной концентрацией гентамицина во время компаундирования и через 6 недель после выщелачивания. Стрелки указывают кратеры и трещины на поверхностях, оставленные растворенными кристаллами лекарственного средства.Масштабные полосы представляют 100 нм. (а) PHBV12; (б) PHBV12 5: 1; (c) PHBV12 2: 1; (d) PHBV12 2: 1, 6 недель; (e) PHBV12 5: 1, 6 недель.
Рисунок 4.
Сравнение влияния комплексов ПОБВ / гентамицин на адгезию чувствительных к гентамицину и резистентных штаммов Staphylococcus . Все составы, кроме PHBV 8% 5: 1, значительно снижали количество прилипших чувствительных к гентамицину S. aureus в первые 3 часа инкубации при 37 ° C (a).С другой стороны, устойчивый к гентамицину S. haemolyticus требовал более длительного периода воздействия (24 часа) для достижения значительного снижения (b).
Рисунок 4.
Сравнение влияния комплексов ПОБВ / гентамицин на адгезию чувствительных к гентамицину и устойчивых к гентамицину штаммов Staphylococcus . Все составы, кроме PHBV 8% 5: 1, значительно снижали количество прилипших чувствительных к гентамицину S. aureus в первые 3 часа инкубации при 37 ° C (a).С другой стороны, устойчивый к гентамицину S. haemolyticus требовал более длительного периода воздействия (24 часа) для достижения значительного снижения (b).
Эта работа частично поддержана исследовательским грантом LURF (Исследовательские фонды Лаврентьевского университета). Мы также благодарны компании Materials and Manufacturing Ontario (MMO) за финансовую поддержку.
Список литературы
1.Дикинсон, Г. М. и Бисно, А. Л. (
1993
). Инфекции, связанные с протезами: клинические аспекты.Международный журнал искусственных органов
16
,749
–54.2.Neut, D., van Horn, J. R., van Kooten, T. G. et al. (
2003
). Выявление инфекций, связанных с биоматериалом, в ортопедических суставных имплантатах.Клиническая ортопедия и сопутствующие исследования
261
–8.3.Гристина А.Г. (
1987
). Инфекция, связанная с биоматериалом: микробная адгезия против тканевой интеграции.Наука
237
,1588
–95.4.Остерманн П. А., Генри С. Л. и Селигсон Д. (
1993
). Роль местной антибактериальной терапии в лечении сложных переломов.Клиническая ортопедия и сопутствующие исследования
102
–11.5.Остерманн, П. А., Генри, С. Л. и Селигсон, Д. (
1994
). Сроки закрытия раны при тяжелых сложных переломах.Ортопедия
17
,397
–9.6.Khardori, N. & Yassien, M. (
1995
).Биопленки при инфекциях, связанных с устройствами.Журнал промышленной микробиологии
15
,141
–7.7.Туресин Ф., Гурсель И. и Хасирчи В. (
2001
). Биоразлагаемые имплантаты из полигидроксиалканоата для лечения остеомиелита: высвобождение антибиотиков in vitro.Journal of Biomaterial Science Polymer Edition
12
,195
–207.8.Сандерсон П. Дж. (
1989
). Предотвращение инфицирования ортопедических имплантатов.Журнал антимикробной химиотерапии
24
,277
–80.9.Sheehan, E., McKenna, J., Mulhall, K. J. et al. (
2004
). Адгезия стафилококка к ортопедическим металлам, исследование in vivo.Журнал ортопедических исследований
22
,39
–43.10.Гурсельт И., Ягмурлу Ф., Коркусуз Ф. et al. (
2002
). Высвобождение антибиотика in vitro из стержней поли (3-гидроксибутират-со-3-гидроксивалерат).Журнал микрокапсулирования
19
,153
–64.11.Коркусуз Ф., Коркусуз П., Эксиоглу Ф. et al. (
2001
). Реакция in vivo на биоразлагаемые системы с контролируемым высвобождением антибиотиков.Журнал исследований биомедицинских материалов
55
,217
–28.12.Канеллакопулу, К. и Джамареллос-Бурбулис, Э. Дж. (
2000
). Системы-носители для местной доставки антибиотиков при костных инфекциях.Лекарственные препараты
59
,1223
–32,13.Калхун, Дж. Х., Генри, С. Л., Энгер, Д. М. et al. (
1993
). Лечение инфицированных несращений гранулами гентамицин-полиметилметакрилатного антибиотика.Клиническая ортопедия и сопутствующие исследования
23
–7.14.Нельсон, К. Л., Хикмон, С. Г. и Скиннер, Р. А. (
1997
). Лечение экспериментального остеомиелита хирургической обработкой раны и имплантацией биоразлагаемых шариков из полиангидрида-гентамицина.Журнал ортопедических исследований
15
,249
–55.15.Коркусуз Ф., Учида А., Синто Ю. и др. (
1993
). Экспериментальный остеомиелит, связанный с имплантатом, лечится керамическими композитами антибиотик-гидроксиапатит кальция.Журнал костной и суставной хирургии
75
,111
–4.16.Thoma, K. & Schlutermann, B. (
1992
). Взаимосвязь производственных параметров и фармацевтически-технологических требований к биоразлагаемым микрочастицам.2. Приготовление инъекционных микрочастиц в биоразлагаемом полиэфире.Аптека
47
,115
–9,17.Санчес Э., Баро М., Сориано И. и др. (
2001
). Исследование in vivo-in vitro биоразлагаемых и остеоинтегрируемых костных имплантатов с гентамицином.Европейский журнал фармацевтики и биофармацевтики
52
,151
–8.18.Husmann, M., Schenderlein, S., Luck, M. et al. (
2002
).Эрозия полимеров в микрочастицах PLGA, полученных методом фазового разделения.Международный фармацевтический журнал
242
,277
. 19.Феррейра, Б. М. П., Завалья, К. А. К. и Дуэк, Э. А. Р. (
2001
). Пленки смесей поли (L-молочная кислота) / поли (гидроксибутират-гидроксивалерат): разложение in vitro.Исследование материалов
4
,34
–42.20.Рицци, С. К., Хит, Д. Дж., Кумбс, А. Г. et al. (
2001
). Биоразлагаемые композиты полимер / гидроксиапатит: анализ поверхности и начальное прикрепление человеческих остеобластов.Журнал исследований биомедицинских материалов
55
,475
–86.21.Сандерс, Дж. Э., Бейл, С. Д. и Нойман, Т. (
2002
). Тканевая реакция на микроволокна из различных полимеров: полиэфира, полиэтилена, полимолочной кислоты и полиуретана.Журнал исследований биомедицинских материалов
62
,222
–7.22.Schierholz, J. M., Steinhauser, H., Rump, A. F. et al. (
1997
). Контролируемое высвобождение антибиотиков из биомедицинских полиуретанов: морфологические и структурные особенности.Биоматериалы
18
,839
–44,23.Adams, K., Couch, L., Cierny, G. et al. (
1992
). Оценка in vitro и in vivo диффузии антибиотиков из гранул из полиметилметакрилата, пропитанных антибиотиком.Клиническая ортопедия и сопутствующие исследования
244
–52.24.Бухгольц, Х. В., Элсон, Р. А. и Хайнерт, К. (
1984
). Акриловый цемент, содержащий антибиотики: современные концепции.Клиническая ортопедия и сопутствующие исследования
96
–108.25.Андерсон, А. Дж., Хейвуд, Г. В. и Дауэс, Э. А. (
1990
). Биосинтез и состав бактериальных поли (гидроксиалканоатов).Международный журнал биологических макромолекул
12
,102
–5.26.Ягмурлу, М.Ф., Korkusuz, F., Gursel, I. et al. (
1999
). Система местной доставки антибиотиков сульбактам-цефоперазон полигидроксибутират-ко-гидроксивалерат (PHBV): эффективность и биосовместимость in vivo при лечении экспериментального остеомиелита, связанного с имплантатами.Журнал исследований биомедицинских материалов
46
,494
–503.27.Сендил Д., Гурсель И., Вайз Д. Л. et al. (
1999
). Высвобождение антибиотика из биоразлагаемых микрочастиц PHBV.Журнал контролируемого выпуска
59
,207
–17.28.Омри А., Сантрес З. Э. и Шек П. Н. (
2002
). Повышенная активность липосомального полимиксина B против Pseudomonas aeruginosa на модели легочной инфекции на крысах.Биохимическая фармакология
64
,1407
–13.29.Национальный комитет по клиническим лабораторным стандартам. (
2001
). Стандарты производительности для испытаний на чувствительность к противомикробным препаратам.М100-С10 . NCCLS, Уэйн, Пенсильвания, США 30.Konig, D. P., Perdreau-Remington, F., Rutt, J. et al. (
1998
). Производство слизи Staphylococcus epidermidis: повышенная адгезия бактерий и их накопление на чистом титане.Acta Orthopaedica Scandinavica
69
,523
–6.31.Шерерц, Р. Дж., Раад, И. И., Белани, А. и др. (
1990
). Трехлетний опыт работы с ультразвуковыми культурами сосудистых катетеров в лаборатории клинической микробиологии.Журнал клинической микробиологии
28
,76
–82.32.Кониг, Д. П., Ширхольц, Дж. М., Хильгерс, Р. Д. et al. (
2001
). Прилипание и накопление Staphylococcus epidermidis RP 62 A и Staphylococcus epidermidis M7 in vitro на четырех различных костных цементах.Архив хирургии Лангенбека
386
,328
–32.33.Сейферт, У. Т., Биль, В. и Шенк, Дж. (
2002
).Тестирование гемосовместимости биоматериалов in vitro в соответствии с ISO 10993-4.Биомолекулярная инженерия
19
,91
–6.34.Biehl, V., Wack, T., Winter, S. et al. (
2002
). Оценка гемосовместимости биоматериалов на основе титана.Биомолекулярная инженерия
19
,97
–101.35.Konig, D. P., Perdreau-Remington, F., Rutt, J. et al. (
1999
).Прилипание и накопление S. epidermidis на различных биоматериалах из-за образования внеклеточной слизи. Сравнение in vitro штамма, продуцирующего слизь (Rp 62 A), и его изогенного слизисто-отрицательного мутанта (M7).Zentralblatt für Bakteriologie
289
,355
–64,36.Степанович, С., Джукич, Н., Опавски, Н. и др. (
2003
). Значение размера инокулята в формировании биопленок стафилококками.Новая микробиология
26
,129
–32.37.Amorena, B., Gracia, E., Monzon, M. et al. (
1999
). Анализ чувствительности к антибиотикам для золотистого стафилококка в биопленках, разработанных in vitro.Журнал антимикробной химиотерапии
44
,43
–55.38.Олсон, М. Э., Цери, Х., Морк, Д. В. et al. (
2002
). Биопленочные бактерии: образование и сравнительная чувствительность к антибиотикам.Канадский журнал ветеринарных исследований
66
,86
–92.Заметки автора
1 Кафедра химии и биохимии, Лаврентийский университет, 935 Ramsey Lake Road, Садбери, Онтарио, Канада P3E 2C6; 2Отдел биомедицинских исследований, Центр здоровья Техасского университета, 11937 US Highway 271, Tyler, TX 75708, USA
JAC vol.54 №6 © Британское общество антимикробной химиотерапии, 2004; все права защищены
Противомикробная эффективность новой системы с контролируемым высвобождением поли (гидроксимасляной и гидроксивалериановой кислоты), содержащей антибиотики | Журнал антимикробной химиотерапии
Абстрактные
Цель : Отказ ортопедических устройств, в основном замены бедренной кости, из-за инфекции приобретает все большее медицинское значение.Существует потребность в улучшенных системах доставки антибиотиков при лечении ортопедических инфекций, и здесь мы оценили составы полигидроксиалканоатов на предмет их пригодности в качестве системы постоянной доставки гентамицина.
Методы : Гентамицин был включен в сополимер поли (гидроксимасляный-гидроксивалерат) (ПОБВ) с содержанием гидроксивалерата (HV) 8% или 12% при соотношении 2: 1 или 5: 1 (вес к весу). В сочетании с исследованием элюирования были проведены сканирующая электронная микроскопия и исследование пористости для изучения физических характеристик комплексов до и после эффекта выщелачивания.Антибактериальную эффективность комплексов анализировали с помощью анализа бактериальной адгезии с использованием клинических изолятов Staphylococcus haemolyticus и Staphylococcus aureus . Кроме того, полимеры подвергались воздействию объединенной крови человека для проверки их биосовместимости как в статической, так и в динамической среде.
Результаты : Мы показали, что увеличение содержания HV с 8% до 12% приводит к более быстрому высвобождению интегрированного антибиотика. Увеличение содержания антибиотика повышает гомогенность, снижая проницаемость комплексов и снижая скорость высвобождения.Значительное снижение количества прикрепленных S. aureus и устойчивых к гентамицину S. haemolyticus в течение 48 часов воздействия наших препаратов подтвердило эффективность комплексов PHBV / гентамицин. Наконец, эти составы не изменяли гемодинамику объединенных образцов крови после продолжительного периода времени.
Заключение : Взятые вместе, составы PHBV / гентамицин могут оказаться эффективными профилактическими терапевтическими средствами при инфекциях, связанных с имплантатами Staphylococcus .
Введение
Замена суставов, поврежденных в результате травмы или артрита, стала обычной процедурой, и только в США ежегодно проводится около 400 000 замен суставов. 1,2 Пациенты, получающие ортопедические протезы, подвержены риску септического артрита, глубоких бактериальных инфекций с вовлечением имплантатов и бактериемии. 3–5 Отказ ортопедических устройств, в основном замены бедренной кости, из-за инфекции приобретает все большее медицинское значение, и после того, как инфекция установлена, пациент должен выдержать длительный режим антимикробной терапии.Кроме того, повторяющиеся неудачи этих методов лечения часто приводят к удалению ортопедических имплантатов и могут потребовать повторной операции. 6–9
Появляется все больше доказательств того, что микробная адгезия и последующая колонизация, ведущая к развитию биопленок, вовлечены в этиологию инфекций, связанных с устройствами. 7,10 Следовательно, эффективное лечение может быть возможным за счет уничтожения бактерий на ранних стадиях колонизации, и непрерывная доставка антибиотиков представляется многообещающим подходом. 11 Хирургическое введение сфер из полиметилметакрилата (ПММА) в очаг инфекции, которые затем выделяют антибиотик в течение примерно 6 недель, 6,10,12,13 было методом выбора в течение последнего десятилетия. Хотя эта система эффективно функционирует с точки зрения доставки антибиотиков и искоренения инфекции, из-за их небиоразлагаемой природы, сферы должны быть удалены, как только васкуляризация области вернется к норме, процесса, которого можно избежать, если доставка биоразлагаемого лекарства система была использована.
Биоразлагаемые синтетические материалы, такие как насыщенные антибиотиками костные трансплантаты, 14 гидроксиапатит-коллагеновые стержни, гидроксиапатит-кальций-фосфатные композиты, 15 кальций-фосфатные костные цементы, 16 полимолочные кислоты и их сополимеры с гликолевыми кислотами, полиангидридами, 12,14,17–19 и полиуретан 20–22 . Эти биоматериалы также использовались в качестве покрывающих веществ на ножках бедренной кости. Преимущество этих синтетических имплантатов в том, что все они полностью метаболизируются в организме человека.Однако они обладают такими недостатками, как снижение pH в месте установки имплантата, что приводит к локализованному воспалению, повреждению тканей и, в конечном итоге, к отказу бедренных имплантатов. 23,24 Полигидроксиалканоаты (ПГА) оказались многообещающими при использовании для покрытия имплантатов, используемых в твердых тканях, благодаря ряду уникальных свойств, таких как пьезоэлектричество, термопластичность, биоразлагаемость и биосовместимость; и при смешивании с антибиотиками они предотвращают бактериальную адгезию. 7,11,25
Полигидроксиалканоаты — это природные полимеры, полученные из бактерий.Поли (3-гидроксимасляная кислота-3-гидроксивалериановая кислота) (ПОБВ) состоит из поли (3-гидроксибутирата) (ПОБ) и различного количества молекул гидроксивалерата (HV). Полимеры PHBV являются биоразлагаемыми и биосовместимыми и фактически способствуют росту костей. 10,11,26,27 В этом исследовании мы оценили физико-химические свойства и характер высвобождения лекарственного средства комплекса PHBV / гентамицин и его влияние на характер роста образующих биопленки Staphylococcus разновидностей in vitro .
Материалы и методы
Изготовление дисков
Диски из бедра (Total Hip System — имплантат с покрытием для использования без цемента: имплантат DePuy Femoral, Варшава, США) были созданы путем разрезания протеза бедра на круглые диски диаметром 9,2 мм и толщиной 2,7 мм.
Приготовление комплекса полимер / антибиотик и покрытие дисков
ПОГБВ с 8% или 12% гидроксивалериановой кислотой было закуплено у Across Organics (Нью-Джерси, США).Один грамм PHBV растворяли в хлороформе и добавляли соответствующее количество гентамицина (Across Organics) для получения содержания антибиотика 2: 1 или 5: 1 (мас. / Мас.). Смесь инкубировали при 55 ° C на водяной бане со встряхиванием и встряхивали до полной гомогенности. Затем смесь полимер / гентамицин выливали в металлическую форму (диаметр 11,5 мм, толщина 5 мм), содержащую ортопедические диски. Диски покрывали и сушили в течение 24 часов. После высыхания диски измеряли электронным штангенциркулем (STM Digimatic Calliper; Дайна, Садбери, Онтарио, Канада) и взвешивали для определения количества покрытия.
Поведение при высвобождении наркотиков
Мы измерили скорость высвобождения гентамицина из комплексов антибиотик / полимер на дисках. Высвобождение гентамицина изучали в 5 мл фосфатно-солевого буфера (PBS, pH 7,4) при 37 ° C в условиях мягкого встряхивания (100 об / мин). Аликвоты по 50 мкл анализировали на гентамицин в моменты времени 0, 0,25, 0,5, 1, 3, 6, 12 и 24 часа, который повторяли через равные промежутки времени в течение 6 недель. Свежий PBS (50 мкл) был добавлен для замены изъятого количества.Концентрацию гентамицина измеряли микробиологическим анализом с использованием Staphylococcus aureus (ATCC 25923; American Type Culture Collection, Manassas, VA, USA), как мы описали ранее. 28 Подобный комплекс полимер / диск без антибиотика служил в качестве контроля, чтобы гарантировать, что весь материал, который элюируется с диска, не влияет на зону ингибирования.
Определение чувствительности к антибиотикам
Использование всего клинического материала в этом проекте было одобрено институциональным наблюдательным советом (IRB) региональной больницы Садбери.Штаммы Staphylococcus haemolyticus и S. aureus , использованные в этом исследовании, представляют собой клинические изоляты инфекций ортопедических имплантатов бедренной кости в региональной больнице Садбери, Садбери, Онтарио, Канада. Бактериальные штаммы тестировали на чувствительность к гентамицину методом разбавления бульона. 29 Минимальная ингибирующая концентрация (МИК) была определена как самая низкая концентрация гентамицина, которая подавляла видимый рост тестируемых бактерий. Все МПК были подтверждены с помощью Microscan (система WalkAway-40SI с LabPro; Dade Behring Inc., Торонто, Онтарио, Канада) в соответствии с инструкциями поставщика. 29
Бактериальная адгезия
Полимерные диски с антибиотиками и металлические диски без покрытия погружали в бактериальные суспензии в PBS (10 8 КОЕ / мл) и инкубировали в течение 5 ч при 37 ° C в статических условиях. 30,31 Образцы переносили в 10 мл бульона Мюллера – Хинтона и инкубировали 3, 24 и 48 ч при 37 ° C. После каждого периода инкубации образцы промывали три раза для удаления неприлипающих бактерий.Затем прикрепленные бактерии удаляли с полимерных поверхностей с помощью ультразвуковой обработки (150 Вт, интервалы 90 с, всего 4,5 мин; ультразвуковой прибор Fisher, Торонто, Канада) и определяли количество колоний жизнеспособных клеток. 31,32
Тест на гемосовместимость
Образцы крови были взяты у 10 здоровых людей, объединены и использованы в течение 2 часов. Дублированные образцы (8 мл) дисков с покрытием или только металлический диск (отрицательный контроль) помещали в 2,5 мл объединенной крови человека.Образцы выдерживали при 37 ° C в течение 2 ч. Одна группа образцов находилась в статическом состоянии, а другая — в динамическом. Мы отбирали образцы каждые 30 минут для анализа крови (CBC) (гематологический аппарат ADVIA 120; Bayer Inc., Торонто, Онтарио, Канада) для анализа биосовместимости полимера с кровью человека в соответствии с рекомендациями ISO. 33,34
Сканирующая электронная микроскопия
Эксперименты по оценке физических характеристик наших комплексов полимер / антибиотик были проведены лабораторией Quantachrome Instruments Laboratory Services (Бойнтон-Бич, Флорида, США).Поверхности полимеров анализировали с помощью автоэмиссионного сканирующего электронного микроскопа (SEM; S-4700, Hitachi Co., Токио, Япония) на образцах, напыленных углеродом. 20 Анализ пористости полимеров проводили на автоматическом анализаторе размера пор (PoreMaster 60; Quantachrome Instruments, Boynton Beach, FL, USA). Прибор измеряет давление, которое прикладывается, чтобы заставить нереактивную несмачивающую жидкость проникнуть в поры. Связь между приложенным давлением и размером поры, в которую будет проникать ртуть, определяется уравнением Уошберна:\ [PD = {-} 4y {\ times} cos {\,} {\ theta} \]
, где P — приложенное давление, D — диаметр, y — поверхностное натяжение ртути (480 дин см -1 ) и θ — угол контакта между ртутью и стенкой поры, обычно около 140 °. .По мере увеличения давления прибор определяет объем проникновения ртути по изменению емкости между столбиком ртути и металлической оболочкой, окружающей шток ячейки для образца. По мере того как столбик ртути укорачивается, данные о давлении и объеме непрерывно собираются и отображаются на специальном компьютере.Анализ данных
Мы использовали тест Стьюдента t (для двух выборок) или ANOVA (для множественных сравнений) с двусторонним анализом после теста Даннета для сравнения средних значений.Значение P ≤0,05 считалось значимым. Результаты представлены в виде средних значений ± среднеквадратичное отклонение. минимум трех независимых экспериментов.
Результаты
Профиль высвобождения гентамицина PHBV 8% и PHBV 12%
Мы сравнили влияние содержания HV (рис. 1) и концентрации гентамицина (рис. 2) на кинетику высвобождения антибиотиков в наших препаратах. После 6 недель инкубации в PBS, PHBV 8% и PHBV 12% с соотношением полимер / гентамицин 5: 1 высвободили 33% и 37% содержащихся в них антибиотиков, соответственно (рис. 1a).Статистически значимые различия в высвобождении антибиотиков были очевидны во все моменты времени ( P < 0,05), что указывает на то, что чем выше содержание HV, тем больше антибиотика будет высвобождено. Однако, когда мы увеличили содержание антибиотиков до 2: 1, мы обнаружили, что полимеры высвобождали меньше антибиотиков за 6-недельный период, независимо от содержания в них HV, хотя различия (33–37% против 29%) не были статистически значимыми.
Чтобы подтвердить наши выводы, мы сравнили влияние концентрации гентамицина на высвобождение антибиотика в параллельном эксперименте с использованием дисков, покрытых полимером / антибиотиком в соотношении 2: 1 и 5: 1.Кривые высвобождения, представленные на рисунке 2, демонстрируют, что увеличение концентрации антибиотика замедляет высвобождение лекарственного средства независимо от состава PHBV и становится статистически значимым ( P <0,05) по мере увеличения времени инкубации, то есть через 5 дней для PHBV 12%. и 18 дней для PHBV 8%.
Влияние содержания антибиотиков на морфологию и пористость полимеров
Мы использовали сканирующую электронную микроскопию (SEM) и анализатор размера пор для исследования однородности и пористости комплексов полимер / антибиотик.Мы показали, что добавление антибиотика делает текстуру полимера более однородной. Как показано на рисунке 3 (a–, образцы PHBV 12% без антибиотика были наименее однородными (а), тогда как образцы PHBV 12% 2: 1 с более высоким содержанием антибиотиков оказались наиболее однородными (c). наблюдались при сравнении изображений PHBV 8% 2: 1 и PHBV 8% 5: 1 (данные не показаны). Кроме того, анализ изображений SEM показал трещины и поверхностные деформации на поверхностях составов, которые остались после растворенного кристаллы лекарственного средства [стрелки на фиг. 3 (d и e)], количество которых прямо пропорционально содержанию гентамицина в формуле.Однако размер поры после выщелачивания был обратно пропорционален концентрации используемого гентамицина; поры PHBV 8% 5: 1 были значительно больше, чем поры PHBV 8% 2: 1 (0,038 мкм ± 0,0001 против 0,015 мкм ± 0,0001, P <0,05), независимо от содержания HV.
При анализе пористости сравнивали количество пор в составе только 8% PHBV с гентамицином во время смешивания или после 6 недель элюирования. Мы протестировали три образца в каждой группе и обнаружили, что после выщелачивания PHBV 8% 2: 1 имеет больше пор, чем PHBV 8% отдельно или свежеприготовленный PHBV 8% 2: 1 (30% против 10% или 15%, соответственно, P <0.05).
Антибактериальное действие комплексов полимер / гентамицин
Мы сравнили адгезию бактерий к полимерам через различные промежутки времени (3, 24 и 48 ч). Мы обнаружили, что все составы, за исключением PHBV 8% 5: 1, значительно снижали количество прикрепленных S. aureus в первые 3 часа инкубации при 37 ° C по сравнению с контролями без антибиотиков (рис. 4a). В конце 24-часовой инкубации S. aureus было уничтожено, в то время как осталось несколько (<100 КОЕ) живых S.haemolyticus (рис. 4b), которые все погибли через 48 часов. Все комплексы полимер / гентамицин, независимо от содержания HV или гентамицина, были способны значительно (<400 КОЕ) после 24-часовой или 48-часовой экспозиции снизить количество прилипших S. aureus и S. haemolyticus . Однако PHBV 8% 5: 1 был наименее эффективным составом, тогда как PHBV 12% 2: 1 был наиболее эффективным составом в этих условиях.
Исследование гемосовместимости
Мы использовали объединенную кровь нормального человека для определения безопасности комплексов полимер / гентамицин in vitro .Ни один из наших составов не изменил количество или морфологию лейкоцитов, эритроцитов или тромбоцитов, независимо от условий эксперимента (статические / нестатические), содержания HV или концентрации гентамицина.
Обсуждение
Анализ изображений SEM показал, что по мере увеличения содержания антибиотика полимеры становятся более однородными. Это явление было связано с встраиванием кристаллов лекарственного средства в полимер, что также затрудняет проникновение PBS во внутреннюю кристаллическую структуру. 10
Увеличение количества кристаллов лекарственного средства в смесях ПОБВ / гентамицин привело к увеличению пористости, что вызвано образованием пустот из-за растворения кристаллов лекарственного средства. Эти пустоты также оставляют кратеры на поверхности полимера. Влияние содержания антибиотика на пористость было больше, чем влияние содержания HV на скорость элюирования антибиотика. Это можно увидеть на рисунке 1 (b), где данные кумулятивного высвобождения для комплексов PHBV с двумя разными концентрациями HV имеют почти одинаковые наклоны из-за одинакового содержания гентамицина.Эти результаты подтверждают, что можно контролировать высвобождение лекарственного средства, контролируя концентрацию кристаллов антибиотика в полимерной матрице.
В экспериментах, посвященных содержанию HV, чем выше содержание HV, тем более кристаллическими и пористыми были полимеры, что приводит к более быстрому высвобождению антибиотиков. Это явление связано с изменением кристалличности ПОБВ при добавлении HV. 10,26,27 Таким образом, увеличение HV с 8% до 12% приводит к более аморфной структуре, что позволяет увеличить водопоглощение.Это ускоряет растворение кристаллов лекарства и приводит к более быстрому высвобождению, как сообщают другие исследователи. 7,10
Во всех экспериментах наблюдалось начальное быстрое высвобождение гентамицина. Этот первоначальный «взрыв» возникает из-за присутствия кристаллов антибиотика на поверхности полимера. Кристаллы лекарства более растворимы, чем полимер, поэтому при их раннем растворении образуются поры или каналы, которые позволяют воде проникать в полимеры. Это ускоряет растворение лекарств внутри полимерной матрицы и, как следствие, приводит к взрывному эффекту.Эффект первоначального взрыва заканчивается, потому что образование каналов заканчивается, когда все лекарства на поверхности, которые находятся в прямом контакте друг с другом, растворяются. После этой точки элюирование больше не является логарифмическим, и наблюдается постоянный характер высвобождения. На этом этапе распад полимера контролирует высвобождение антибиотика, позволяя подвергнуть новые кристаллы лекарства воздействию среды. Фактически, быстрое выбросное высвобождение может быть полезным с терапевтической точки зрения, потому что высокое высвобождение убьет любые бактерии, введенные до или во время операции. 7
Наряду с увеличением гомогенности по мере увеличения содержания антибиотика мы также наблюдали, что количество пор значительно увеличилось после начала элюирования. Этот эффект вызван растворением кристаллов антибиотика в полимерной матрице и прямо пропорционален концентрации лекарства.
Адгезия S. haemolyticus только к PHBV 8% или PHBV 12% и стальных имплантатов без покрытия была практически идентична ( P > 0.05), что указывает на то, что ни полимеры, ни образцы стали не обладают антимикробными свойствами. 35,36 Однако через 24 часа гентамицин-содержащие полимеры, которые высвободили наибольшее количество гентамицина, показали наибольшее снижение количества прикрепившихся бактерий. Анализы адгезии также показали, что S. haemolyticus оставалось на дисках в течение более длительного периода времени (48 часов), чем S. aureus (24 часа), возможно, из-за его более высокого МИК. В целом, наши комплексы полимер / гентамицин показали сходный или превосходящий бактерицидный эффект по сравнению с другими методами ингибирования биопленки 6,22,30,32,37,38 с хорошей биосовместимостью.
В заключение, PHBV 8% и PHBV 12% демонстрируют замедленное высвобождение гентамицина с постоянной скоростью и выше МИК для S. haemolyticus и S. aureus в течение 6 недель. Содержание HV и загрузка лекарства влияют на кинетику высвобождения. Эти комплексы полимер / гентамицин уничтожают S. aureus и устойчивые к гентамицину S. haemolyticus , прилипшие к поверхности, и не оказывают неблагоприятного воздействия на целостность клеток крови. Таким образом, наша недавно разработанная система гентамицина со встроенным полимером может потенциально снизить инфекционные осложнения при хирургии тазобедренного сустава. In vivo исследования показаны для определения безопасности и эффективности этих комплексов в доклинических условиях.
Рисунок 1.
Влияние содержания HV на совокупное высвобождение (%) гентамицина из полимеров PHBV с 8% или 12% HV и содержанием гентамицина 5: 1 (а) или 2: 1 (б). * Значения показали статистически значимые различия (критерий Стьюдента t , P <0,05).
Рисунок 1.
Влияние содержания HV на кумулятивное высвобождение (%) гентамицина из полимеров PHBV с 8% или 12% HV и содержанием гентамицина 5: 1 (a) или 2: 1 (b). * Значения показали статистически значимые различия (критерий Стьюдента t , P <0,05).
Рисунок 2.
Влияние нагрузки лекарством на совокупный процент высвобожденного гентамицина с содержанием гентамицина 5: 1 и 2: 1 и (а) 12% или (б) 8% HV.* Значения показали статистически значимые различия (критерий Стьюдента t , P <0,05).
Рисунок 2.
Влияние нагрузки лекарством на совокупный процент высвобожденного гентамицина с содержанием гентамицина 5: 1 и 2: 1 и (а) 12% или (б) 8% HV. * Значения показали статистически значимые различия (критерий Стьюдента t , P <0,05).
Рис. 3.
СЭМ-изображения полимеров с различной концентрацией гентамицина во время компаундирования и через 6 недель после выщелачивания.Стрелки указывают кратеры и трещины на поверхностях, оставленные растворенными кристаллами лекарственного средства. Масштабные полосы представляют 100 нм. (а) PHBV12; (б) PHBV12 5: 1; (c) PHBV12 2: 1; (d) PHBV12 2: 1, 6 недель; (e) PHBV12 5: 1, 6 недель.
Рис. 3.
СЭМ-изображения полимеров с различной концентрацией гентамицина во время компаундирования и через 6 недель после выщелачивания. Стрелки указывают кратеры и трещины на поверхностях, оставленные растворенными кристаллами лекарственного средства.Масштабные полосы представляют 100 нм. (а) PHBV12; (б) PHBV12 5: 1; (c) PHBV12 2: 1; (d) PHBV12 2: 1, 6 недель; (e) PHBV12 5: 1, 6 недель.
Рисунок 4.
Сравнение влияния комплексов ПОБВ / гентамицин на адгезию чувствительных к гентамицину и резистентных штаммов Staphylococcus . Все составы, кроме PHBV 8% 5: 1, значительно снижали количество прилипших чувствительных к гентамицину S. aureus в первые 3 часа инкубации при 37 ° C (a).С другой стороны, устойчивый к гентамицину S. haemolyticus требовал более длительного периода воздействия (24 часа) для достижения значительного снижения (b).
Рисунок 4.
Сравнение влияния комплексов ПОБВ / гентамицин на адгезию чувствительных к гентамицину и устойчивых к гентамицину штаммов Staphylococcus . Все составы, кроме PHBV 8% 5: 1, значительно снижали количество прилипших чувствительных к гентамицину S. aureus в первые 3 часа инкубации при 37 ° C (a).С другой стороны, устойчивый к гентамицину S. haemolyticus требовал более длительного периода воздействия (24 часа) для достижения значительного снижения (b).
Эта работа частично поддержана исследовательским грантом LURF (Исследовательские фонды Лаврентьевского университета). Мы также благодарны компании Materials and Manufacturing Ontario (MMO) за финансовую поддержку.
Список литературы
1.Дикинсон, Г. М. и Бисно, А. Л. (
1993
). Инфекции, связанные с протезами: клинические аспекты.Международный журнал искусственных органов
16
,749
–54.2.Neut, D., van Horn, J. R., van Kooten, T. G. et al. (
2003
). Выявление инфекций, связанных с биоматериалом, в ортопедических суставных имплантатах.Клиническая ортопедия и сопутствующие исследования
261
–8.3.Гристина А.Г. (
1987
). Инфекция, связанная с биоматериалом: микробная адгезия против тканевой интеграции.Наука
237
,1588
–95.4.Остерманн П. А., Генри С. Л. и Селигсон Д. (
1993
). Роль местной антибактериальной терапии в лечении сложных переломов.Клиническая ортопедия и сопутствующие исследования
102
–11.5.Остерманн, П. А., Генри, С. Л. и Селигсон, Д. (
1994
). Сроки закрытия раны при тяжелых сложных переломах.Ортопедия
17
,397
–9.6.Khardori, N. & Yassien, M. (
1995
).Биопленки при инфекциях, связанных с устройствами.Журнал промышленной микробиологии
15
,141
–7.7.Туресин Ф., Гурсель И. и Хасирчи В. (
2001
). Биоразлагаемые имплантаты из полигидроксиалканоата для лечения остеомиелита: высвобождение антибиотиков in vitro.Journal of Biomaterial Science Polymer Edition
12
,195
–207.8.Сандерсон П. Дж. (
1989
). Предотвращение инфицирования ортопедических имплантатов.Журнал антимикробной химиотерапии
24
,277
–80.9.Sheehan, E., McKenna, J., Mulhall, K. J. et al. (
2004
). Адгезия стафилококка к ортопедическим металлам, исследование in vivo.Журнал ортопедических исследований
22
,39
–43.10.Гурсельт И., Ягмурлу Ф., Коркусуз Ф. et al. (
2002
). Высвобождение антибиотика in vitro из стержней поли (3-гидроксибутират-со-3-гидроксивалерат).Журнал микрокапсулирования
19
,153
–64.11.Коркусуз Ф., Коркусуз П., Эксиоглу Ф. et al. (
2001
). Реакция in vivo на биоразлагаемые системы с контролируемым высвобождением антибиотиков.Журнал исследований биомедицинских материалов
55
,217
–28.12.Канеллакопулу, К. и Джамареллос-Бурбулис, Э. Дж. (
2000
). Системы-носители для местной доставки антибиотиков при костных инфекциях.Лекарственные препараты
59
,1223
–32,13.Калхун, Дж. Х., Генри, С. Л., Энгер, Д. М. et al. (
1993
). Лечение инфицированных несращений гранулами гентамицин-полиметилметакрилатного антибиотика.Клиническая ортопедия и сопутствующие исследования
23
–7.14.Нельсон, К. Л., Хикмон, С. Г. и Скиннер, Р. А. (
1997
). Лечение экспериментального остеомиелита хирургической обработкой раны и имплантацией биоразлагаемых шариков из полиангидрида-гентамицина.Журнал ортопедических исследований
15
,249
–55.15.Коркусуз Ф., Учида А., Синто Ю. и др. (
1993
). Экспериментальный остеомиелит, связанный с имплантатом, лечится керамическими композитами антибиотик-гидроксиапатит кальция.Журнал костной и суставной хирургии
75
,111
–4.16.Thoma, K. & Schlutermann, B. (
1992
). Взаимосвязь производственных параметров и фармацевтически-технологических требований к биоразлагаемым микрочастицам.2. Приготовление инъекционных микрочастиц в биоразлагаемом полиэфире.Аптека
47
,115
–9,17.Санчес Э., Баро М., Сориано И. и др. (
2001
). Исследование in vivo-in vitro биоразлагаемых и остеоинтегрируемых костных имплантатов с гентамицином.Европейский журнал фармацевтики и биофармацевтики
52
,151
–8.18.Husmann, M., Schenderlein, S., Luck, M. et al. (
2002
).Эрозия полимеров в микрочастицах PLGA, полученных методом фазового разделения.Международный фармацевтический журнал
242
,277
. 19.Феррейра, Б. М. П., Завалья, К. А. К. и Дуэк, Э. А. Р. (
2001
). Пленки смесей поли (L-молочная кислота) / поли (гидроксибутират-гидроксивалерат): разложение in vitro.Исследование материалов
4
,34
–42.20.Рицци, С. К., Хит, Д. Дж., Кумбс, А. Г. et al. (
2001
). Биоразлагаемые композиты полимер / гидроксиапатит: анализ поверхности и начальное прикрепление человеческих остеобластов.Журнал исследований биомедицинских материалов
55
,475
–86.21.Сандерс, Дж. Э., Бейл, С. Д. и Нойман, Т. (
2002
). Тканевая реакция на микроволокна из различных полимеров: полиэфира, полиэтилена, полимолочной кислоты и полиуретана.Журнал исследований биомедицинских материалов
62
,222
–7.22.Schierholz, J. M., Steinhauser, H., Rump, A. F. et al. (
1997
). Контролируемое высвобождение антибиотиков из биомедицинских полиуретанов: морфологические и структурные особенности.Биоматериалы
18
,839
–44,23.Adams, K., Couch, L., Cierny, G. et al. (
1992
). Оценка in vitro и in vivo диффузии антибиотиков из гранул из полиметилметакрилата, пропитанных антибиотиком.Клиническая ортопедия и сопутствующие исследования
244
–52.24.Бухгольц, Х. В., Элсон, Р. А. и Хайнерт, К. (
1984
). Акриловый цемент, содержащий антибиотики: современные концепции.Клиническая ортопедия и сопутствующие исследования
96
–108.25.Андерсон, А. Дж., Хейвуд, Г. В. и Дауэс, Э. А. (
1990
). Биосинтез и состав бактериальных поли (гидроксиалканоатов).Международный журнал биологических макромолекул
12
,102
–5.26.Ягмурлу, М.Ф., Korkusuz, F., Gursel, I. et al. (
1999
). Система местной доставки антибиотиков сульбактам-цефоперазон полигидроксибутират-ко-гидроксивалерат (PHBV): эффективность и биосовместимость in vivo при лечении экспериментального остеомиелита, связанного с имплантатами.Журнал исследований биомедицинских материалов
46
,494
–503.27.Сендил Д., Гурсель И., Вайз Д. Л. et al. (
1999
). Высвобождение антибиотика из биоразлагаемых микрочастиц PHBV.Журнал контролируемого выпуска
59
,207
–17.28.Омри А., Сантрес З. Э. и Шек П. Н. (
2002
). Повышенная активность липосомального полимиксина B против Pseudomonas aeruginosa на модели легочной инфекции на крысах.Биохимическая фармакология
64
,1407
–13.29.Национальный комитет по клиническим лабораторным стандартам. (
2001
). Стандарты производительности для испытаний на чувствительность к противомикробным препаратам.М100-С10 . NCCLS, Уэйн, Пенсильвания, США 30.Konig, D. P., Perdreau-Remington, F., Rutt, J. et al. (
1998
). Производство слизи Staphylococcus epidermidis: повышенная адгезия бактерий и их накопление на чистом титане.Acta Orthopaedica Scandinavica
69
,523
–6.31.Шерерц, Р. Дж., Раад, И. И., Белани, А. и др. (
1990
). Трехлетний опыт работы с ультразвуковыми культурами сосудистых катетеров в лаборатории клинической микробиологии.Журнал клинической микробиологии
28
,76
–82.32.Кониг, Д. П., Ширхольц, Дж. М., Хильгерс, Р. Д. et al. (
2001
). Прилипание и накопление Staphylococcus epidermidis RP 62 A и Staphylococcus epidermidis M7 in vitro на четырех различных костных цементах.Архив хирургии Лангенбека
386
,328
–32.33.Сейферт, У. Т., Биль, В. и Шенк, Дж. (
2002
).Тестирование гемосовместимости биоматериалов in vitro в соответствии с ISO 10993-4.Биомолекулярная инженерия
19
,91
–6.34.Biehl, V., Wack, T., Winter, S. et al. (
2002
). Оценка гемосовместимости биоматериалов на основе титана.Биомолекулярная инженерия
19
,97
–101.35.Konig, D. P., Perdreau-Remington, F., Rutt, J. et al. (
1999
).Прилипание и накопление S. epidermidis на различных биоматериалах из-за образования внеклеточной слизи. Сравнение in vitro штамма, продуцирующего слизь (Rp 62 A), и его изогенного слизисто-отрицательного мутанта (M7).Zentralblatt für Bakteriologie
289
,355
–64,36.Степанович, С., Джукич, Н., Опавски, Н. и др. (
2003
). Значение размера инокулята в формировании биопленок стафилококками.Новая микробиология
26
,129
–32.37.Amorena, B., Gracia, E., Monzon, M. et al. (
1999
). Анализ чувствительности к антибиотикам для золотистого стафилококка в биопленках, разработанных in vitro.Журнал антимикробной химиотерапии
44
,43
–55.38.Олсон, М. Э., Цери, Х., Морк, Д. В. et al. (
2002
). Биопленочные бактерии: образование и сравнительная чувствительность к антибиотикам.Канадский журнал ветеринарных исследований
66
,86
–92.Заметки автора
1 Кафедра химии и биохимии, Лаврентийский университет, 935 Ramsey Lake Road, Садбери, Онтарио, Канада P3E 2C6; 2Отдел биомедицинских исследований, Центр здоровья Техасского университета, 11937 US Highway 271, Tyler, TX 75708, USA
JAC vol.54 №6 © Британское общество антимикробной химиотерапии, 2004; все права защищены
Вмешательства по замене отсутствующих зубов: антибиотики при установке дентальных имплантатов для предотвращения осложнений
Обзорный вопрос
Этот обзор, проведенный авторами Кокрановской группы по гигиене полости рта, был подготовлен для оценки возможных преимуществ антибиотиков, принимаемых перорально. время установки дентального имплантата с целью предотвращения инфицирования.Если показано, что антибиотики помогают предотвратить инфекцию, в этом обзоре также делается попытка установить, какой тип, дозировка и продолжительность лечения являются наиболее эффективными. Использование антибиотиков для предотвращения инфекций в имплантационной стоматологии является спорным вопросом, и существует необходимость ответить на эти вопросы, чтобы улучшить показатели успешности зубных имплантатов при минимизации осложнений, вреда или побочных эффектов.
Предпосылки
Отсутствующие зубы иногда можно заменить дентальными имплантатами, к которым можно прикрепить коронку, мостовидный протез или протез.Бактерии, занесенные во время установки имплантата, могут привести к инфекции, а иногда и к отказу имплантата. Инфекции вокруг биоматериалов (например, зубных имплантатов) трудно поддаются лечению, и почти все инфицированные имплантаты необходимо удалять, поэтому так важно по возможности предотвратить инфекцию.
Было высказано предположение, что пероральный прием антибиотиков до или после установки (или обоих) может минимизировать вероятность заражения.
Как правило, использование антибиотиков в хирургии для предотвращения инфекции рекомендуется только людям из группы риска, когда операция обширна или проводится на инфицированных участках, а также когда в организм имплантируются большие инородные материалы.В последнее время рекомендуется краткосрочный курс антибиотиков, когда необходимо использовать антибиотики, потому что иногда антибиотики могут вызывать побочные эффекты, которые варьируются от диареи до опасных для жизни аллергических реакций. Еще одна серьезная проблема, связанная с широким использованием антибиотиков, — это увеличение числа устойчивых к антибиотикам бактерий.
Характеристики исследования
Доказательства, на которых основан этот обзор, были актуальными по состоянию на 17 июня 2013 года. Было включено шесть испытаний с общим числом участников 1162.
Во всех шести этих испытаниях сравнивали использование антибиотиков для предотвращения инфекции (неудач и осложнений) с отсутствием лечения или лечением плацебо (поддельное лекарство без активного ингредиента). Во всех исследованиях использовался антибиотик амоксициллин; дозы и время введения доз варьировались, хотя в большинстве использовалась разовая доза, принимаемая непосредственно перед установкой имплантата. В одном из испытаний с участием 100 человек также рассматривались разные дозы амоксициллина, принимаемые в разное время.
Не было испытаний, в которых рассматривались бы альтернативные антибиотики.
Участниками были люди старше 18 лет, которые могли дать согласие на участие в медицинском исследовании. Потенциальные участники были исключены по ряду причин, в том числе: если они были подвержены риску сердечных заболеваний, имели искусственные суставы, имели проблемы с иммунной системой, страдали диабетом, прошли лучевую терапию в области головы и шеи, нуждались в лечении. дополнительные процедуры во время установки имплантата, аллергия на пенициллин, наличие хронических / острых инфекций рядом с запланированным местом имплантации, лечение антибиотиками по каким-либо другим причинам (или принимавшее их не более шести месяцев назад), проходили лечение или получали амино-бисфосфонаты внутривенно, были беременны или кормили грудью, получали длительную терапию нестероидными противовоспалительными препаратами или имели проблемы со свертыванием крови.Срок наблюдения во всех исследованиях составлял не менее трех месяцев.
Ключевые результаты
Похоже, что пероральное введение двух граммов амоксициллина за час до установки дентальных имплантатов эффективно в сокращении количества отказов имплантатов. В частности, введение антибиотиков 25 людям позволит избежать потери имплантата у одного человека. До сих пор неясно, полезны ли послеоперационные антибиотики или какие антибиотики работают лучше всего.
Качество доказательств
Доказательства шести испытаний (1162 участника), в которых сравнивалось использование антибиотиков с плацебо или отсутствием лечения, были признаны среднего качества.Однако в одном испытании (100 участников), в котором изучались антибиотики, назначаемые в течение разного периода времени, был обнаружен высокий риск систематической ошибки.
Антибиотики — тесты и лечение
Антибиотики используются для лечения или профилактики некоторых видов бактериальных инфекций. Они работают, убивая бактерии или предотвращая их размножение и распространение.
Антибиотики неэффективны против вирусных инфекций, таких как простуда, грипп, кашель и боль в горле.
Многие легкие бактериальные инфекции также могут излечиваться вашей иммунной системой без использования антибиотиков, поэтому они обычно не назначаются.
Важно, чтобы антибиотики назначались и принимались правильно, чтобы предотвратить прогрессирование устойчивости к антибиотикам. Это когда штамм бактерий больше не реагирует на лечение одним или несколькими типами антибиотиков.
Когда используются антибиотики
Антибиотики могут использоваться для лечения бактериальных инфекций, которые:
- вряд ли вылечится без антибиотиков
- может заразить других без лечения
- может занять слишком много времени для очистки без обработки
- несут риск более серьезных осложнений
Людям с высоким риском заражения также могут назначать антибиотики в качестве меры предосторожности, известной как антибиотикопрофилактика.
Подробнее о применении антибиотиков.
Как мне принимать антибиотики?
Принимайте антибиотики в соответствии с указаниями на упаковке или в информационном буклете для пациента, который прилагается к лекарству, либо в соответствии с указаниями вашего терапевта или фармацевта.
Дозы антибиотиков могут быть предоставлены несколькими способами:
- Пероральные антибиотики — таблетки, капсулы или жидкость, которую вы пьете, которые можно использовать для лечения большинства типов инфекций организма от легкой до средней степени тяжести
- антибиотики для местного применения — кремы, лосьоны, спреи или капли, которые часто используются для лечения кожных инфекций
- инъекций антибиотиков — их можно вводить в виде инъекций или вливаний через капельницу непосредственно в кровь или мышцу, и обычно они предназначены для более серьезных инфекций
Важно закончить назначенный курс лечения антибиотиками, даже если вы почувствуете себя лучше, если только медицинский работник не скажет вам иное.Если вы прекратите прием антибиотика в середине курса, бактерии могут стать устойчивыми к антибиотику.
Пропущена доза антибиотиков
Если вы забыли принять дозу антибиотиков, примите эту дозу, как только вспомните, а затем продолжайте курс антибиотиков в обычном режиме.
Но если почти пришло время для следующей дозы, пропустите пропущенную дозу и продолжайте свой обычный график дозирования. Не принимайте двойную дозу, чтобы восполнить пропущенную.
Существует повышенный риск побочных эффектов, если вы примете 2 дозы ближе друг к другу, чем рекомендуется.
Случайно принял дополнительную дозу
Случайный прием одной дополнительной дозы антибиотика вряд ли причинит вам серьезный вред.
Но это увеличит ваши шансы испытать побочные эффекты, такие как боль в животе, диарея, чувство или тошнота.
Если вы случайно приняли более одной дополнительной дозы антибиотика, обеспокоены или испытываете серьезные побочные эффекты, как можно скорее обратитесь к своему терапевту или позвоните в службу NHS 24 111.
Побочные действия антибиотиков
Как и любые лекарства, антибиотики могут вызывать побочные эффекты. Большинство антибиотиков не вызывают проблем при правильном применении, а серьезные побочные эффекты возникают редко.
К наиболее частым побочным эффектам относятся:
- болеет
- плохое самочувствие
- Вздутие живота и расстройство желудка
- понос
У некоторых людей может быть аллергическая реакция на антибиотики, особенно на пенициллин и цефалоспорины.В очень редких случаях это может привести к серьезной аллергической реакции (анафилаксии), требующей неотложной медицинской помощи.
Узнайте больше о побочных эффектах антибиотиков.
Соображения и взаимодействия
Некоторые антибиотики не подходят людям с определенными заболеваниями, а также беременным или кормящим женщинам. Вам следует принимать только те антибиотики, которые вам прописаны — никогда не «одалживайте» их у друга или члена семьи.
Некоторые антибиотики могут также непредсказуемо реагировать с другими лекарствами, такими как оральные противозачаточные таблетки и алкоголь.Важно внимательно прочитать информационную брошюру, прилагаемую к вашему лекарству, и обсудить любые проблемы с фармацевтом или терапевтом.
Подробнее о взаимодействии антибиотиков с другими лекарствами
Виды антибиотиков
Существуют сотни различных типов антибиотиков, но большинство из них можно условно разделить на шесть групп. Они описаны ниже.
- пенициллины (такие как пенициллин и амоксициллин) — широко используются для лечения различных инфекций, включая кожные инфекции, инфекции грудной клетки и инфекции мочевыводящих путей
- цефалоспорины (например, цефалексин) — используются для лечения широкого спектра инфекций, но некоторые также эффективны для лечения более серьезных инфекций, таких как сепсис и менингит. Аминогликозиды
- (такие как гентамицин и тобрамицин) — как правило, используются только в больницах для лечения очень серьезных заболеваний, таких как сепсис, поскольку они могут вызывать серьезные побочные эффекты, включая потерю слуха и повреждение почек; их обычно вводят в виде инъекций, но можно давать в виде капель при некоторых ушных или глазных инфекциях
- тетрациклины (такие как тетрациклин и доксициклин) — могут использоваться для лечения широкого спектра инфекций, но обычно используются для лечения умеренных и тяжелых угрей и розацеа Макролиды
- (такие как эритромицин и кларитромицин) — могут быть особенно полезны для лечения инфекций легких и грудной клетки, или как альтернатива для людей с аллергией на пенициллин, или для лечения устойчивых к пенициллину штаммов бактерий
- фторхинолоны (такие как ципрофлоксацин и левофлоксацин) — антибиотики широкого спектра действия, которые можно использовать для лечения широкого спектра инфекций
Устойчивость к антибиотикам
Как NHS, так и организации здравоохранения по всему миру пытаются сократить использование антибиотиков, особенно при несерьезных состояниях.


