Что нужно знать о бактериальном вагинозе
Многие женщины сталкиваются с симптомами влагалищного дисбиоза. Обильные выделения, молочно-серого цвета и с неприятным запахом часто путают с «молочницей» и проводят «соответствующее» самолечение.
В большинстве случаев, такая стратегия быстрее навредит, чем поможет, поскольку причиной может быть бактериальный вагиноз (БВ).
Что такое баквагиноз
Согласно официальному определению, это невоспалительное заболевание влагалища, характеризующееся резким снижением или полным отсутствием лактофлоры и её заменой на анаэробные бактерии, среди которых наиболее распространены Gardnerella vaginalis (гарднерелла) и Atopobium vaginae (атопобиум).
У здоровых женщин репродуктивного возраста влагалищный микробиом на 95% представлен лактобактериями. Их способность к кислотообразованию (молочная кислота) и продукции перекиси водорода способствует поддержанию кислого pH и подавлению роста остальных микроорганизмов.
Оставшиеся 5% микрофлоры занимают более 300 видов аэробных и анаэробных микроорганизмов, среди которых:
- грамположительные палочки — Corynebacterium spp.
 , Eubacterium spp., Bifidobacterium spp., Propionibacterium spp., Clostridium spp.;
, Eubacterium spp., Bifidobacterium spp., Propionibacterium spp., Clostridium spp.; - грамотрицательные палочки (14-55%) — Bacteroides spp., Fusobacterium spp., Prevotella spp., Porphyromonas spp., Leptotrichia spp.;
- грамположительные кокки (30-80%) — Peptostreptococcus spp., Peptococcus spp., Staphylococcus spp., Micrococcus varians, Enterococcus spp., Streptococcus viridans и др.
- грамотрицательные кокки — Veilonella spp., Acidominococcus fermentans, непатогенные Neisseria spp.,
- энтеробактерии — Echerihia coli, Klebsiella spp., Enterobacter spp., Citrobacter spp. и др.
Все это многообразие бактерий является частью нормального «женского» биоценоза, не вызывая симптомов и не требуя лечения. Однако это правомерно до тех пор, пока их численность лактобацилл не начинает снижаться, а остальных — расти.
Факторы риска и симптомы
Почему происходит такой «сдвиг» — достоверно пока не известно. Однако к факторам риска относят:
- ранее перенесенные воспалительные заболевания половых путей,
- длительный и бесконтрольный прием антибиотиков,
- гормональные нарушения (расстройства менструального цикла),
- длительное применение ВМС,
- прием оральных контрацептивов.

Колонизация влагалища микрофлорой, связанной с баквагинозом, особенно Gardnerella vaginalis и Atopobium vaginae, сопровождается:
- сдвигом pH в щелочную сторону (>4,5),
- появлением обильных (иногда пенистых) выделений молочно-серого цвета
- появлением характерного «рыбного» запаха, усиливающегося при защелачивании среды (половой контакт, менструация).
Отека и покраснения обычно не наблюдается, что является отличительным признаком от банального вагинита и кандидоза влагалища («молочницы»).
Диагностика
Самым простым, но косвенным, признаком нарушения влагалищной микрофлоры служит повышение pH >4,5. Для проведения такого «анализа» требуются всего лишь тест-полоски для измерения рН, доступные к покупке в любой аптеке. Однако, чтобы выявить возбудителя и начать адекватную терапию такой диагностики, конечно, недостаточно.
Современным и высокоточным методом диагностики влагалищных дисбиозов служит комплексное исследование «Флороценоз».
Этот тест разработан научными специалистами совместно с практикующими клиницистами. И предназначен для определения состава и соотношения нормальной и условно-патогенной флоры влагалища методом ПЦР.
Исследование представлено в 3-х вариантах для различных клинических ситуаций:
1. Флороценоз – бактериальный вагиноз
Название теста «говорит само за себя», а в результате будет отражено количество:
- всех обнаруженных бактерий,
- ДНК Lactobacillus spp.,
- ДНК Atopobium vaginae,
- ДНК Gardnerella vaginalis.
2. В случае, когда есть подозрения на нарушения более «широкого спектра», к применению рекомендован «Флороценоз», включающий подсчет:
- ДНК всех бактерий,
- ДНК Lactobacillus spp.,
- Gardnerella vaginalis
- и Atopobium vaginae,
- ДНКвозбудителейаэробноговагинита
- Enterobacteriaceae,
- Staphylococcus spp.
 ,
, - Streptococcus spp.,
- ДНК условно-патогенных микоплазм
- Ureaplasma urealyticum,
- Ureaplasma parvum,
- Mycoplasma hominis,
- ДНК возбудителей кандидоза («молочницы»)
- Candida albicans,
- Candida glabrata,
- Candida paraps./ tropicalis.
3. При необходимости в дополнительной диагностике ИППП – подходит «Флороценоз – комплексное исследование», включающий в себя подсчет «классического состава» бактерий + выявление ДНК «виновников» ИППП:
- Neisseria gonorrhoeae (гонокок)
- Chlamydia trachomatis (хламидия)
- Mycoplasma genitalium (микоплазма гениталиум)
- Trichomonas vaginalis (трихомонада)
Готовность анализов составляет 4-5 дней, а результат можно получить по электронной почте, в личном кабинете на сайте или в любом удобном отделении KDL.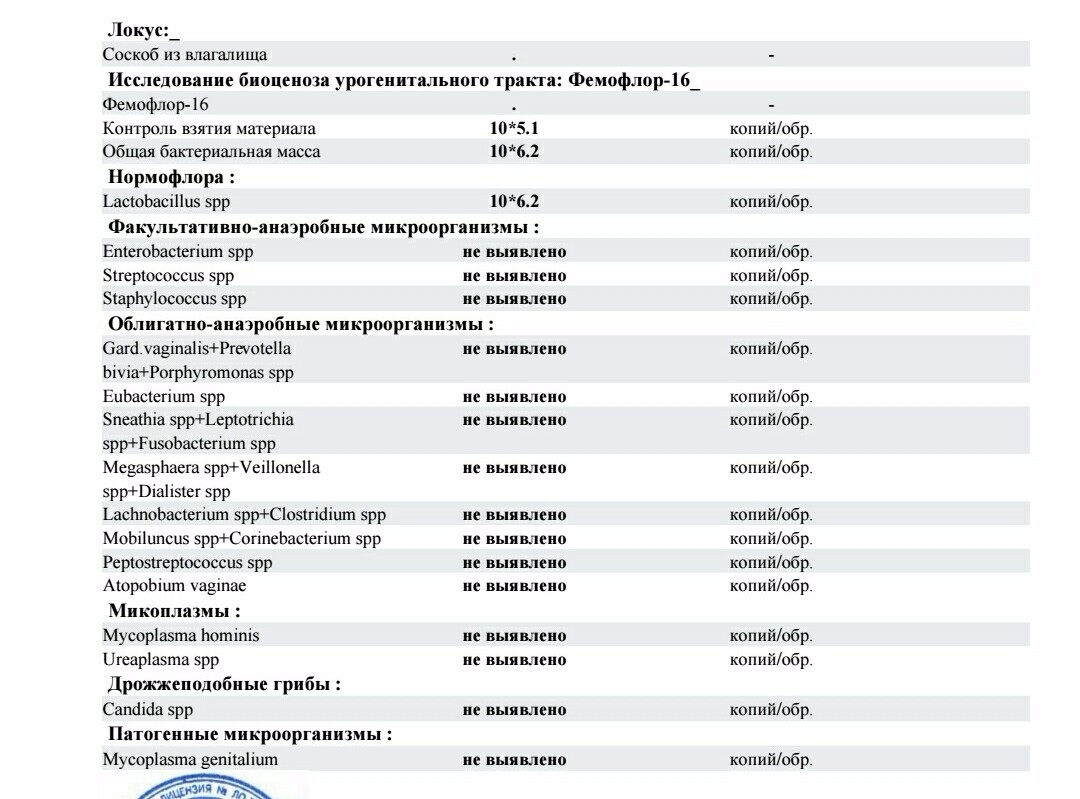
Поделиться статьей:
Остались вопросы?Streptococcus spp в мазке у женщин норма
Стрептококк в мазке у женщин выявляется с помощью лабораторных исследований. Когда такой результат является нормой, а что считать патологией?
Чтобы безошибочно разобраться в цифрах на бланке, нужно знать, что такое гинекологическая стрептококковая инфекция и чем она опасна.
Кто такие стрептококки?
Стрептококки – очень распространенные микроорганизмы, паразиты животных и людей.
Среди них есть настоящие универсалы – например, стрептококк gallolyticus. Он может обитать в организмах практически любых теплокровных существ – от человека до мышей.
Большинство разновидностей стрептококков условно патогенны, то есть могут стать причиной болезни только в ослабленном организме. У здорового человека стрептококки никак не проявляют себя.
О чем говорит присутствие бактерий в гинекологическом мазке?
Если анализы показали присутствия стрептококка во влагалище, особых поводов для беспокойства нет. Но и пренебрегать результатами лабораторного исследования не стоит – стрептококковая инфекция может развиться в любое время. Нужно обратиться гинекологу, чтобы специалист назначил лечение, если в нем есть необходимость.
Во влагалище могут находиться гемолитические стрептококки следующих разновидности:
- группы А (anginosus и др.) – обычно обитают на коже, но могут оказаться и во влагалище, где провоцируют омертвение тканей и токсический шок;
- группы Б – обнаруживаются в основном у беременных, способны проходить через плаценту, инфицировать плод и вызывать выкидыши.
Все гемолитические стрептококки очень опасны для беременных женщин, так как во время родов могут переходить на новорожденных, вызывая серьезные осложнения. Для небеременной женщины они опасны только условно, так как здоровая флора влагалища не дает им массово размножаться и выделять много токсинов.
Для небеременной женщины они опасны только условно, так как здоровая флора влагалища не дает им массово размножаться и выделять много токсинов.
Если выявить вид бактерий не удалось, в бланке с результатами анализа будет написано streptococcus spp. Это означает, что в лаборатории определили только родовую принадлежность микробов, а более детальные исследования не увенчались успехом или их не проводили, так как в этом не было необходимости.
У здоровой женщины в мазке обычно обнаруживается немного стрептококков следующих разновидностей:
Стрептококковая инфекция влагалища вызывает те же болезни, что и золотистый стафилококк, но развивается более медленно.
Симптомы гинекологической стрептококковой инфекции:
- зуд и боль в гениталиях, желто-кровянистая слизь;
- боли в почечной области и животе;
- нерегулярный менструальный цикл.
По симптомам стрептококковая инфекция влагалища похожа на гонорею. Чтобы точно определить болезнь, врач должен провести дифференциальное обследование.
Причины инфекции
В силу различных причин даже вполне безобидная флора может развиться в тяжелые инфекции. Основные из них:
- нерациональный прием антибиотиков, из-за чего нарушается нормальная флора влагалища;
- изменения гормонального фона, которые происходят из-за беременности, грудного кормления, приема гормонсодержащих препаратов;
- ослабление иммунитета из-за неправильного образа жизни, стрессов инфекционных заболеваний;
- неправильный уход за влагалищем, в том числе частое спринцевание дезинфицирующими растворами, приводящее к гибели полезных лактобацилл;
- частая смена интимных партнеров без использования барьерных средств защиты.
В отличие от гонореи, вагинальная инфекция, вызванная стрептококком, лечится быстро, не оставляя осложнений. Чтобы полностью выздороветь, нужно выполнять все рекомендации врача.
Доктор назначит антибиотик или другой антибактериальный препарат, который нужно обязательно пропить рекомендованным курсом. Если же надолго отложить визит к специалисту, инфекция может привести к серьезным осложнениям.
Если же надолго отложить визит к специалисту, инфекция может привести к серьезным осложнениям.
При беременности
Кокки группы Б – самая распространенная причина инфекций у беременных женщин и новорожденных малышей. Они обнаруживаются в микрофлоре влагалища почти 25% будущих мам.
Мазок на стрептококк B (агалактию) – обязательный перед родами анализ. Чем больше стрептококков находится во влагалище, тем больше вероятность заражения ребенка, когда он будет продвигаться по родовым путям.
Агалактия проявляется у беременных на 32-33 неделе вынашивания. Особенно велика вероятность обнаружения стрептококков у беременных младше 20 лет.
Streptococcus agalactiae не опасен для самой женщины, но очень опасен для новорожденного. Дети могут инфицироваться от матери, являющейся бессимптомной носительницей бактерий этой разновидности.
Результат заражения трагичен: пневмония, менингит и сепсис. Смертность младенцев от стрептококковой инфекции доходит до 30 %.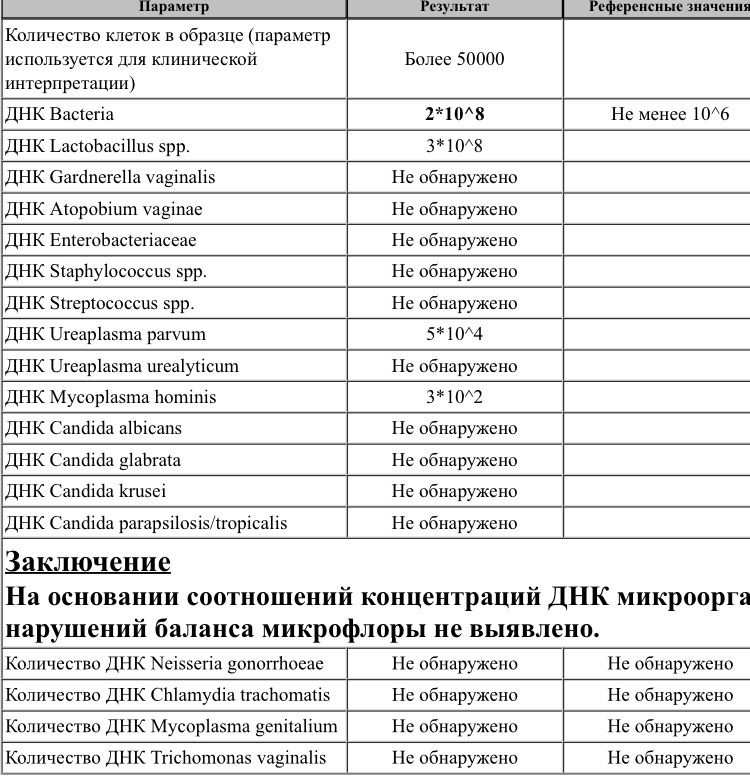 Поэтому любая беременная, у которой выявлено аномально большое количество агалактии, должна пройти санацию – пролечиться до полного исчезновения микроба.
Поэтому любая беременная, у которой выявлено аномально большое количество агалактии, должна пройти санацию – пролечиться до полного исчезновения микроба.
Стрептококки в мазке у женщин – довольно частое явление. Эта бактерия одна из самых распространенных на Земле, она может обитать почти в любой среде, даже в неподходящих условиях и при ослаблении защитных сил организма существенно вредить здоровью человека. В обычном состоянии здоровья незначительное количество стрептококка отображает лишь естественный состав влагалищной среды.
Микроорганизмы могут распространяться по всему организму, но более благоприятные условия для их проживания имеются на коже и слизистых оболочках. Есть много вариантов обнаружения инфекции, но чтобы ее выявить достаточно провести исследование мазка.
Варианты заражения
Патологические симптомы возникают только в случае благоприятной среды для этого. Инфекция передается несколькими способами:
- контактно;
- половым путем;
- внутриутробное;
- воздушно-капельное заражение.

Повод для беспокойства – инфицирование дыхательных путей, такое случается при скарлатине или ангине.
Стрептококки сохраняют способность к жизнедеятельности порядка трех месяцев в порошковых биологических веществах. Симптомы заражения могут возникнуть во время контакта с инфекционным носителем или человеком с уже проявленными признаками болезни. При повышении температуры до 60 и более градусов вирус гибнет. Уничтожается бактерия также под влиянием химических веществ: моющих средств, шампуня и прочего. Причины размножения стрептококка следующие:
- сбои гормонального баланса;
- ослабление иммунных сил;
- заражение другими вирусами;
- хронические болезни, подрывающие защиту организма от инфекций;
- повышенная чувствительность к бактериям.
Вызывает распространение стрептококков также прием антибактериальных средств. Такое лечение негативно отражается на состоянии микрофлоры и провоцирует состояние, при котором отмечается преобладание кокков над другими бактериями.
Симптоматика
Стрептококковая инфекция в гинекологии может проявляться различными признаками, все определяется тем, какие заболевания развились вследствие активности бактерии. Но есть и характерные симптомы:
- болезненные ощущения и зуд промежности;
- выделения желтоватого цвета с кровянистыми примесями;
- острые или тянущие боли в нижней части живота, пояснице;
- сбои месячного цикла.
Вагинальная инфекция быстро лечиться при своевременном вмешательстве специалиста, не оставляя значительных последствий. Но если откладывать гинекологический осмотр, то бактерия вызывает серьезные осложнения.
Стоит отметить, что симптомы инфицирования стрептококком сильно напоминают проявление гонореи и потому их часто путают. Чтобы предельно достоверно определить причину патологического состояния и установить, что норма, а что отклонение, врач принимает решение о целесообразности проведения дифференциального обследования.
Стрептококки у беременных
Условно-патогенная бактерия может находиться в пищеварительной системе, симптомы не развиваются. Почти у 40% представительниц женского пола, вынашивающих ребенка, имеется стрептококк агалактия. Этот подтип инфекции можно обнаружить исключительно у беременных на 32-33 неделе срока. Бактерия сильно влияет на женский организм, может спровоцировать ранние роды или даже смерть плода.
Почти у 40% представительниц женского пола, вынашивающих ребенка, имеется стрептококк агалактия. Этот подтип инфекции можно обнаружить исключительно у беременных на 32-33 неделе срока. Бактерия сильно влияет на женский организм, может спровоцировать ранние роды или даже смерть плода.
Стоит обратить внимание: стрептококковая инфекция вызывает те же заболевания, что и золотистый стафилококк. Отличие заключается только в клинической картине болезни и в скорости развития патологии.
Есть факторы, повышающие вероятность распространения инфекции:
- выявление стрептококков подтипа В в моче;
- молодой возраст беременной, менее 20;
- угроза преждевременного начала процесса рождения;
- заражение инфекцией предыдущих детей.
Стрептококк подтипа агалактия преимущественно вызывает воспалительные и инфекционные процессы в мочеполовой системе, но случается и развитие таких заболеваний, как эндометрит, эндокардит, пневмония. Вынашивание ребенка сильно подрывает женский организм, в этот период иммунитет сильно ослаблен, поэтому вероятность распространения инфекции существенно повышается. Чтобы предупредить проблему, гинекология рекомендует внимательно относиться к состоянию своего здоровья и выполнять все правила относительно личной гигиены.
Чтобы предупредить проблему, гинекология рекомендует внимательно относиться к состоянию своего здоровья и выполнять все правила относительно личной гигиены.
Лечебные мероприятия
Антибактериальная терапия инфекционной болезни – это норма, так как стрептококки устойчивы и сложно поддаются лечению. Препарат побирается после проведенного анализа, которым определяется реакция бактерии на те или иные средства. Лечение могут назначать разные специалисты: педиатр, терапевт, гинеколог, хирург и другие врачи. Все зависит от формы проявления инфекции.
При обнаружении первичных форм стрептококка чаще всего назначается прием антибактериальных средств пенициллинового ряда. Если пятидневный курс не привел к выздоровлению, то это признак подбора неправильного препарата, тогда антибиотик отменяют. Используют Эритромицин, Сумамед, Азитромицин, Цифран и так далее. Препараты тетрациклинового ряда не являются эффективными при лечении стрептококка.
Дополнительно применяются методы лечения, направленные на устранение симптомов, которые зависят от клинического проявления болезни.
При вторичном распространении инфекции проведение длительных курсов приема антибактериальных препаратов – это норма. Здесь применяют средства с пролонгированным действием. По необходимости дополняют терапию иммуномодулирующими средствами.
Особенности стрептококковой инфекции в гинекологии
Инфицирование стрептококком может произойти где угодно, бактерия присутствует везде и чаще всего поражает слизистые, ткани. Заражение может случиться в медицинском заведении, роддоме, общественном месте. Стрептококки проникают в организм при повреждении покровов.
Если имеется воспалительный процесс в органах, например, малого таза, то инфицирование может произойти при незащищенном половом акте. Патологические проблемы ослабляют женский организм, что повышает вероятность распространения инфекции.
Заключение
Именно стрептококки – наиболее распространенный вид, сохраняющий жизнеспособность практически в любой среде. Распространение патогенного микроба происходит при снижении способности организма сопротивляться заболеваниям. Бактерии проходят в дыхательную систему, где начинают стремительное размножение, отравляя вредоносными веществами.
Бактерии проходят в дыхательную систему, где начинают стремительное размножение, отравляя вредоносными веществами.
Стрептококки могут существовать в любых органах, но наиболее благоприятные условия для них имеются на поверхности кожи, слизистых оболочках. Инфекция передается стандартными путями: контактно, воздушно-капельным способом и в процессе полового акта. Чтобы диагностировать заболевание, нужно сдать мазок на анализ.
Практически все люди во взрослом возрасте являются носителями стрептококка. В допустимых пределах бактерии являются составляющей обычной микрофлоры влагалища. Поэтому если мазок показал незначительное содержание кокков – 3-5%, то это не представляет опасности для здоровья и не требует специального лечения.
Микрофлора женского влагалища состоит более чем из 100 видов разнообразных бактерий и микроорганизмов. Присутствие полезных и патогенных клеток обусловливается тем, что подобным образом организм пытается выработать иммунитет.
Присутствие полезных и патогенных клеток обусловливается тем, что подобным образом организм пытается выработать иммунитет.Благодаря иммунной системе полезные микроорганизмы контролируют патогенную флору, понижая численность вредных микроорганизмов. Механизм защиты женского влагалища и внутренних половых органов работает самостоятельно. Для поддержания его функционирования не нужно принимать дополнительные препараты, пользоваться свечами и т.д. Залог здоровой микрофлоры – это ведение здорового образа жизни и соблюдение правил гигиены.
Норма стрептококков в женском влагалище
В профилактических целях каждая женщина должна раз в полгода сдавать анализ на микрофлору. Результат покажет, из чего состоит слизистая и выделения.Если в мазке обнаружили стрептококки, не стоит сразу паниковать. Дело в том, что в норме у каждой женщины во влагалище присутствуют стрептококки, стафилококки, энтерококки и т.д. Это не считается патологией при условии, что 95% содержимого мазка – это палочки Додерлейна (полезные лактобактерии), а только 5% — условно-патогенная микрофлора (стрептококки, грибки рода Кандида и т. д.).
д.).
Причины резкого увеличения количества стрептококков в мазке
Бывает и так, что мазке обнаруживает чрезмерное количество стрептококков, которое говорит о наличии воспалительного процесса. Это может происходить по разным причинам. Наиболее частыми предпосылками к росту стрептококков являются следующие факторы:
- наличие болезней, передающихся половым путем;
- снижение иммунитета вследствие дополнительных заболеваний;
- постоянные стрессы;
- депрессивные состояния;
- нарушенный режим сна;
- несбалансированный рацион питания;
- чрезмерная усталость и т.д.
Точную причину данной проблемы может выяснить только врач. Однако женщина, в мазке которой оказалось чрезмерное количество патогенной флоры, должна нормализовать свой образ жизни и следить за своей половой жизнью.
Симптомы, после которых нужно обращаться к гинекологу
Половые заболевания имеют схожие проявления. Однако женщина сразу понимает, что это не является нормой. Если наблюдается зуд, жжение или странные выделения из половых органов, это может говорить о том, что уровень стрептококков повысился. Понять это наверняка нельзя, потому что для уточнения диагноза нужно сдать анализ. Результаты будут даны лабораторией, и только после этого можно утверждать, какая именно патология присутствует в женском организме.
Однако женщина сразу понимает, что это не является нормой. Если наблюдается зуд, жжение или странные выделения из половых органов, это может говорить о том, что уровень стрептококков повысился. Понять это наверняка нельзя, потому что для уточнения диагноза нужно сдать анализ. Результаты будут даны лабораторией, и только после этого можно утверждать, какая именно патология присутствует в женском организме.Также могут отмечаться боли в нижней части живота, обильные месячные или же наоборот долгое отсутствие менструации. На начальном этапе беременности стрептококки могут спровоцировать самопроизвольный выкидыш в форме менструации, о котором женщина даже не догадывается.
В любом случае это не является нормальным физиологическим состоянием, поэтому при обнаружении первых симптомов нужно немедленно идти на прием к гинекологу.
Лечение стрептококковой инфекции
Терапия требуется только в тех случаях, когда стрептококки превышают допустимую норму. Следует также учесть, что речь идет не о лечении от стрептококков, а об избавлении от факторов, которые спровоцировали рост этих бактерий. Чаще всего этими факторами являются заболевания, передающиеся половым путем. Например, хламидиоз, сифилис, гонорея, уреаплазмоз и т.д.
Следует также учесть, что речь идет не о лечении от стрептококков, а об избавлении от факторов, которые спровоцировали рост этих бактерий. Чаще всего этими факторами являются заболевания, передающиеся половым путем. Например, хламидиоз, сифилис, гонорея, уреаплазмоз и т.д.В зависимости от патологии доктор назначает лечение антибиотиками. После антибактериальной терапии в обязательном порядке нужно восстановить нормальную микрофлору. Для этого могут назначаться препараты, которые содержат в своем составе лактобактерии. Они выпускаются в форме вагинальных свечей и таблеток. Также могут назначаться спринцевания, чтобы вымыть патогенную микрофлору из влагалища.
Повышенный уровень бактерий при беременности
Вынашивание ребенка – ответственный период. Любые сбои в организме могут оказаться фатальными для плода. Именно поэтому повышение допустимого уровня стрептококков в мазке на микрофлору при беременности может плохо сказаться на состоянии ребенка. В этой ситуации женщине назначают пройти ряд дополнительных анализов.
В этой ситуации женщине назначают пройти ряд дополнительных анализов.Если выявляется половая инфекция или воспалительный процесс, то проводят щадящую терапию, которая не угрожает жизни будущего малыша. Ребенок защищен от инфекций плацентой, поэтому к кардинальным мерам, например, лечению антибиотиками пенициллиновой группы, можно и не прибегать в период вынашивания плода.
Также может быть такая ситуация, когда повышенные стрептококки являются нормальной реакцией организма на развитие в нем живого существа. Известно, что в период беременности иммунная система дает сбой. Это отражается, прежде всего, на состоянии женских половых органов. В это время развиваются кандидозы, бактериальные вагинозы и т.д. специального лечения такие патологические состояния не требуют. Достаточно того, чтобы женщина следила за рационом питания во время беременности, не подвергалась психологическим и эмоциональным стрессам.
После рождения малыша все показатели постепенно приходят в норму. Однако нужно постоянно находиться под присмотром гинеколога, который вел женщину в период беременности. Врач может назначить препараты, которые помогают восстановить нормальную микрофлору после рождения ребенка. В течение нескольких недель после родов уровень стрептококков понижается, неприятные симптомы исчезают, и новоиспеченная мама начинает жить привычной здоровой жизнью.
Однако нужно постоянно находиться под присмотром гинеколога, который вел женщину в период беременности. Врач может назначить препараты, которые помогают восстановить нормальную микрофлору после рождения ребенка. В течение нескольких недель после родов уровень стрептококков понижается, неприятные симптомы исчезают, и новоиспеченная мама начинает жить привычной здоровой жизнью.
Streptococcus spp в мазке у женщин норма
О чем говорит присутствие бактерий в гинекологическом мазке?
Если анализы показали присутствия стрептококка во влагалище, особых поводов для беспокойства нет. Но и пренебрегать результатами лабораторного исследования не стоит – стрептококковая инфекция может развиться в любое время. Нужно обратиться гинекологу, чтобы специалист назначил лечение, если в нем есть необходимость.
Во влагалище могут находиться гемолитические стрептококки следующих разновидности:
- группы А (anginosus и др.) – обычно обитают на коже, но могут оказаться и во влагалище, где провоцируют омертвение тканей и токсический шок;
- группы Б – обнаруживаются в основном у беременных, способны проходить через плаценту, инфицировать плод и вызывать выкидыши.

Все гемолитические стрептококки очень опасны для беременных женщин, так как во время родов могут переходить на новорожденных, вызывая серьезные осложнения. Для небеременной женщины они опасны только условно, так как здоровая флора влагалища не дает им массово размножаться и выделять много токсинов.
Если выявить вид бактерий не удалось, в бланке с результатами анализа будет написано streptococcus spp. Это означает, что в лаборатории определили только родовую принадлежность микробов, а более детальные исследования не увенчались успехом или их не проводили, так как в этом не было необходимости.
У здоровой женщины в мазке обычно обнаруживается немного стрептококков следующих разновидностей:
Стрептококковая инфекция влагалища вызывает те же болезни, что и золотистый стафилококк, но развивается более медленно.
Симптомы гинекологической стрептококковой инфекции:
- зуд и боль в гениталиях, желто-кровянистая слизь;
- боли в почечной области и животе;
- нерегулярный менструальный цикл.

По симптомам стрептококковая инфекция влагалища похожа на гонорею. Чтобы точно определить болезнь, врач должен провести дифференциальное обследование.
Причины инфекции
В силу различных причин даже вполне безобидная флора может развиться в тяжелые инфекции. Основные из них:
- нерациональный прием антибиотиков, из-за чего нарушается нормальная флора влагалища;
- изменения гормонального фона, которые происходят из-за беременности, грудного кормления, приема гормонсодержащих препаратов;
- ослабление иммунитета из-за неправильного образа жизни, стрессов инфекционных заболеваний;
- неправильный уход за влагалищем, в том числе частое спринцевание дезинфицирующими растворами, приводящее к гибели полезных лактобацилл;
- частая смена интимных партнеров без использования барьерных средств защиты.
В отличие от гонореи, вагинальная инфекция, вызванная стрептококком, лечится быстро, не оставляя осложнений. Чтобы полностью выздороветь, нужно выполнять все рекомендации врача.
Чтобы полностью выздороветь, нужно выполнять все рекомендации врача.
Доктор назначит антибиотик или другой антибактериальный препарат, который нужно обязательно пропить рекомендованным курсом. Если же надолго отложить визит к специалисту, инфекция может привести к серьезным осложнениям.
При беременности
Кокки группы Б – самая распространенная причина инфекций у беременных женщин и новорожденных малышей. Они обнаруживаются в микрофлоре влагалища почти 25% будущих мам.
Мазок на стрептококк B (агалактию) – обязательный перед родами анализ. Чем больше стрептококков находится во влагалище, тем больше вероятность заражения ребенка, когда он будет продвигаться по родовым путям.
Агалактия проявляется у беременных на 32-33 неделе вынашивания. Особенно велика вероятность обнаружения стрептококков у беременных младше 20 лет.
Микроорганизмы внутри нас: чем опасны стрептококки?
Это довольно распространенные микроорганизмы. Их относят к условно-патогенным, то есть свою вредную деятельность они развивают при определенных условиях, например, при снижении иммунитета. Они обитают в организме человека и селятся в разных органах на слизистых оболочках: во рту, в носу, горле, пищеварительной системе и половых органах.
Они обитают в организме человека и селятся в разных органах на слизистых оболочках: во рту, в носу, горле, пищеварительной системе и половых органах.
Если анализ показал присутствие стрептококка, то сильно расстраиваться не стоит. Сегодня производится много лекарств, которые способны его победить. Но и пренебречь такой проблемой – значит, навредить здоровью. Если не вылечить стрептококковую инфекцию, то она может спровоцировать развитие многих опасных болезней.
В зависимости от того, где и какой тип стрептококков выявлен, лечением будет заниматься гинеколог, отоларинголог, уролог или другой специалист.
- стрептококк А. Вызывает гнойный воспалительный процесс в любой ранке на коже. При попадании внутрь организма провоцирует некроз тканей либо токсический шок.
- В. Обнаруживается при беременности (этому способствуют гормональные изменения). Этот стрептококк способен проникать сквозь плаценту, что может закончиться инфицированием плода или выкидышем.
- гемолитический.
 Селится в половых органах и кишечнике. Особенно опасен для беременных, потому что в процессе родов способен заразить малыша.
Селится в половых органах и кишечнике. Особенно опасен для беременных, потому что в процессе родов способен заразить малыша.
Варианты заражения
Патологические симптомы возникают только в случае благоприятной среды для этого. Инфекция передается несколькими способами:
Повод для беспокойства – инфицирование дыхательных путей, такое случается при скарлатине или ангине.
Стрептококки сохраняют способность к жизнедеятельности порядка трех месяцев в порошковых биологических веществах. Симптомы заражения могут возникнуть во время контакта с инфекционным носителем или человеком с уже проявленными признаками болезни. При повышении температуры до 60 и более градусов вирус гибнет. Уничтожается бактерия также под влиянием химических веществ: моющих средств, шампуня и прочего. Причины размножения стрептококка следующие:
Причины размножения стрептококка следующие:
- сбои гормонального баланса;
- ослабление иммунных сил;
- заражение другими вирусами;
- хронические болезни, подрывающие защиту организма от инфекций;
- повышенная чувствительность к бактериям.
Вызывает распространение стрептококков также прием антибактериальных средств. Такое лечение негативно отражается на состоянии микрофлоры и провоцирует состояние, при котором отмечается преобладание кокков над другими бактериями.
Симптоматика
Стрептококковая инфекция в гинекологии может проявляться различными признаками, все определяется тем, какие заболевания развились вследствие активности бактерии. Но есть и характерные симптомы:
- болезненные ощущения и зуд промежности;
- выделения желтоватого цвета с кровянистыми примесями;
- острые или тянущие боли в нижней части живота, пояснице;
- сбои месячного цикла.

Вагинальная инфекция быстро лечиться при своевременном вмешательстве специалиста, не оставляя значительных последствий. Но если откладывать гинекологический осмотр, то бактерия вызывает серьезные осложнения.
Стоит отметить, что симптомы инфицирования стрептококком сильно напоминают проявление гонореи и потому их часто путают. Чтобы предельно достоверно определить причину патологического состояния и установить, что норма, а что отклонение, врач принимает решение о целесообразности проведения дифференциального обследования.
Стрептококки у беременных
Условно-патогенная бактерия может находиться в пищеварительной системе, симптомы не развиваются. Почти у 40% представительниц женского пола, вынашивающих ребенка, имеется стрептококк агалактия. Этот подтип инфекции можно обнаружить исключительно у беременных на 32-33 неделе срока. Бактерия сильно влияет на женский организм, может спровоцировать ранние роды или даже смерть плода.
Этот подтип инфекции можно обнаружить исключительно у беременных на 32-33 неделе срока. Бактерия сильно влияет на женский организм, может спровоцировать ранние роды или даже смерть плода.
Стоит обратить внимание: стрептококковая инфекция вызывает те же заболевания, что и золотистый стафилококк. Отличие заключается только в клинической картине болезни и в скорости развития патологии.
Есть факторы, повышающие вероятность распространения инфекции:
- выявление стрептококков подтипа В в моче;
- молодой возраст беременной, менее 20;
- угроза преждевременного начала процесса рождения;
- заражение инфекцией предыдущих детей.
Стрептококк подтипа агалактия преимущественно вызывает воспалительные и инфекционные процессы в мочеполовой системе, но случается и развитие таких заболеваний, как эндометрит, эндокардит, пневмония. Вынашивание ребенка сильно подрывает женский организм, в этот период иммунитет сильно ослаблен, поэтому вероятность распространения инфекции существенно повышается. Чтобы предупредить проблему, гинекология рекомендует внимательно относиться к состоянию своего здоровья и выполнять все правила относительно личной гигиены.
Чтобы предупредить проблему, гинекология рекомендует внимательно относиться к состоянию своего здоровья и выполнять все правила относительно личной гигиены.
Лечение и профилактика поражения, вызванного enterococcus faecalis
Процесс назначения лечения обычно начинается с диагностики и подтверждения диагноза. Для постановки диагноза необходимо проведение ряда исследований, так как большинство симптомов, сопровождающих поражение слизистых фекальным энтерококком, являются общими для многих видов инфекционных заболеваний мочеполовой системы у мужчин. К необходимым анализам относится:
- бактериальный посев на микрофлору с забором из уретры;
- бактериальный посев на микрофлору с забором из секрета простаты;
- бактериурия свежевыпущенной мочи.
После подтверждения диагноза требуется серьезное и довольно длительное лечение. Лечение фекальной энтерококковой инфекции осложнено тем, что эти микроорганизмы чрезвычайно жизнестойки, поэтому после постановки такого диагноза стоит обратиться к высококвалифицированному врачу, способному подобрать наиболее оптимальную медикаментозную составляющую, так как в противном случае невылеченная инфекция перейдет в хроническую форму и будет проявляться каждый раз, когда иммунная система будет ослаблена. Можно выделить 3 аспекта лечения воспалительного процесса, вызванного фекальной энтерококковой инфекцией:
- Антибактериальная терапия.
 Так как энтерококк фекалис невосприимчив к антибиотикам тетрациклиновой группы, назначается длительный срок применения препаратов-бактериофагов. Препараты подбираются на основе данных о штамме бактерий и их восприимчивости к тем или иным средствам.
Так как энтерококк фекалис невосприимчив к антибиотикам тетрациклиновой группы, назначается длительный срок применения препаратов-бактериофагов. Препараты подбираются на основе данных о штамме бактерий и их восприимчивости к тем или иным средствам. - Использование препаратов местного назначения. К средствам местного воздействия относятся гели, мази, свечи, которые способствуют нормализации микрофлоры и скорейшему заживлению поврежденных тканей слизистой органов половой системы. Кроме того, для стимуляции кровотока в простате и других органах мочеполовой системы у мужчин может быть назначен курс массажа простаты. Эти средства позволяют существенно снизить риск развития осложнений, а также увеличить площадь поражения слизистой оболочки.
- Меры, направленные на стимуляцию иммунной системы. При диагностировании воспалительного процесса, вызванного энтерококком фекалис, необходим прием витаминно-минеральных комплексов, способствующих улучшению общего состояния организма и иммунной системы.

Благотворно влияет на скорость лечения правильное питание, лечебная физкультура и другие средства, способствующие укреплению иммунитета.
Поделитесь ей с друзьями и они обязательно поделятся чем-то интересным и полезным с Вами! Это очень легко и быстро, просто нажмите кнопку сервиса, которым чаще всего пользуетесь:
youtube.com/embed/NY6EWMEI-xU?feature=oembed» frameborder=»0″ allow=»accelerometer; autoplay; encrypted-media; gyroscope; picture-in-picture» allowfullscreen=»»/>Лечебные мероприятия
Антибактериальная терапия инфекционной болезни – это норма, так как стрептококки устойчивы и сложно поддаются лечению. Препарат побирается после проведенного анализа, которым определяется реакция бактерии на те или иные средства. Лечение могут назначать разные специалисты: педиатр, терапевт, гинеколог, хирург и другие врачи. Все зависит от формы проявления инфекции.
Препарат побирается после проведенного анализа, которым определяется реакция бактерии на те или иные средства. Лечение могут назначать разные специалисты: педиатр, терапевт, гинеколог, хирург и другие врачи. Все зависит от формы проявления инфекции.
При обнаружении первичных форм стрептококка чаще всего назначается прием антибактериальных средств пенициллинового ряда. Если пятидневный курс не привел к выздоровлению, то это признак подбора неправильного препарата, тогда антибиотик отменяют. Используют Эритромицин, Сумамед, Азитромицин, Цифран и так далее. Препараты тетрациклинового ряда не являются эффективными при лечении стрептококка.
Дополнительно применяются методы лечения, направленные на устранение симптомов, которые зависят от клинического проявления болезни.
При вторичном распространении инфекции проведение длительных курсов приема антибактериальных препаратов – это норма. Здесь применяют средства с пролонгированным действием. По необходимости дополняют терапию иммуномодулирующими средствами.
youtube.com/embed/QZ6zHlMOKN8?feature=oembed» frameborder=»0″ allow=»accelerometer; autoplay; encrypted-media; gyroscope; picture-in-picture» allowfullscreen=»»/>
Какое требуется лечение?
Самостоятельно или под наблюдением врача?
Лечение назначает гинеколог, сопоставляя результаты мазка с наличием жалоб и данными, полученными в ходе осмотра. При наличии клинической картины воспаления назначаются антибиотики.
Мнение эксперта
Ковалева Елена Анатольевна
Врач-Лаборант. Опыт работы в клинико-диагностической службе 14 лет.
Задать вопрос эксперту
Антибактериальный препарат подбирается строго исходя из результатов определения чувствительности микроорганизма к антибиотикам.
Еnterococcus faecalis обладает природной устойчивостью к некоторым классам антибиотиков, например, к цефалоспоринам, эритромицину и др. Кроме того он может стать нечувствительным к ряду препаратов и вследствие ранее проводимого противомикробного лечения.
Местное или системное лечение антибиотиками?
В настоящее время существует множество вагинальных суппозиториев (свечей), обладающих противомикробной активностью. Но при введении во влагалище входящие в их состав активные вещества, если и проникают в цервикальный канал, то только в очень небольших количествах. Основной же их антимикробный эффект распространяется на стенки влагалища.
Но при введении во влагалище входящие в их состав активные вещества, если и проникают в цервикальный канал, то только в очень небольших количествах. Основной же их антимикробный эффект распространяется на стенки влагалища.
Поэтому в данном случае назначают системную терапию антибиотиками. Они принимаются внутрь или вводятся в организм в виде инъекций. При этом действующее вещество попадает в ток крови, и с ней разносится ко всем органам и тканям.
Местные антибактериальные препараты могут применяться только в качестве вспомогательного средства для усиления эффекта и при сопутствующем кольпите.
Особенности стрептококковой инфекции в гинекологии
Инфицирование стрептококком может произойти где угодно, бактерия присутствует везде и чаще всего поражает слизистые, ткани. Заражение может случиться в медицинском заведении, роддоме, общественном месте. Стрептококки проникают в организм при повреждении покровов.
Если имеется воспалительный процесс в органах, например, малого таза, то инфицирование может произойти при незащищенном половом акте. Патологические проблемы ослабляют женский организм, что повышает вероятность распространения инфекции.
Патологические проблемы ослабляют женский организм, что повышает вероятность распространения инфекции.
Какие болезни могут развиться
Наличие бактерий в моче называют бактериурией. Заболевания, к которым она приводит, в течение длительного времени могут развиваться без каких-либо явных симптомов. Очень часто энтерококк фекальный обнаруживается у больного случайно, когда возникает необходимость сдать мочу или мазок на анализ. Однако дальнейшее развитие инфекции может привести к более серьезным последствиям.
В первую очередь энтерококки могут привести к болезням мочеполовой сферы, таким как цистит, пиелонефрит, аднексит. Их чрезмерное размножение может вызвать и воспалительные процессы во внутренней оболочке сердца – эндокардит. У женщин могут также развиться различные заболевания органов малого таза.
Особое внимание на возможные негативные последствия бактериурии следует обращать беременным женщинам. В этот период у них часто случается застой мочи, что приводит к созданию благотворных условий для более интенсивного размножения бактерий
Способствуют этому и изменения в гормональном фоне.
Поэтому, если в анализах обнаружен энтерококк, следует отнестись к этому с максимальной серьезностью.
Чего следует опасаться мужчинам
Несмотря на то, что от энтерококковых инфекций больше страдают женщины, относить их к сугубо женским проблемам нельзя. У мужчин также могут возникнуть ситуации, когда в моче будут найдены эти бактерии. Как правило, это происходит в случаях длительного приема антибиотиков, недостаточного внимания к личной гигиене или как осложнение на фоне вирусной инфекции.
Точно так же, как и у женщин, наличие инфекции у мужчин приводит к заболеваниям мочеполовой сферы. Однако, в силу анатомических особенностей, мужчины более подвержены заболеваниям нижних мочевых путей. У них может воспалиться мочевой пузырь, мочеточники, или предстательная железа. В самых тяжелых случаях может развиться простатит. Поэтому пренебрегать опасностью при обнаружении энтерококка в моче ни в коем случае нельзя.
Норма стрептококков в женском влагалище
В профилактических целях каждая женщина должна раз в полгода сдавать анализ на микрофлору. Результат покажет, из чего состоит слизистая и выделения.
Результат покажет, из чего состоит слизистая и выделения.
Если в мазке обнаружили стрептококки, не стоит сразу паниковать. Дело в том, что в норме у каждой женщины во влагалище присутствуют стрептококки, стафилококки, энтерококки и т.д. Это не считается патологией при условии, что 95% содержимого мазка – это палочки Додерлейна (полезные лактобактерии), а только 5% — условно-патогенная микрофлора (стрептококки, грибки рода Кандида и т.д.).
Виды [ править | править код ]
[ источник не указан 772 дня
] Включаемые ранее в род пептострептококки виды
P. asaccharolyticus, P. magnus, P. micros, P. prevotii, P. vaginalis
согласно современным представлениям переименованы и перенесены в другие роды:
Peptoniphilius asaccharolyticus, Finegoldia magnus, Micromonas micros, Anaerococcus prevotii, Anaerococcus vaginalis
соответственно.
Стрептококк в мазке у женщин выявляется с помощью лабораторных исследований. Когда такой результат является нормой, а что считать патологией?
Чтобы безошибочно разобраться в цифрах на бланке, нужно знать, что такое гинекологическая стрептококковая инфекция и чем она опасна.
Причины резкого увеличения количества стрептококков в мазке
Бывает и так, что мазке обнаруживает чрезмерное количество стрептококков, которое говорит о наличии воспалительного процесса. Это может происходить по разным причинам. Наиболее частыми предпосылками к росту стрептококков являются следующие факторы:
- наличие болезней, передающихся половым путем;
- снижение иммунитета вследствие дополнительных заболеваний;
- постоянные стрессы;
- депрессивные состояния;
- нарушенный режим сна;
- несбалансированный рацион питания;
- чрезмерная усталость и т.д.
Симптомы, после которых нужно обращаться к гинекологу
Половые заболевания имеют схожие проявления. Однако женщина сразу понимает, что это не является нормой. Если наблюдается зуд, жжение или странные выделения из половых органов, это может говорить о том, что уровень стрептококков повысился. Понять это наверняка нельзя, потому что для уточнения диагноза нужно сдать анализ. Результаты будут даны лабораторией, и только после этого можно утверждать, какая именно патология присутствует в женском организме.
Также могут отмечаться боли в нижней части живота, обильные месячные или же наоборот долгое отсутствие менструации. На начальном этапе беременности стрептококки могут спровоцировать самопроизвольный выкидыш в форме менструации, о котором женщина даже не догадывается.
В любом случае это не является нормальным физиологическим состоянием, поэтому при обнаружении первых симптомов нужно немедленно идти на прием к гинекологу.
Причины обнаружения
Микроорганизмы энтерококка всегда в наличии в организме человека в некотором количестве. Если их концентрация невелика, они приносят пользу, но при превышении допустимых показателей могут вызвать серьезные болезни. Чаще всего от подобных проблем страдают женщины, но появиться он может и у мужчин.
Кроме того, во время ожидания ребёнка женский организм страдает от многих изменений, в том числе и от повышенной концентрации бактерий энтерококка фекального типа в моче.
https://youtube.com/watch?v=P0stz7Laacs
Именно по этой причине беременные часто жалуются на уретриты и циститы, хотя внешних симптомов этих болезней нет. Enterococcus faecalis в моче у ребенка указывает на инфицирование мочевыводящей системы.
Наиболее подвержены риску заражения энтерококками те пациентки, которые принимали сильные антибактериальные препараты или подвергались инструментальному обследованию в условиях стационара, где, по статистике, чаще всего и происходит заражение.
Причины, по которым фекальный энтерококк может попасть в женские половые органы, немногочисленны.
Самый распространенный фактор, провоцирующий развитие энтерококковой инфекции — несоблюдение правил личной гигиены. а именно:
- нерегулярное мытье наружных половых органов;
- использование чужих полотенец, белья, бритв;
- несвоевременная замена гигиенических прокладок и тампонов.
Передается бактерия и половым путем, через не защищенные контакты. поэтому женщины, не использующие барьерные средства контрацепции и не имеющие постоянного партнера, могут заразиться от мужчины.
Зачастую микроорганизм начинает активироваться в организме тех женщин, которые перенесли курсы антибиотикотерапии — в ослабленном организме энтерококк развивается гораздо активнее, чем у совершенно здорового человека с сильной иммунной системой.
Лечение стрептококковой инфекции
Терапия требуется только в тех случаях, когда стрептококки превышают допустимую норму. Следует также учесть, что речь идет не о лечении от стрептококков, а об избавлении от факторов, которые спровоцировали рост этих бактерий. Чаще всего этими факторами являются заболевания, передающиеся половым путем. Например, хламидиоз, сифилис, гонорея, уреаплазмоз и т.д.
В зависимости от патологии доктор назначает лечение антибиотиками. После антибактериальной терапии в обязательном порядке нужно восстановить нормальную микрофлору. Для этого могут назначаться препараты, которые содержат в своем составе лактобактерии. Они выпускаются в форме вагинальных свечей и таблеток. Также могут назначаться спринцевания, чтобы вымыть патогенную микрофлору из влагалища.
Повышенный уровень бактерий при беременности
Вынашивание ребенка – ответственный период. Любые сбои в организме могут оказаться фатальными для плода. Именно поэтому повышение допустимого уровня стрептококков в мазке на микрофлору при беременности может плохо сказаться на состоянии ребенка. В этой ситуации женщине назначают пройти ряд дополнительных анализов.
Если выявляется половая инфекция или воспалительный процесс, то проводят щадящую терапию, которая не угрожает жизни будущего малыша. Ребенок защищен от инфекций плацентой, поэтому к кардинальным мерам, например, лечению антибиотиками пенициллиновой группы, можно и не прибегать в период вынашивания плода.
Также может быть такая ситуация, когда повышенные стрептококки являются нормальной реакцией организма на развитие в нем живого существа. Известно, что в период беременности иммунная система дает сбой. Это отражается, прежде всего, на состоянии женских половых органов. В это время развиваются кандидозы, бактериальные вагинозы и т.д. специального лечения такие патологические состояния не требуют. Достаточно того, чтобы женщина следила за рационом питания во время беременности, не подвергалась психологическим и эмоциональным стрессам.
После рождения малыша все показатели постепенно приходят в норму. Однако нужно постоянно находиться под присмотром гинеколога, который вел женщину в период беременности. Врач может назначить препараты, которые помогают восстановить нормальную микрофлору после рождения ребенка. В течение нескольких недель после родов уровень стрептококков понижается, неприятные симптомы исчезают, и новоиспеченная мама начинает жить привычной здоровой жизнью.
Энтерококк фекалис | Страница 3
331 ответ
Последний — 25 июля, 00:16 Перейти
Автор
У кого он был обнаружен в посеве мочи и влагалище – напишите, пожалуйста, смогли ли вы от него избавиться и как. Очень прошу! Восстановилось ли у вас нормальное мочеиспускание?Много где пишут, что полностью удалить его из мочевых путей если он туда попал уже не получится, но может есть те кто с ним всё-таки справились и теперь живут здоровой жизнью?
Буду всем благодарна за ответы.
Гость
Энтерококк может убить только линезолид – это современный препарат и очень эффективный, поможет когда он в моче и есть видимое воспаление
Гость
Кто будет так лечиться, отпишитесь о результатах, плиз
Нэн
От энтерококка помогают бактериофаги. Проверена на собственном опыте. Больше года пила от него разные чувствительные к нему антибиотики и все без толку. Помог бактериофаг интести и секстафаг. Сприциваться ими и пить. Поможет обязательно! Только курс длительный, желательно две-три недели.
Гость
А вы знаете кого-то, кто вылечился линезолидом?
autor
Cine a fost găsit la însămânțarea urinei și a vaginului – scrieți, vă rog, dacă ați putea scăpa de ea și cum. Foarte mult vă întreb! Mulți oameni scriu că o elimină complet din tractul urinar, dacă nu a mai ajuns acolo, dar poate că sunt cei care au reușit încă cu ea și trăiesc acum o viață sănătoasă? Voi fi recunoscător tuturor pentru răspunsuri.
Гость
Это не правда, что причина в ЖКТ, не пишите, если не знаете и не сталкивались с этим. Каким образом гастроэнтеролог будет лечить энтероккок в органах малого таза? Обычно, заражение половым путем, и этот патоген передается половым путем и вызывает дальше воспаление в яичниках.
Анна
Вроде как фурамаг действует на него. Кто-нибудь пробовал?
гость я
Я девственница, много мастурбирую, vожет быть, от этого? Других инфекций нет. Есть дисбиоз. Но когда принимаю бифидо и лактобактерии, чешется еще сильнее
Лола Шнайдер
Я тоже девственница, но мастурбировать прекратила летом, уже полгода воздерживаюсь, что и тебе рекомендую. Натирание повреждает слизистую и распространяет бактерию. Какие бактериофаги ты пробовала и каким способом (пила или вводила во влагалище)? Секстафаг или другой?
Лола Шнайдер
И да, линезолид пьется легко. Ни одной побочки – ни тошноты, ни вздутия, ни диареи, ни головной боли, ни запаха дисбактериоза изо рта, как после амоксиклава (утренний запах наоборот исчез, у меня пробки в гландах).
Единственное предупреждение в инструкции – возрастает риск нейропатий глазного нерва, лицевого, конечностей и т.д. Поэтому лучше пить с витаминами группы В. Я пила Нейрорубин по 1 таблетке в день вместе с линезолидом.
Правда, была бессонница.
Анна
Вроде как фурамаг действует на него. Кто-нибудь пробовал?
Гость
мне фурамаг не помог я его курсами пила
гость.
А у меня в бак. Посеве написано, что линезолид устойчив к энтерококку в моем случае
Лола Шнайдер
Я тоже девственница, но мастурбировать прекратила летом, уже полгода воздерживаюсь, что и тебе рекомендую. Натирание повреждает слизистую и распространяет бактерию. Какие бактериофаги ты пробовала и каким способом (пила или вводила во влагалище)? Секстафаг или другой?
гость
Как получилось воздерживаться? у меня это жжение от энтерококка вызывает желание мастурбировать
Лола Шнайдер
гость.
Беспокоит ли жжение ежедневно? При энтерококке 105?
Гость
Не поверите, но я девственница, и у меня во влагалище и уретре энтерококк фекалис.
Гость
Вы могли занести его, неправильно вытираясь после туалета- сзади наперед , а не спереди назад, он мог попасть в уретру, а потом в мочевой пузырь.
Гость
Жжение может быть от молочницы, которая обостряется после антибиотиков и после большого количества сладкого, сдайте посев на вид кандиды и чувствительность к препаратам
Гость
Ну если, например, у ее партнера простатит, вызванный энтерококком, и он проходил не один курс линезолида, и выработалась устойчивость к нему, и он заразил ее этим штаммом, то такое может быть.
Лола Шнайдер
Резюмирую по линезолиду (пришел бакпосев). Сказать, что я в шоке, это ничего не сказать. Энтерококк фекалис – 10*7, клебсиелла пневмониа – 10*6. То есть энтерококка стало больше, а клебсиеллы вообще до этого не было… Но что самое интересное, жжение не так выражено, как до приема линезолида.
Загадка… Но то, что я не буду больше жpать антибиотики, это точно. Планирую с завтрашнего дня пить растительные препараты на клюкве и гибискусе, а также буду поглядывать в сторону бактериофагов (Секстафаг, он и от клебсиеллы), и на питьевую вакцину в капсулах Уривак. Всем желаю выздоровления.
Streptococcus agalactiae и spp в мазке у женщин: норма содержания, причины, лечение
Выявление Streptococcus spp. в мазке у женщин не всегда свидетельствует о явном или скрытом течении инфекционно-воспалительного заболевания. Только при превышении значений нормы врачи подозревают развитие патологических процессов. Для обнаружения стрептококков выполняется забор слизистых выделений при гинекологическом осмотре. Затем мазок направляется на бактериологическое исследование, которое определяет наличие или отсутствие этих представителей условно-патогенной микрофлоры. При необходимости проводится лечение, но иногда микробиоценоз влагалища восстанавливается самостоятельно.
Почему в мазке появляется стрептококк
Стрептококки — представители условно-патогенного микробиоценоза. Это означает, что в небольшом количестве они всегда присутствуют в организме, практически ничем себя не проявляя. Поэтому их обнаружение в мазке из влагалища или зева не становится чем-то из ряда вон выдающимся.
Но подобное «соседство» перестает быть мирным при ослаблении иммунной защиты. Нормальное соотношение микроорганизмов нарушается:
- активизируются условно-патогенные микроорганизмы, в том числе стрептококки, начинают усиленно размножаться;
- гибнут полезные лакто- и бифидобактерии, еще более ослабляя иммунитет.
Колонизация стрептококками слизистых оболочек становится причиной развития инфекционно-воспалительного процесса. Обычно организм с ним не справляется, так что не обходится без антибиотикотерапии.
Стрептококки могут проникать в верхние дыхательные пути извне. Воздушно-капельный путь передачи традиционен для этих патогенов, особенно в прохладное время года. Заболеет женщина или нет, зависит только от функциональной активности иммунной системы. А также исходного состояния микрофлоры. Если оно оптимально, то стрептококки погибают, не успев достигнуть органов-мишеней и спровоцировать воспаление. Но стоит учесть, что именно такие бактерии наиболее опасны из-за многочисленных мутаций во внешней среде. Они устойчивы к большинству известных антисептиков и антибактериальных препаратов.
Важно:
Обнаружение стрептококков в уретральном мазке чаще всего указывает на гнойно-воспалительное или инфекционное заболевание, поразившее мочеполовую систему. Их численность всегда увеличивается при цистите, пиелонефрите, уретрите и других патологиях.
Виды микробов
Одного выявления стрептококка в мазке из горла, влагалища или мочеиспускательного канала недостаточно. Существует много видов этих бактерий, и принадлежность к одному из них часто становится определяющим критерием при составлении терапевтических схем. Некоторые стрептококки относительно безвредны, проявляют свою патогенность исключительно редко. А другие могут спровоцировать развитие заболеваний, которые пока еще не поддаются окончательному излечению.
В мазках преимущественно обнаруживаются такие условно-патогенные и патогенные микроорганизмы:
- гемолитические альфа-стрептококки, в том числе pneumoniae, thermophilus, mitis провоцируют частичное патологическое разрушение эритроцитов крови с выделением в окружающую среду гемоглобина;
- гемолитические бета-стрептококки, включая разновидности pyogenes, agalactiae, anginosus, вызывают полную гибель красных кровяных телец;
- гамма-стрептококки наименее патогенны, не оказывают влияния на жизненный цикл эритроцитов.
После обнаружения микробов в мазке устанавливается их видовая принадлежность и опасность для человека
Также в отдельную группу медики выделяют фекальные стрептококки, повышение численности которых может стать причиной сепсиса. Их выявление в любом мазке требует незамедлительного лечения.
Пути проникновения в организм
Нередко стрептококки передаются от человека к человеку фекально-оральным путем. Часть из них атакует слизистые оболочки, а другие выводятся из организма вместе с каловыми массами. Если заболевший не моет руки после посещения туалета, то с большой долей вероятности симптомы стрептококковой инфекции вскоре возникнут у окружающих его людей — членов семьи, коллег, попутчиков в общественном транспорте.
Какие еще существуют пути передачи:
- попадание слюны бактерионосителя на лицо при кашле или чихании. Именно из-за воздушно-капельной передачи случаются целые эпидемии в замкнутых коллективах — детских садах, офисах;
- незащищенный половой акт;
- контакт с предметом, к которому ранее прикасался зараженный человек.
Инфицирование взрослых женщин происходит во время ухода за больным ребенком. Вероятность такого развития событий возрастает при отказе от врачебной помощи, попытке самостоятельно справиться с инфекцией. Отмечены случаи внедрения патогенов в организм пациенток и в медицинских учреждениях вследствие некачественной обработки инструментов, перевязочного материала.
Провоцирующие факторы
Существует ряд факторов, вызывающих активизацию стрептококков, обитающих на слизистых респираторных путей или органов мочевыделительной системы. Они способствуют и более легкому проникновению патогенов из внешней среды.
Основные причины развития инфекционно-воспалительных процессов следующие:
- прием антибиотиков без назначения врача, проведения предварительных исследований, что приводит к дисбалансу микрофлоры влагалища;
- расстройства гормонального фона во время вынашивания беременности, грудного вскармливания;
- ослабление иммунной защиты в результате малоподвижного образа жизни, стрессов;
- несоблюдение правил интимной гигиены, в том числе частые спринцевания антисептиками, что приводит к гибели полезных лактобактерий;
- частая смена интимных партнеров без использования барьерных контрацептивов.
К предрасполагающим факторам относятся пожилой возраст, избыточный вес, недавние хирургические вмешательства, переохлаждение. В группу риска входят женщины в период менопаузы и проживающие в неблагоприятной экологической обстановке. Облегчает проникновение стрептококков в организм дефицит в рационе продуктов с витаминами и микро- и макроэлементами.
Болезнетворные бактерии в мазке
Мочеполовые патологи, причиной которых становится стрептококковая инфекция, можно было бы предотвратить при своевременной сдаче мазка. Инфекционные возбудители обнаруживаются независимо от того, каким путем они проникли в организм, — экзогенным или эндогенным. В последнем случае они обычно внедряются в слизистые из первичных воспалительных очагов, например, из респираторных путей, кишечника. Врачи назначают исследование не только вагинального соскоба, но и мазка из зева для оценки степени обсеменения органов патогенами.
Streptococcus agalactiae
Streptococcus agalactiae в мазке не всегда свидетельствует о наличии в мочеполовой системе воспаления. Примерно 30% женщин являются бактерионосителями. Микроорганизмы стали частью естественной вагинальной микрофлоры, не наносят никакого вреда и даже несколько сдерживают рост патогенов. Но забывать о том, что стрептококки агалактия — условно-патогенные микроорганизмы не стоит. При создании благоприятных условий они начинают размножаться, вызывая воспалительный процесс.
Численность Streptococcus agalactiae в мазке не должна превышать 104 КОЕ на миллилитр слизистого секрета. Если бактерий больше, то развилось неспецифическое воспаление.
Патологическое отклонение, требующее лечения, — показатель 105 и больше КОЕ/мл. Пока микроорганизмы размножаются, женщина не страдает от каких-либо выраженных симптомов. Они возникают после высвобождения бактериями в окружающее пространство токсичных продуктов своей жизнедеятельности.
Чаще всего симптомы интоксикации уже сопровождают цистит или уретрит, которые следующим образом:
- острой болью внизу живота;
- частыми позывами в туалет;
- резями и жжением при мочеиспускании;
- ощущением неполноценного опорожнения мочевого пузыря.
Появление большого количества стрептококков в мазке — сигнал о высокой вероятности развития инфекции
При остром течении патологии женщина страдает от головной боли, общей слабости, расстройств сна. Streptococcus agalactiae может стать причиной и бактериального вагиноза, характеризующегося тянущими болями в паху, отечностью и гиперемией половых губ, зудом и жжением промежности.
На спровоцированный патогенами инфекционный процесс указывают желтоватые или коричневатые выделения из влагалища, болезненный дискомфорт при половом контакте, стремление избегать интимных связей.
Streptococcus anginosus
Streptococcus anginosus — представитель естественной микрофлоры влагалища, незначительная часть 5% всех кокков. Оставшиеся 95%— лактобактерии, обеспечивающие местный иммунитет. При уменьшении их популяции увеличивается количество Streptococcus anginosus. Если оно превышает 105 КОЕ/мл, то медики говорят о стрептококковой инфекции. Но не только. Их численность нередко увеличивается в микробных ассоциациях, в том числе вместе с возбудителями заболеваний, передающихся половым путем.
Превышение параметров нормы в любом случае свидетельствует о дисбактериозе влагалища. Это его невоспалительное инфекционное поражение, при котором происходит замещение нормальной флоры на ассоциации анаэробов. Происходит увеличение концентрации аминов и органических кислот, сдвиг pH в щелочную сторону, изменению среды влагалища на щелочную. В комплексе все это приводит к разрушению эпителиальных клеток, повреждению слизистых и более глубоко расположенных тканей.
У беременных
Доказано, что повышенная активность стрептококков негативно воздействует на течение беременности. В клинической практике отмечены вызванные ею самопроизвольные аборты, выкидыши, преждевременные роды. Тяжелейшими осложнениями инфекции становятся гестозы, инфекционные заболевания, повреждения почечных и почечных структур. Любой из этих факторов предрасполагает к невынашиванию беременности. Своевременно обнаруженный в мазке стрептококк и адекватная антибиотикотерапия позволяют не допустить негативных последствий и заражения ребенка во время прохождения по родовым путям.
Важно:
Стрептококковая инфекция угрожает здоровью беременной, но особенно она опасна для плода недоразвитием внутренних органов, физическими дефектами, врожденными уродствами.
У мужчин
В мазке из мочеиспускательного канала, забранного у мужчин, также могут в избыточном количестве обнаруживаться стрептококки. Поражение ими урогенитального канала проявляется преимуществами характерными признаками баланитов или баланопоститов:
- головка полового члена воспаляется, краснеет;
- крайняя плоть отекает, несколько утолщается;
- из уретры выделяет желтоватая слизь;
- на половом члене формируется сыпь.
Плохое самочувствие мужчины еще более усугубляется из-за сильнейшего жжения, выраженного дискомфорта во время опорожнения мочевого пузыря. Если стрептококки внедрились в предстательную железу, то возникают сильные боли в яичках, затрудненное и учащенное мочеиспускание.
Исследование мазка
Перед сдачей мазка необходимо подготовиться. Большинство лабораторий не предъявляет строгих требований к этому этапу, лишь рекомендует за 1-2 недели отказаться от приема антибактериальных средств. Мазок у женщин берет гинеколог, специальной щеточкой собирая слизистый секрет со стенок влагалища, цервикального канала, шейки матки. Затем он распределяет его на промаркированном стекле и направляет для исследования в лабораторию.
Практикуется бактериальный посев очищенного от примеси секрета в питательную среду, предназначенную именно для стрептококков. В таких благоприятных условиях они начинают активно размножаться, формируя на поверхности специфические колонии. По их количеству специалисты лаборатории судят о виде патогена, степени обсеменения бактериями органов мочеполовой системы. Недостатком культурального метода считается долгое ожидание результатов — около недели. Но есть у него и преимущества. Только с помощью бакпосева удается выявить резистентность (устойчивость) стрептококков к тому или иному антибактериальному препарату.
Исследование мазка на наличие стрептококков выполняется с помощью бактериального посева
Еще один часто практикующийся метод исследования мазка — ПРЦ. Секрет очищается с помощью центрифуги, а затем помещается в амплификатор. Так называется прибор, охлаждающий и нагревающий пробирки с биоматериалом. Смена температур необходима для проведения репликации — многократного клонирования ДНК бактерий. ПРЦ отличается высокой точностью, чувствительностью, информативностью. Результат исследования готов в тот же день. Но вот чувствительность бактерий к антибиотикам с его помощью установить не удастся.
Расшифровка выполняется специалистами лаборатории, а трактует результаты мазка лечащий врач. Если показатели находятся в пределах нормы, то проведения лечения не требуется. В ином случае назначается курсовая антибиотикотерапия, в том числе для профилактики распространения патогенов по направлению к почкам.
Таблица основных трактовок данных исследования мазка на стрептококки:
| Результаты мазка на стрептококки | Интерпретация данных |
| 10*1-10*2 КОЕ/мл | Количество микроорганизмов в норме и не может спровоцировать развития инфекционно-воспалительного процесса |
| 10*3-10*4 КОЕ/мл | Количество бактерий в норме, безопасно при отсутствии клинических симптомов |
| 10*6-10*7 КОЕ/мл | Количество микробов высокое и может быть причиной инфекционно-воспалительного процесса |
| Сливной рост | Высокое количество условно-патогенных микроорганизмов, соответствующее острой инфекции и требующее немедленного лечения |
Практические советы
Совет №1
Стрептококковая инфекция опасна во время вынашивания ребенка, поэтому гинекологи рекомендуют сдать мазок на этапе планирования зачатия.
Совет №2
Информативность исследования будет выше, если за сутки до взятия мазка отказаться от физических нагрузок, жирной пищи, алкоголя, а также использования средств интимной гигиены с противомикробными компонентами.
Совет №3
Категорически запрещено лечить стрептококковую инфекцию народными средствами — это неизбежно закончится развитием осложнений.
Ответы на частые вопросы
Нужно ли лечение во время беременности?
Если концентрация стрептококка в мазке не превышает значений нормы и даже выявляется инфекция или воспаление, то врачи проводят щадящее лечение, которое не угрожает здоровью ребенка. Он защищен от инфекционных возбудителей плацентой, поэтому нередко кардинальные меры, например, антибиотикотерапия пенициллинами, не нужны.
Какие препараты используются для лечения?
Стрептококки не выработали резистентности к антибактериальным средствам пенициллинового ряда. Поэтому именно они становятся препаратами первого выбора в лечении инфекции. При их непереносимости или неэффективности пациенткам назначаются Эритромицин, Азитромицин, Кларитромицин.
Скажем женским проблемам — НЕТ!
20.03.2019
Скажем женским проблемам – НЕТ!
В жизни каждой женщины множество вопросов, которые нельзя откладывать на завтра. Мы стремимся все сделать лучшим образом и на себя порой сил и времени остается крайне мало. И если мы его находим, то тратить ценные минуты на неприятности в виде интимных инфекций желание небольшое. Сегодня в нескольких словах мы расскажем о том, как справиться с женскими проблемами без душевных, временных и денежных трат.
Проблема № 1
Более половины женщин, инфицированных ИППП не знают об этом.
Инфекции, передаваемые половым путем (ИППП) — вопрос, скрывающий массу домыслов, мифов и ошибочных представлений. Зачастую человек стесняется получить достоверную информацию и черпает знания из рекламы, советов знакомых или руководствуется собственным «здравым смыслом». Но осведомленность в области ИППП это не только вопрос здоровья, но защита от трат в виде ненужных анализов и лечения.
Правда, как она есть:
-
Грозные инфекции могут протекать бессимптомно. Например, гонорея и хламидиоз.
-
Сильнодействующие препараты широкого профиля могут навредить организму и при этом не решить существующую проблему.
-
Некоторых возбудителей можно выявить исключительно методом ПЦР, например, микоплазму гениталиум (Mycoplasma genitalium).
-
Не существует признаков, по которым можно отличить одну инфекцию от другой на 100% при обычном осмотре.
Самые распространенные ИППП — группа NCMT инфекций:
-
Гонорея (Neisseria gonorrhoeae)
-
Хламидиоз (Chlamydia trachomatis)
-
Микоплазмоз (Mycoplasma genitalium)
-
Трихомониаз (Trichomonas vaginālis)
ПЦР (полимеразная цепная реакция) — самый точный метод диагностики различных инфекций.
Тест NCMT— выявление облигатных патогенов, обнаружение которых требует обязательного лечения!
Проблема № 2
Просто о сложном и наболевшем.
Кандидоз (молочница) недуг, о котором 7 женщин из 10 знают на собственном опыте. Жжение, зуд, проблемы с мочеиспусканием, обильные выделения создают массу беспокойств и только одно желание — избавиться от проблемы быстро и не возвращаться к ней никогда.
Добиться этого получается не у всех.
И причина проста. При диагностике и лечении женщины руководствуются не фактами, а ошибочными представлениями.
Молочницу способна вызвать не только Candida albicans, как думают многие. Но и Candida tropicalis, Candida glabrata, Candida krusei и Candida parapsilosis. Естественно, что анализ выявляющий только Candida albicans может дать отрицательный результат, но не отразить истинной картины. В то же самое время проводить анализ на все грибы Сandida spp нет необходимости, так как они могут быть непатогенными.
Первый простой вывод: необходимо проводить анализ на 5 видов грибов рода Сandida, вызывающих Кандидоз.
Реклама нам говорит, что можно решить вопрос с молочницей приняв одну таблетку. Такой метод работает лишь в 20% случаев. Это связано с тем, что виды грибов Сandida реагируют на лечение разнообразно. Если в случае с Candida albicans эффективны азоловые препараты, то Сandida krusei легко переживает такое лечение.
Candida tropicalis и Candida parapsilosis лечиться одинаково хорошо.
Candida glabrata реагирует на лечение в зависимости от дозы препарата.
Второй простой вывод: разные виды кандид требуют разного лечения.
Выявление грибов Candida не означает необходимость немедленного лечения. Кандидоз развивается лишь тогда, когда грибы бурно размножаются. Чтобы отличить болезнь от ее носительства необходимо оценить количество грибов Candida. Лишь высокая концентрация грибов может быть подозрением на кандидоз. Необходим гинекологический осмотр и микроскопия мазка для подтверждения или опровержения диагноза. Не нужно «лечить анализы». Это трата сил, нервов и денег на уничтожение микроорганизма, который даже не вызывает заболевания.
Третий простой вывод: Информативен лишь количественный ПЦР-тест на значимые виды кандид.
Решение: ПЦР на 5 важных видов кандид — шаг навстречу лучшему решению для лечения молочницы.
Флороценоз – Кандиды самый информативный и современный тест для диагностики кандидоза.
Проблема №3
Микрофлора здоровой женщины — это совокупность микроорганизмов. И лактобактерии тут играют важнейшую роль. Чем меньше полезных лактобактерий, тем больше условно-патогенных микроорганизмов. Если они аэробные, то развивается аэробный вагинит. Если же анаэробные, то бактериальный вагиноз.
Бактериальный вагиноз — это одно из нарушений женской микрофлоры.
Симптомы могут быть знакомым многим представительницам прекрасного пола. Выделения обычно с запахом, напоминающим тухлую рыбу. Но бывает он и без симптомов, и со всеми теми же последствиями. В частности, бактериальный вагиноз увеличивает риск воспалительных заболеваний матки и придатков, осложнений беременности, преждевременных родов. Бактериальный вагиноз увеличивает риск заражения ИППП.
Наиболее значимые микроорганизмы вызывающие бактериальный вагиноз это Gardnerella vaginalis и Atopobium vaginae.
Выявление Gardnerella vaginalis и Atopobium vaginae недостаточно для выявления бактериального вагиноза, так как их часто обнаруживают у здоровых женщин. При этом их количество незначительно по отношению ко всем микроорганизмам влагалища.
Необходимо определить соотношение полезных и условно-патогенных бактерий и выявить микроорганизмы, присутствие которых требует особой терапии. Эти данные дадут возможность доктору поставить точный диагноз и начать эффективное лечение.
Определение общего количества бактерий, лактобактерий, Gardnerella vaginalis и Atopobium vaginae методом количественной ПЦР в реальном времени — современный и точный способ диагностики бактериального вагиноза.
Флороценоз — Бактериальный вагиноз самый информативный и современный тест для диагностики бактериального вагиноза.
Проблема №4
Введенный недавно диагноз аэробный вагинт еще не приобрел широкой известности. Этот недуг может проявляться через зуд, жжение, выделения. Иными словами, иметь те же симптомы, что при кандидозе или бактериальном вагинозе. Разница лишь в том, что лекарства, назначаемые для лечения при этих болезнях, не помогут при аэробном вагините.
Ввиду бесполезности неправильного лечения нераспознанный аэробный вагинит превращается в непроходящий кандидоз или неизлечимый бактериальный вагиноз. Для решения этой проблемы необходимо распознать нарушение баланса вагинальной микрофлоры, сопровождаемое экспансией определенной группы бактерий-аэробов с преобладанием их над «полезными» лактобактериями.
При всем многообразии аэробной микрофлоры врачу для выявления аэробного вагинита достаточно информации о главных возбудителях.
-
Энтеробактерии (Enterobacteriaceae)
-
Стафилококки (Staphylococcus spp.)
-
Стрептококки (Streptococcus spp.)
На самом деле понять нужен ли мне анализ на аэробы довольно просто:
-
Если есть жалобы (воспаление, зуд, жжение, выделения).
-
Продолжительное время и без результата Вы боретесь с «беспричинным» воспалением влагалища.
-
Результат анализов говорит о том, что у Вас восполнение влагалища (количество лейкоцитов повышено), но специфические возбудители не обнаружены.
Для исслеодвания необходимо сдать мазок на микроскопию и ПЦР исследование.
Результаты анализов врач будет трактовать следующим образом:
Микроскопия покажет количество лейкоцитов. Повышение этого количества говорит о воспалительной реакции. Она может быть вызвана аэробами.
ПЦР покажет есть ли в Вашей микрофлоре аэробы и какова их доля. Так как аэробы в небольшом количестве есть практически у каждой женщины, то именно количественный показатель поможет врачу определиться с диагнозом.
Флороценоз — Аэробы — это Ваша уверенность в правильности диагноза и эффективности лечения аэробного вагинита.
Проблема №5
Микоплазмы — это семейство со множеством видов. Заболевания могут вызвать только Ureaplasma urealyticum, Ureaplasma parvum, Mycoplasma genitalium и Mycoplasma hominis.
Если лечение Mycoplasma genitalium обязательно, то обнаружение других не дает однозначного ответа.
Популярные источники разделились во мнениях. Одни говорят, что необходимо срочно избавится от всех. Другие же утверждают, что обращать внимание на их присутствие не стоит и микоплазмы нормальные жители влагалища.
Можно заподозрить проблемы, если врач обнаружил у Вас воспаление влагалища и/или шейки матки. В этом случае тест Флороценоз-NCMT первоочередной. Он выявит NCMT инфекции если они есть. При отрицательном результате необходимы тесты Флороценоз — бактериальный вагиноз, Флороценоз — Аэробы и количественная ПЦР на Ureaplasma urealyticum, Ureaplasma parvum и Mycoplasma hominis.
Выявляем количество, но не наличие!
Мы часто видим, что у женщин мико- и уреаплазмы спокойно сосуществуют с нормальной микрофлорой влагалища. Сам факт их наличия никак не отображает истинную суть вещей. Они могут быть агрессорами или мирными соседями. Определение их количества более точная и полезная информация.
Стоит ли делать анализ на мико — и уреаплазмы понять довольно просто. Он необходим если:
-
Вы планируете беременность
-
У Вас было невынашивание или осложнения беременности
-
У Вас есть жалобы (выделения, боль внизу живота, межменструальные кровотечения) и нет NCMT – инфекций
-
У Вас выявлен бактериальный вагиноз или аэробный вагинит
-
Вам предстоит хирургическое вмешательство в области малого таза.
Врачу необходимо назначить следующие виды анализов:
-
Микроскопия мазка.
-
Флороценоз -Микоплазмы
Результаты анализов врач будет трактовать следующим образом:
Микроскопия покажет количество лейкоцитов. Повышение этого количества говорит о воспалительной реакции.
ПЦР может не только обнаружить, но и определить конкретный вид микоплазмы и его количество.
Флороценоз — Микоплазмы — это ПЦР- исследование в количественном формате
Результат количественного ПЦР-исследования Флороценоз — Микоплазмы и Ваши жалобы в совокупности с осмотром и опросом это необходимые и достаточные данные для врача. С их помощью будет понятно необходимо Вам лечение или нет.
Итак, 5 тестов на Флороценоз дают полную картину Вашему лечащему врачу!
Сдайте анализы сегодня — освободитесь от ложных представлений и домыслов.
Врачу необходимо назначить следующие виды анализов:
1. Флороценоз
2. Флороценоз и микроскопия мазка
3. Флороценоз и NCMT
4. Флороценоз, NCMT и микроскопия5. Комплексное исследование ИППП, качественное определение ДНК
Анатомия влагалища — VMC Verte medical clinic
Анатомия влагалища
16.12.2014
Автор статьи
Затикян Нара Геворковна
Врач ультразвуковой диагностики,врач акушер-гинеколог, первой категории.
Министерство здравоохранения и социального развития Российской Федерации
ГОУ ВПО Росздрава Российский Государственный Медицинский Университет
Кафедра акушерства и гинекологии московского факультета с курсом ФУВ
ГОРОДСКАЯ КЛИНИЧЕСКАЯ БОЛЬНИЦА №1 ИМ. Н.И. ПИРОГОВА
Влагалище (vagina s. colpos) представляет собой эластичный, трубкообразный мышечный орган, верхняя часть которого соединяется с шейкой матки, нижняя часть открывается в преддверии влагалища (vestibulum vaginаe). Влагалище является экстраперитонеальным органом – только его задний свод покрыт брюшиной. Он по отношению к матке находится под углом, равным к 90градусов. Последний открывается кпереди (anteflexio).
Влагалище — изогнутый полый орган с двумя чётко различимыми частями: выпуклой нижней частью и более широкой и объемной верхней частью, расположенной почти горизонтально, когда женщина стоит. Угол между верхней и нижней осями влагалища составляет 130 градусов. Длина влагалища составляет 10-12 см, ширина – 3 см, толщина стенки не превышает 3-4 мм. В средней части стенки влагалища соприкасаются.
Влагалище граничит:
спереди с мочевым пузырем и с мочеточником, разделяясь от них пузырно-влагалищной перегородкой. У основания мочевого пузыря, с помощью фасциальных утолщений (лобково-пузырные связки), передняя стенка влагалища соединяется с задней поверхностью лонной кости;
сзади с прямой кишкой, при этом нижняя его часть отделена от заднепроходного канала перитонеальным телом.
Влагалище со своей верхней самой подвижной частью, сливаясь с шейкой матки, формирует своды влагалища: передний, задний и два боковых. Задний свод самый глубокий, примыкает к прямокишечно-маточному углублению (дугласово пространство), через него производят все диагностические и лечебные манипуляции.
В связи с указанными топографическими особенностями, состояние соседних органов малого таза тесно взаимосвязано.
Структурные особенности стенки влагалища
Стенка влагалища состоит из трех слоев: внутреннего, среднего и наружного.
Наружный слой (adventia vaginae) преимущественно состоит из соединительной ткани и содержит отдельные мышечные волокна. Это довольно крепкий слой – особенно в нижних отделах влагалища;
Средний или мышечный слой (tunica muscularis), в свою очередь состоит из трех слоев гладкой мускулатуры (наружный и внутренний продольный, срединный кольцевидный). В нижних отделах влагалища – в области мочеполового треугольника, к гладкой мускулатуре присоединяются поперечно полосатые мышечные волокна, которые являются производными глубоких поперечных мышц промежности и мышц, поднимающих задний проход.
Внутренний слой (tunica mucosa) представлен многослойным плоским неорговевающим эпителием. Его поверхностные слои каждый месяц, в зависимости от фазы менструального цикла, отторгаются. Слизистая влагалище представляет собой видоизмененную кожу, но при этом лишена желез. В этом слое находятся ложные железы, которые представляют собой «каверны», образовавшиеся вследствие внедрения гладкого эпителия в мышечный слой.
В многослойном плоском эпителии, в свою очередь, различают следующие слои: поверхностный, промежуточный и базальный. Субмукозный слой влагалища слабо выражен, поэтому эпителий отделяется от мышечного слоя собственной оболочкой (membranа propria).
В период полового созревания слизистая влагалища приобретает поперечную и продольную складчатость. Поперечные складки (rugae vaginalis) более выражены на передней, особенно в области нижней трети и на задней стенке влагалища. Продольные складки образуют столбы (columnae rugarum), которые находятся, соответственно, по передней и задней стенке влагалища. Складчатость слизистой уменьшается после родов и у многорожавших женщин бывает невыраженной.
Емкость и размеры влагалища подлежат существенным индивидуальным колебаниям.
Кровоснабжение влагалища
Кровоснабжение влагалища осуществляется ветвями внутренней подвздошной артерии (a. iliaca interna) и нисходящей ветвью (a. cervicovaginalis) маточной артерии (a. uterinae). Влагалищная артерия, отходя от маточной артерии, продолжается по боковым стенкам влагалища и кровоснабжает его верхние отделы. Средняя часть влагалища питается от нижней пузырной артерии (a. vesicalis inferior). Средняя прямокишечная артерия (a. haemorrhoidalis media) и внутренняя половая артерия (a. pudenda interna) обеспечивают кровоснабжение нижних отделов влагалища.
Вены, отходящие от влагалища, составляют сплетение (plexus venosus vaginalis), откуда кровь собирается и переходит в нижнеабдоминальную венозную систему (v. hypogastricae), которая идет в обход портальной системы печени. Поэтому при влагалищном пути введении препараты всасываются быстро и постоянно, при этом не подвергаются первичному метаболизму в печени и применяются в виде активных метаболитов.
Лимфоотток влагалища
В основном отток лимфы от влагалища осуществляется двумя путями: от его нижней трети лимфа собирается в поверхностные и глубокие паховые лимфоузлы (gl. unquinalis), а от верхней – в три группы лимфоузлов малого таза (общие подвздошные, внутренние подвздошные и крестцовые).
Иннервация влагалища
Симпатическую иннервацию обеспечивает «солнечное» сплетение, отходящие от которого волокна образуют верхнее подчревное сплетение (plexus hypogastricus sinister et dexter superior), а дальше правые и левые нижние подчревные сплетения (plexus hypogastricus sinister et dexter inferior). От последних также отходят ветви, образующие в свою очередь маточно-влагалищное сплетение Рейна-Ястребова (plexus uterovaginalis), которое локализуется в параметральной клетчатке сбоку и сзади от матки, на уровне внутреннего зева и шеечного канала и непосредственно иннервирует влагалище. Парасимпатическую иннервацию обеспечивают ветви тазового нерва (n. pelvicus).
Кроме того, в верхней части влагалища находится мало чувствительных нервных волокон, что делает эту часть относительно нечувствительной. Вот почему женщины редко чувствуют локализованные ощущения или какой-либо дискомфорт при использовании таких вагинальных продуктов как тампоны, суппозитории или вагинальные кольца, и часто не задумываются о присутствии таких предметов во влагалище.
Функции влагалища
- Участвует в процессе оплодотворения.
Сперматозоиды, находящиеся во влагалище после эякуляции, поступают в цервикальный канал, который обладает слабощелочной реакцией, в результате чего повышается двигательная активность сперматозоидов.
- Имеет большое значение при родовой деятельности.
Влагалище совместно с шейкой матки формирует родовой канал, через который проходят плод и послед. Эластичность стенки влагалища обеспечивается гиперплазией и гипертрофией мышечных элементов, серозным пропитыванием всех слоев (за счет усиления кровоснабжения) во время беременности.
- Защитная функция.
Гликоген, синтезируемый в эпителиальных клетках под воздействием эстрогенов, расщепляется палочками Додерляйна (Н2О2 продуцирующие лактобациллы – ЛБ+) до молочной кислоты, которая обеспечивает кислотность влагалищной среды, которая оказывает бактерицидное действие на патогенную флору.
- Диагностическая функция.
Исследуя морфо-функциональные изменения многослойного плоского эпителия, можно судить о функциях яичников.
- Лечебная функция.
Многочисленные медицинские препараты (вагинальные суппозитории и таблетки, контрацептивные средства) имеют трансвагинальный путь введения в организм женщины.
Микроэкология влагалища
Микроэкология влагалища это сложные взаимоотношения между вагинальной средой и микрофлорой влагалища, имеет большое значение, как в гинекологии, так и в неонатологии.
Вагинальная среда: Стенки влагалища и влагалищная часть шейки матки покрыты многослойным плоским неорговевающим эпителием, не содержащем желез. Клетки базального слоя эпителия делятся и созревают в процессе их продвижения к просвету влагалища.
Вагинальный секрет: представляет собой серозный транссудат, секрет желез слизистой канала шейки матки и больших желез преддверия влагалища, лейкоциты, клетки слущенного эпителия. Основной химический состав вагинального секрета – вода, неорганические соли, белки (альбумины, иммуноглобулины), углеводы, жирные кислоты, мочевина, лизоцим. Физиологическое созревание эпителиоцитов, их слущивание, обогащение гликогеном, а так же обеспечение кислотности вагинального секрета – это эстрогензависимые процессы, находящие под контролем яичниковых гормонов.
Особенности экологии влагалища в разные периоды жизни
В норме влагалище новорожденных девочек в первые часы жизни стерильно. Однако, уже к концу первых суток, оно колонизируется аэробными и факультативно-анаэробными микроорганизмами, а через несколько дней во влагалище начинают преобладать лактобактерии. Это обусловлено тем, что трансплацентарным путем полученные от матери эстрогены индуцируют интенсивное накопление гликогена в эпителиальных клетках. Так как гликоген является субстратом для роста лактобактерий, увеличение его количества приводит к преобладанию последних. Но, через 3 недели после рождения, материнские эстрогены полностью метаболизируются. Эпителий становится тонким, «незрелым», содержание в нем гликогена уменьшается, и в связи с этим, снижается уровень органических кислот, продуцируемых бактериями. Реакция влагалищного содержимом (рН) повышается с 4,5 до 7,0. Нейтральные значения рН способствуют снижению окислительно-восстановительного потенциала, что обуславливает снижение содержания лактобактерий. В микрофлоре начинают доминировать строго анаэробные бактерии. Общее количество микроорганизмов во влагалище у девочек, со второго месяца жизни, значительного ниже, чем в период новорождения, когда во влагалище уровень эстрогенов высокий.
В пубертатный период с момента активации овариальной функции и появления в организме девушек эндогенных эстрогенов происходит накопление гликогена в клетках вагинального эпителия (эстроген-стимулированный эпителий). На поверхности вагинальных эпителиоцитов повышается число рецепторных участков для адгезии лактобактерий, увеличивается толщина эпителиального слоя. С этого момента лактобактерии вновь становятся доминирующими и в последующем сохраняют это положение на протяжении всего репродуктивного периода женщины. Метаболизм лактобактерий способствует стабильному сдвигу рН вагинальной среды в кислую сторону до 3,8-4,4. С другой стороны, в вагинальной среде повышается окислительно-восстановительный потенциал, что создает менее благоприятные условия для роста и размножения строго анаэробных микроорганизмов.
У здоровых женщин детородного возраста эстрогены воздействуют на вагинальный эпителий в фолликулярную (пролиферативную) фазу менструального цикла, а прогестерон – в лютеиновую (секреторную) фазу. В связи с этим, вагинальная микрофлора может меняться в различные фазы менструального цикла. По данным одних авторов наименьшее количество микроорганизмов определяется в период менструации, а по данным других – в период менструации определяется более интенсивный рост микрофлоры, чем через 7 дней после её окончания. Предполагается, что менструальная кровь является питательной средой, поддерживающей рост микроорганизмов. Частота высеваемости и количество строго анаэробных и большинства аэробных представителей нормальной микрофлоры выше в пролиферативную фазу, чем в секреторную. По данным Ohashi A. (1980), во 2-14 день менструального цикла во влагалище аэробные бактерии преобладают над строго анаэробными микроорганизмами, а непосредственно перед менструацией количество строго анаэробных микроорганизмов в 100 раз выше количества аэробных бактерий.
При наступлении менопаузы, в половом тракте существенно снижается уровень эстрогенов, гликогена и окислительно-восстановительного потенциала, уменьшается количество лактобактерий и бифидобактерий, рН среды приобретает нейтральные значения. Обедняется и качественный состав микрофлоры, снижается также общее содержание бактерий. Среди выявляющихся во влагалище микроорганизмов преобладают облигатно-анаэробные бактерии.
У беременных женщин концентрация гликогена во влагалище увеличивается, что создает благоприятные условия для жизнедеятельности лактобактерий. Увеличивается скорость колонизации половых путей дрожжевыми микроорганизмами и лактобактериями. Количество лактобактерий значительно увеличивается по сравнению с уровнем у небеременных женщин. В то же время уменьшается количество бактероидов и других неспорообразующих строгих анаэробов, а также аэробных грамположительных кокковидных и грамотрицательных палочковидных бактерий. Эти изменения достигают пика в III триместре беременности. Морфо-функциональные, физиологические и биохимические изменения в генитальном тракте во время беременности приводят к тому, что вагинальная микрофлора становится более однородной, с выраженным доминированием лактобктерий, что, в свою очередь, снижает вероятность контаминации плода условно-патогенными микроорганизмами при его прохождении через родовые пути. В итоге ребенок рождается в среде, содержащей микроорганизмы с низкой вирулентностью.
Роды приводят к существенным изменениям качественного и количественного состава микрофлоры влагалища: значительно увеличивается количество неспорообразующих грамотрицательных строгих анаэробов (преимущественно бактероидов), эшерихий и снижается содержание лакто- и бифидобактерий. Нарушения нормальной вагинальной микрофлоры, возникающие к 3 – 4 суткам после родов, способствуют развитию таких инфекционных осложнений как эндометрит. Резко наступающие изменения микрофлоры родовых путей, возможно, связаны с травмой родового канала, контаминацией влагалища кишечной микрофлорой, выделением лохий, значительным снижением уровня эстрогенов. Однако изменения микрофлоры в этих случаях являются транзиторными, и к 6 неделе послеродового периода вагинальная микрофлора восстанавливается до нормы.
Защитные механизмы влагалища
- Физиологические бели (в норме 1 -2 мл/сут).
- Физиологическая десквамация эпителия.
- Микрофлора влагалища (конкурирование с патологическим агентами за питательные вещества)
- Создание кислой среды (рН влагалищного содержимого в пределах 4-4,5).
- Колонизационная резистентность влагалищного секрета.
- Цервикальная пробка (обеспечивает механическую преграду за счет вязкости).
- Иммунная система
- Бактерицидные вещества (перекись водорода, лизоцим, лизин, бактериоцины и т.д.)
Механизм поддержания нормальной кислотности влагалищной среды
В пролиферативной фазе менструального цикла эстрогены индуцируют накопление в эпителиальных клетках гликогена (последний является субстратом для роста лактобактерий) и стимулируют рецепторную активность вагинального эпителия по отношению к лактобактериям. Вследствие десквамации и цитолиза поверхностных клеток эпителия влагалища, под воздействием прогестерона, в секреторной фазе происходит высвобождение гликогена и его ферментативное расщепление до сахара, мальтозы и декстрозы. которые с помощью лактобактерий, продолжают расщепляться до α-оксипропионовой (молочной) кислоты, что приводит к сдвигу рН в кислую сторону (до 4,4-4,6). Тем самым ограничивается рост и размножение микроорганизмов, чувствительных к кислой среде.
КОЛОНИЗАЦИОННАЯ РЕЗИСТЕНТНОСТЬ
Колонизационная резистентность — это совокупность механизмов, поддерживающих стабильность популяционного и количественного состава компонентов нормального микробиоценоза.
Механизмы действия колонизационной резистентности влагалища:
- Доминирование лактобактерий. Лактобактерии преобладают не только во влагалище, но и в дистальном отделе уретры, что препятствует колонизации нижних отделов мочевыделительной системы уропатогенными микроорганизмами.
- Конкуренция анаэробных бактерий с другими микроорганизмами за питательные вещества и рецепторы на эпителиальных клетках; продукция анаэробными бактериями антимикробных соединений – органических кислот, которые снижают рН влагалища, бактериоцинов и бактериоциноподобных веществ, и, возможно, биосурфактантов.
- Продукция лактобациллами перекиси водорода. Этим можно объяснить присутствие продуцирующих перекись водорода лактобацилл во влагалище большинства здоровых женщин, и отсутствие или значительное снижение у женщин с бактериальным вагинозом или вагинитом.
- Фагоцитарная активность (способность осуществлять киллинг) лейкоцитов и достаточное количество гуморальных факторов – опсонинов, способствующих процессу киллинга.
- Наличие в цервикальной слизи комплекса белков, обладающих прямой антимикробной активностью опсонинов. Примером таких биоцидных белков являются лизоцим и β-лизины влагалищного отделяемого, которые выделяются в основном тромбоцитами. Лизоцим, помимо выраженной литической активности в отношении, прежде всего, грамположительных бактерий, способен усиливать фагоцитарную активность нейтрофилов. Также, сущзествует мнение, что этот белок может обеспечивать естественную толерантность организма к чужеродным агентам. Во-первых, эта функция реализуется за счет участия лизоцима в регуляции иммунных и метаболических процессов. Во-вторых, обволакивая генетически чужеродный материал, лизоцим защищает его посредством нейтрализации и выведения из организма повреждающих компонентов.
- Наличие в цервикальной слизи антител, вырабатываемых, прежде всего, местной лимфоидной тканью (IgA, и IgM) и поступающих из кровеносного русла (IgA, IgM и IgG). Эти антитела также способны стимулировать фагоциты в уничтожении бактерий. Так, например, при бактериальном вагинозе содержание иммуноглобулинов в крови практически не меняется, а их уровень во влагалищном секрете претерпевает значительные изменения. На фоне снижения IgA, заметно возрастает уровень IgM. Значительное их повышение объясняется тем, что IgM составляют основную часть антител против липополисахаридных О-антигенов (эндотоксины) грамотрицательных бактерий, которые замещают лактофлору при данном заболевании. Снижение IgA ведет к уменьшению числа опсонизированных бактериальных клеток. В результате этого их фагоцитоз становится менее вероятным.
Таблица №1. Основные показатели нормального биоценоза влагалища.
| рН | < 4,5 |
| Общая колонизация | 105 – 108 КОЕ/мл |
| Общая численность условнопатогенных микроорганизмов | не более 103 – 104 КОЕ/мл |
| Доминирующая флора | Lactobacillus spp. (95 – 98%) |
| Основные «защитные» бактерии | Lactobacillus spp.
Bifidobacterium spp. |
Таблица №2. Микроскопическая характеристика биоценоза влагалища в норме и при патологии (Кира Е.Ф. 2001).
| Нормоценоз | Доминирование лактобактерий, отсутствие грамотрицательной микрофлоры, спор, мицелия, псевдогифов, лейкоцитов. Единичные «чистые» эпителиальные клетки. | Типичное состояние нормального биотопа влагалища |
| Промежуточный тип | Умеренное или сниженное количество лактобак-терий, наличие грамположительных кокков, грамотрицательных палочек. Обнаруживаются лейкоциты, моноциты, макрофаги, эпителиальные клетки. | Часто наблюдается у здоровых женщин, редко сопровождается субъектиными жалобами и клиническими проявлениями |
| Дисбиоз влагалища | Незначительное количество или полное отсутствие лактобактерий, обильная полиморфная грамотрицательная и грамположительная палочковая и кокковая флора; наличие «ключевых клеток». Количество лейкоцитов вариабельно, отсутствие или незавершенность фагоцитоза. Полимикробная картина мазка. | Бактериальный вагиноз |
| Вагинит (воспалительный тип мазка) | Большое количество лейкоцитов, макрофагов, эпителиальных клеток, гонококков, трихомонад, мицелия, псевдогифов, спор; выраженный фагоцитоз. | Неспецифический вагинит. Гонорея. Трихомоноз. Микотический вагинит. |
Таблица №3. Видовой состав микрофлоры влагалища здоровых женщин репродуктивного возраста.
| Виды микроорганизмов | Частота выделения
(%) |
Способность вызвать заболевание |
| МИКРОАЭРОФИЛЬНЫЕ БАКТЕРИИ | ||
| Lactobacillus spp. Lactobacillus fermentum Lactobacillus crispatus Lactobacillus jensenii Lactobacillus gasseri Lactobacillus acidophilus Lactobacillus plantarum Lactobacillus brevis Lactobacillus delbruckii Lactobacillus salivarius |
71-100 | – |
| Gardnerella vaginalis | 6-60 | + |
| ОБЛИГАТНО-АНАЭРОБНЫЕ ГРАМПОЛОЖИТЕЛЬНЫЕ БАКТЕРИИ | ||
| Lactobacillus spp. | 5-30 | – |
| Bifidobacterium spp. Bifidobacterium bifidum Bifidobacterium breve Bifidobacterium adolescentis Bifidobacterium longum |
12 | – |
| Clostridium spp. | 10-25 | + |
| Propionibacterium spp. Propionibacterium acnes |
25
5 |
–
+ |
| Mobiluncus spp. | 30-90 | + |
| Peptostreptococcus spp. Peptostreptococcus asaccharolyticus Peptostreptococcus magnus Peptostreptococcus prevotii Peptostreptococcus tetradius |
80-88 53 32 32 |
+ |
| ОБЛИГАТНО-АНАЭРОБНЫЕ ГРАМОТРИЦАТЕЛЬНЫЕ БАКТЕРИИ | ||
| Bacteroides fragilis Bacteroides vulgatus Bacteroides ovatus Bacteroides distasonis Bacteroides uniformis Bacteroides caccae Bacteroides multiacidus |
9-13 | + |
| Prevotella spp. Prevotella bivia Prevotella disiens |
60 | + |
| Porphyromonas spp. Porphyromonas asaccharolytica |
31 | + |
| Fusobacterium spp. Fusobacterium nucleatum |
14-40 | – |
| Veilonella spp. | 11-14 | – |
| ФАКУЛЬТАТИВНО-АНАЭРОБНЫЕ ГРАМПОЛОЖИТЕЛЬНЫЕ БАКТЕРИИ | ||
| Corinebacterium spp. Corinebacterium aquatum Corinebacterium minutissium Corinebacterium equi Corinebacterium xerosis Corinebacterium bovis Corinebacterium enzymicum Corinebacterium kutsheri |
30-40 8-10 |
возбудители оппортунистических инфекций |
| Staphylococcus spp. Staphylococcus epidermidis Staphylococcus saprophyticus |
62 | + |
| Streptococcus spp. >Streptococcus viridans Streptococcus fecalis Streptococcus faecium Streptococcus agalactie |
+ | |
| Enterobacteriaceae | 5-30 | + |
| Esherichia coli Enterobacter spp. Klebsiella spp. Proteus spp. Proteus aerugenosa |
2-10 | |
| Mycoplasma hominis | 2-15 | + |
| Ureaplasma urealyticum | 6-7 | + |
| Mycoplasma fermentans | 2-5 | + |
| ДРОЖЖЕПОДОБНЫЕ ГРИБЫ РОДА CANDIDA | ||
| Candida albicans Candida tropicalis Torulopsis glabrata |
15-20 | + |
ЛАКТОБАКТЕРИИ
В основном своем лактобациллы – микроаэрофилы: культивируются в атмосфере углекислого газа или редуцированного содержания кислорода. В норме количество лактобацилл во влагалище здоровой женщины составляет 107 КОЕ/мл – это 95% всей микрофлоры влагалища. Выявлены значительные отличия видового состава лактобактерий, колонозирующих влагалище здоровых женщин:
L. acidophilus – встречаемость ~ 42,8%
L. paracasei
L. fermentum встречаемость ~ 10-18,6%
L. plantarum
L. corineformis встречаемость ~ 5,7%
L. catenaforme
Все они объединены под общим названием «палочки Додерлейна». Влагалище может быть колонизовано сразу 1-4 видами лактобактерий и практически не встречается одинаковой комбинации даже у двух женщин. При этом у одной и той же женщины, видовой состав лактобактерий непостоянный и меняется в различные периоды жизни.
Механизмы контроля вагинального биоценоза лактобактериями
- В процессе жизнедеятельности лактобактерий образуется молочная кислота и другие органические кислоты, поддерживающие низкий рН влагалищной среды. Снижение рН вагинального содержимого влечет за собой повышение его редокс-потенциала, что сильнее подавляет рост анаэробных микроорганизмов, поддерживая высокий окислительно-восстановительный потенциал. Закисление среды подавляет рост таких условно-патогенных микроорганизмов, как Candida albicans, Esherichia coli, Gardnerella vaginalis, Mobilinus spp., |Peptostreptococcus spp., Bacteroides spp. и других бактерий, выделяющихся из влагалища женщин с дисбиотическими нарушениями.
- Продукция лактобациллами перекиси водорода, которая необходима для подавления как близкородственных штаммов, так и других видов микроорганизмов напрямую или через пероксидазные системы. Лактобактерии, обладающие этим свойством (ЛБ+), эффективно предотвращают колонизацию влагалища такими бактериями, как P. bivia, P. disiens, Mobiluncus spp., которые играют важную роль в нарушении вагинальной микрофлоры. При наличии миелопероксидазы, ЛБ+ снижают жизнеспособность Gardnerella vaginalis в 2000 раз. Также ЛБ+ способны подавлять каталазную активность гонококков и рост Staphylococcus aureus. Рост во влагалище вышеперечисленных микробов в обратной степени зависит от колонизации ЛБ+. У женщин, страдающих дисбактериозом влагалища, только в 35% случае были выделены лактобактерии и только у 11% из них были ЛБ+. В то время как у 96% здоровых женщин все выделенные лактобактерии являются ЛБ+. Однако, на чувствительность бактерий к перекиси водорода оказывают влияние многие факторы: метаболическая активность, уровень каталазной активности микроорганизма-мишени, повышение рН среды и т.д.
- Высокая адгезивная способность лактобактерий к поверхности эпителиальных клеток. У эндогенных лактобактерий это качество более выраженное, поэтому они имеют селективное преимущества как перед условнопатогенными, так и перед экзогенными лактобактериями. Адгезином лактобактерий является липотейхоевая кислота. Прикрепляясь к эпителиоцитам, лактобактерии покрывают стенку влагалища сплошным слоем и препятствуют адгезии других микробов к рецепторам эпителиоцитов, обеспечивая тем самым колонизационную резистентность.
- Некоторые виды лактобактерий вырабатывают бактериоцины, которые являются термостабильными пептидами, имеют узкий спектр активности и воздействуют на близкородственные микроорганизмы. Лактобактерии могут также вырабатывать бактерициноподобные вещества. Последние не обладают типичными для бактериоцинов свойствами, имеют широкий спектр антимикробной активности, подавляя, грамположительные бактерии и грибы. Продукт L. salivarius subsp. CRL 1328 активен по отношению к Enterococcus faecalis и E.faecium. А продукт L. pentosus TV35b подавляет рост Clostridium sporogenes, C. tyrobutyricum, L. curvatus, L.fermentum, L.sake, Listeria innocua, Propionibacterium acidipropionici, Candida albicans.
- Способность лактобактерий к неспецифической стимуляции местного иммунитета. Этот эффект проявляется в виде активации макрофагов, накопления фагоцитов и местного повышения уровня иммуноглобулинов, воздействующих на патогенные микроорганизмы. Иммуностимулирующими свойствами обладает мурамилдипептид клеточной стенки лактобактерий.
ДИСБИОЗ
Дисбиоз – это нарушение подвижного равновесия микрофлоры, сущность которого определяется характером качественных и количественных изменений в видовом составе микробных ассоциаций.
Этапы развития инфекционного заболевания влагалища (Долгушина В.Ф. 2004).
I этап – адгезия микробов к эпителиальным клеткам, которая обеспечивается специальными механизмами.
II этап – закрепившись своими рецепторами на клетке, микробы начинают размножаться – патологическая обсемененность слизистой влагалища (вагинальный дисбиоз).
III этап – преодоление микроорганизмами защитных барьеров влагалища, проникновение в эпителиальные клетки или подлежащие ткани, индукция местной иммуновоспалительной реакции – клиническая манифестация (вагинит).
IV этап – преодоление местного защитного барьера – генерализация инфекции. При эффективной деятельности механизмов антимикробной защиты, инфекционный процесс может остановится на любом этапе.
Бактериальный вагиноз
Бактериальный вагиноз (БВ) — это общий невоспалительный синдром, связанный с дисбиозом влагалищного биотопа, характеризующийся чрезмерно высокой концентрацией облигатно и факультативно анаэробных условно-патогенных микроорганизмов и резким снижением или отсутствием молочнокислых бактерий в отделяемом влагалища.
В настоящее время БВ не рассматривается как инфекционный процесс влагалища. Частота возникновения БВ варьирует от 30 до 60-80% в структуре воспалительных заболеваний половых органов.
Номенклатура
1892г. – Неспецифический вагинит
1955г. – Вагинит, вызванный Haemophilus
1963г. – Вагинит, вызванный Corynebacterium
1980г. – Гарднерелез
1982г. – Анаэробный вагиноз
1983г. – Неспецифический вагиноз
1984г. – Бактериальный вагиноз
Слово «бактериальный» объясняет повышенное содержание аэробных и анаэробных бактерий во влагалище (с преобладанием последних), а «вагиноз» – отсутствие лейкоцитов – клеток ответственных за воспаление.
Этиология
Основная роль в возникновении бактериального вагиноза отводится нарушениям микробиоценоза влагалища, происходящим в результате воздействия как эндогенных, так и экзогенных триггерных факторов:
| Эндогенные триггерные факторы ↓ |
ЭкзогенныЕ триггерные факторы ↓ |
| Гормональные изменения при половом созревании, при беременности, после родов и абортов | Терапия антибиотиками, цитостатиками, кортикостероидами, противовирусными, противогрибковыми препаратами, лучевая терапия |
| Нарушение в системе местного иммунитета | Частые и чрезмерные влагалищные спринцевания |
| Изменение баланса между микроорганизмами во влагалище | Пороки развития и анатомические деформации после разрывов в родах, хирургические вмешательства |
| Снижение количества Н2О2 продуцирующих лактобактерий, и концентрации Н2О2 в содержимом влагалища | Инородные тела во влагалище, матке: влагалищные тампоны и диафрагмы, пессарии, ВМС и др. |
| Желудочно-кишечный тракт как резервуар микроорганизмов, ассоциированных с бактериальным вагинозом | Спермициды |
Патогенез
На фоне вышеуказанных триггерных факторов, во влагалище начинают преобладать не факультативные, а анаэробные лактобациллы, которые обладают недостаточной способностью продуцировать Н2О2. Поскольку перекись водорода подавляет рост патогенных микроорганизмов ввиду прямой токсичности, снижение ее количества приводит к увеличению содержания различных факультативных (Gardnerella vaginalis) и анаэробных (Bacteroides peptococcus) бактерий. Общая концентрация бактерий во влагалище возрастает до 1011 в 1 мл.
В результате уменьшается содержание молочной кислоты, повышается рН влагалищной среды, что в свою очередь стимулирует рост анаэробных микроорганизмов. При увеличении бактериального роста, возрастает продукция аномальных аминов факультативными анаэробами. Амины, при увеличении вагинального рН, становятся летучими, обусловливая типичный «рыбный запах», усиливающийся при добавлении 10% раствора КОН во влагалищный секрет.
Бактериальные полиамины, вместе с находящимся во влагалище органическими кислотами (уксусной и сукциновой), оказывают цитотоксическое действие, вызывая отторжение эпителиальных клеток, что приводит к обильным вагинальным выделениям. Gardnerella vaginalis способствует усилению десквамации эпителиальных клеток, особенно в условиях алколоза, обнаруживаемого при бактериальном вагинозе. В результате адгезии микроорганизмов на поверхности десквамизированных эпителиальных клеток, образуются так называемые «ключевые клетки» или «влагалищный песок», которые имеют важное дифференциально-диагностическое значение при бактериальном вагинозе.
Вышеперечисленные процессы имеют следующее схематическое изображение:
Таблица№4. Патогенез бактериального вагиноза.
Уменьшение лактобацилл, продуцирующих Н2О2
↓
Повышение рН влагалищного содержимого
↓
Рост анаэробов
↓
Выделение аминов («рыбный запах»)
↓
Формирование «ключевых клеток»
Диагностика
Диагноз может быть поставлен на основании наличия не менее 3-х указанных признаков (критерии Амселя):
Ÿ Белые или сероватые гомогенные выделения, покрывающие всю слизистую влагалища;
Ÿ рН > 4,5;
Ÿ Положительный аминотест: «рыбный» запах при смешивании влагалищного отделяемого с 10% КОН;
Ÿ Обнаружение «ключевых» клеток в мазках из влагалища, окрашенных по Грамму, или в нативном препарате.
Микроскопия вагинального мазка с окраской по Грамму
Ÿ Массивное количество микрофлоры с преобладанием облигатных анаэробов:
— Gardnerella vaginalis в 100% случаев
— Mobiluncus в 50-70% случаев
— Mycoplasma hominis в 60-75% случаев
Ÿ Полное отсутствие или не большое количество лактобацилл
Ÿ Отсутствие лейкоцитарной реакции
Особые указания
Ÿ Культуральное исследование (посев) на Gardnerella vaginalis не рекомендуется, т.к. этот возбудитель часто обнаруживается у здоровых женщин
Ÿ Обследование не проводят во время менструации
Ÿ Исследование проводят не ранее чем через 72 часа после последнего полового сношения
Ÿ На бумагу для рН-метрии не должна попадать вода или слизь
Принципы терапии
Ÿ Противомикробная терапия, направленная на подавление анаэробной флоры, местно или системно
Ÿ Восстановление нормальной микрофлоры влагалища
Ÿ Коррекция иммунитета и эндокринного статуса, устранение провоцирующих факторов
Ÿ При бессимптомном течении лечение обязательно при беременности, наличии патологии шейки матки, при предстоящих гинекологических операциях.
Ÿ После проведенной терапии рекомендуется провести курс восстановления нормальной микрофлоры влагалища
Ÿ Рутинное лечение половых партнеров не рекомендуется
Гормональный статус и микробиоценоз влагалища
На состояние микрофлоры влагалища женщин, в сочетании с многими другими факторами, также имеет большое влияние гормональный статус организма в целом (оптимальное соотношение эстрогенов и прогестерона). Установлено, что гормональные нарушения в организме женщины создают благоприятный фон для развития воспалительного процесса нижнего отдела гениталий.
Слизистая оболочка влагалища реагирует на различные гормоны, но к эстрогенам она более чувствительна. Резистентность влагалища к инфекции во многом определяется насыщенностью организма эстрогенами. Эстрогены стимулируют пролиферацию многослойного плоского эпителия и повышают продукцию гликогена в поверхностных клетках. Непрерывно слущивающиеся эпителиальные клетки подвергаются цитолизу, с освобождением гликогена, который является идеальным субстратом для жизнедеятельности и роста лактобактерий. При снижении уровня эстрогенов, нарушается процесс образования гликогена, ухудшаются условия для жизнедеятельности лактобактерий и количество их уменьшается. Это приводит к снижению колонизационной резистентности слизистой влагалища и шейки матки, увеличению количества факультативной микрофлоры, что создает благоприятные условия для развития и хронизации воспалительного процесса.
Второй путь влияния гормонов на защитные механизмы влагалища обеспечивается способностью прогестагенов снижать содержание сиаловой кислоты в слизи цервикального канала, что ведет к изменению её биохимических свойств. Слизь становится более вязкой и резистентной для пенетрации как для сперматозоидов, так и для микроорганизмов.
Первичность гормональных нарушений при развитии воспалительного процесса подтверждается тем, что выраженность дисбиотических явлений в шейке матки и во влагалище мало зависит от этиологии воспалительного процесса, а больше связана с характером гормональных нарушений. Наиболее значимое угнетение резидентной флоры наблюдается при дисфункции яичников, менее существенное – при гиперпролактинемии и изменении уровня гормонов гипофиза. При гормональных нарушениях обсемененность влагалища и цервикального канала условно патогенными микроорганизмами обратно пропорциональна содержанию в них лактобактерий и бифидобактерий. Улучшение состояния микрофлоры цервикального канала и влагалища происходит при проведении противовоспалительной терап
Вернуться
Нормоценоз влагалища и его влияние на здоровье женщин
Различные органы и полости человека с присущей им микрофлорой представляют собой единую экологическую систему – микробиоценоз. Микробиоценоз различных органов и полостей человека является весьма чувствительной индикаторной системой, которая способна реагировать качественными и количественными изменениями на любые физиологические и патологические сдвиги в состоянии макроорганизма и препятствовать инвазии патогенных микрорганизмов. Нормальная микрофлора влагалища у здоровых женщин репродуктивного возраста характеризуется широким спектром микроаэрофилов, факультативных и облигатных анаэробов.
Влагалище с присущей ему микрофлорой образуют единую систему, в которой вагинальная среда контролирует микрофлору, а микрофлора, в свою очередь, оказывает воздействие на вагинальную среду ;1 ,2;.
Микроэкология влагалища во многом обусловлена его эмбриональным происхождением и гистоморфологическим строением. Влагалище покрыто многослойным неороговевающим плоским эпителием, который не содержит желез. Делящиеся клетки базального слоя эпителия созревают в процессе их продвижения к просвету влагалища. Процессы физиологического созревания эпителиоцитов, их слущивания и толщина поверхностного слоя подвержены циклическим изменениям в ответ на действие половых гормонов.
Эпителий влагалища выполняя защитную функцию, обеспечивает его устойчивость к воздействию патогенных агентов (бактерии, вирусы, грибы). Важным показателем резистентности вагинального эпителия является количество гликогена, который содержится преимущественно в поверхностных клетках. Поскольку эти клетки постоянно слущиваются и подвергаются цитолизу, гликоген освобождается, обеспечивая питательный субстрат для нормальной микрофлоры. Гликоген также способствует регенерации тканей, является важным углеводным компонентом организма, принимающим участие в выработке иммунных тел. Таким образом, возможные гормональные изменения на протяжении жизни женщины (пубертат, менопауза, беременность) определяют интенсивность ферментативных процессов во влагалище и оказывают влияние на состояние его микрофлоры. Нормальная микрофлора влагалища у здоровых женщин репродуктивного возраста характеризуется большим разнообразием видов бактерий, жизнедеятельность которых во многом зависит от их способности к адгезии на клетки вагинального эпителия и возможности конкуренции между собой за места обитания и продукты питания. Микрофлора влагалища здоровых женщин репродуктивного возраста включает широкий спектр микроаэрофилов, факультативных и облигатных анаэробов.
Чаще всего выделяют микроаэрофильные, продуцирующие H2O2 (71-100%), реже анаэробные (5-30%) грамположительные палочки – представителей рода Lactobacillus [3]. Среди представителей облигатных анаэробов с высокой частотой (30-90%) обнаруживают группу Peptostreptococcus, включающую в себя всех членов рода ранее известных как Peptococcus (за исключением P. niger) и все грамположительные анаэробные кокки, ранее идентифицированные как Gaffkya anaerobia. Грамположительные палочки, строгие анаэробы – Bifidobacterium spp. выявляются у здоровых женщин с частотой равной 12%, Clostridium spp. – в 10-25% случаев соответственно. В редких случаях (0-5%) в вагинальном отделяемом обнаруживают виды Mobiluncus [4, 5 ,6]. Типичными представителями нормальной микрофлоры генитального тракта у женщин являются Propionibacterium spp. (P. acnes), которые могут быть выделены с частотой до 25%. Грамотрицательные строго анаэробные палочковидные бактерии такие как Bacteroidides spp. (B. urealyticum, B. fragilis, B. vulgatus, B. ovatus, B. distasonis, B. uniformis, B. coccae, B. multiacidus), выявляются у 9-13% женщин, Fusobacterium spp. у 14-40%, Porphyromonas spp. у 31%, Prevotella spp. присутствуют во влагалище у женщин в 60% случаев. Значительное место отводится Pr. bivia и Pr. disiens – уникальным микроорганизмам женского полового тракта, роль которых приравнивается к роли B. fragilis в кишечнике [7,8]. B. fragilis выделяют из половых путей здоровых женщин, по разным данным, в 5-12% случаев [9].
Микроаэрофилы во влагалище здоровых женщин помимо лактобактерий представлены G. vaginalis. По данным различных авторов G. vaginalis встречается в 6-60% случаев [10,11].
Среди факультативно-анаэробных микроорганизмов часто выделяют каталазопозитивные, коагулазонегативные S.epidermidis, и новобиоцинрезистентные S. saprophyticus (62%), Streptococcus spp. (стрептококки группы viridans – «зеленящие», альфа (или гамма), гемолитические, стрептококки серологической группы В (Str. agalactie) и стрептококки серологической группы D (энтерококки), непатогенные коринебактерии (C. minutissium, C. equi (новое название Rhodococcus equi), C. aquaticum, C. xerosis) присутствуют у 30-40%. E. coli, по разным данным, выделяют у 5-30% женщин [12,13,14]. Прочие энтеробактерии (Klebsiella spp., Citrobacter spp., Enterobacter spp.) встречаются менее чем у 10% здоровых женщин. Для нормоценоза характерно присутствие генитальных микоплазм – M. hominis и U. urealyticum, которые встречаются у 2-15% сексуально активных женщин, в то время как M. fermentas определяются редко [15].
Дрожжеподобные грибы рода Candida: C. albicans, C. tropicalis и Torulopsis glabrata (ранее Candida glabrata) выявляются во влагалище здоровых женщин в 15-20% случаев. Candida albicans – наиболее характерный вид, определяемый у 80-90% женщин, влагалище которых колонизировано грибами рода Candida [16].
Отделяемое влагалища в норме содержит 108-1012 КОЕ/мл микроорганизмов, при этом факультативно-анаэробные бактерии составляют 103-105 КОЕ/мл, анаэробные – 105-109 КОЕ/мл [15,17,18]. На фоне всего видового многообразия ведущее место в вагинальном микроценозе занимают микроаэрофильные лактобактерии число которых может достигать 109 КОЕ/мл [19]. Колонизируя слизистую влагалища, лактобактерии участвуют в формировании экологического барьера и обеспечивают тем самым резистентность вагинального биотопа. Защитные свойства лактобактерий реализуются по-разному: за счет антагонистической активности, способности продуцировать лизоцим, перекись водорода и адгезивных свойств. Однако основным механизмом, обеспечивающим колонизационную резистентность вагинального биотопа является способность лактобактерий к кислотообразованию. Молочная кислота – продукт метаболизма лактобактерий. Она образуется в процессе деструкции гликогена вагинального эпителия лактобактериями и определяет кислую реакцию рН вагинального содержимого, которое в норме составляет 3,8-4,5. Лактобактерии продуцируют молочную кислоту в количествах, достаточных для создания выраженной кислой среды вагинального отделяемого и, тем самым, препятствуют размножению ацидофобных бактерий.
Бифидобактерии, входя в состав микроценоза влагалища, как и бактерии рода Lactobacillus, относятся к флоре Дедерлейн. У здоровых женщин репродуктивного возраста они выявляются с меньшей частотой, в концентрациях 103-107 КОЕ/мл. Как и лактобактерии, они относятся к кислотопродуцирующим микроорганизмам и участвуют в поддержании во влагалище низких значений рН. Бифидобактерии адгезируются на поверхности эпителиальных клеток влагалища, способны продуцировать бактериоцины, лизоцим, спирты, что также обеспечивает им участие в создании и поддержании колонизационной резистентности во влагалище по отношению к условно-патогенным и патогенным микроорганизмам. Бифидобактерии синтезируют аминокислоты и витамины, которые активно используются организмом хозяина в его метаболизме.
Пептострептококки являются третьей составляющей частью флоры Дедерлейн. Количество анаэробных кокков в вагинальном отделяемом составляет 103-104 КОЕ/мл. Несмотря на то, что пептострептококки составляют часть нормальной флоры женского полового тракта, их часто обнаруживают при септических абортах, трубно-яичниковых абсцессах, эндометритах и других тяжело протекающих инфекциях женских половых органов. В ассоциации с другими анаэробными бактериями пептострептококки в большом количестве случаев выделяют при бактериальном вагинозе.
Пропионобактерии – комменсалы человеческого организма. За счет вырабатываемых ими органических кислот эти бактерии могут участвовать в поддержании колонизационной резистентности влагалища. Обладают иммуностимулирующими свойствами. Выделяются в количествах, не превышающих в норме 104 КОЕ/мл [20,21].
В норме количественный уровень порфиромонасов, вейлонелл и фузобактерий не превышает 103 КОЕ/мл, а бактероидов и превотелл – 104 КОЕ/мл соответственно [22].
Патогенные свойства строго анаэробных грамотрицательных бактерий связаны с их ферментативными системами. Так, у B. fragilis выявлены гиалуронидаза, коллагеназа, фибринолизин, иммуноглобулин-протеазы, гепариназа и сиалидаза. B. fragilis обладают и другими факторами патогенности, например, капсульным полисахаридом. Кроме того бактероиды группы «fragilis» способны к продукции каталазы, что позволяет им противостоять действию H2О2 , вырабатываемой лактобактериями. Различные протеазы и коллагеназы были найдены у бактерий рода Porphyromonas. Протеазы и фибринолизин выявлены также у различных видов рода Prevotella. Fusobacterium necrophorum обладают способностью синтезировать гемолизин и факторы агрегации томбоцитов.
У бактероидов, фузобактерий, а также у анаэробных стептококков и гарднерелл была выявлена высокая способность к продукции фосфолипазы А2. Последняя в свою очередь активирует продукцию простогландинов путем освобождения арахидоновой кислоты из ее эфирной формы. У беременных женщин бактериальные протеазы и липазы могут воздействовать на хорионамниотическую мембрану, приводя к ее разрыву. Нарушение целостности хорионамниотической оболочки в совокупности с увеличением концентрации простогландинов в амниотической жидкости инициируют преждевременные роды [23,24].
Органические кислоты, продуцируемые грамотрицательными анаэробами, а также бактериями рода Mobiluncus, в частности янтарная кислота, ингибируют функциональную активность полинуклеарных нейтрофилов, с чем связывают малое количество последних или их полное отсутствие в выделениях из влагалища при бактериальных вагинозах.
Таким образом, бактерии – представители нормальной микрофлоры влагалища тесно взаимодействуя между собой и с клетками вагинального эпителия создают и поддерживают высокую колонизационную резистентность влагалищного биотопа, но иногда могут стать причиной воспалительных процессов урогенитального тракта. Ввиду того, что вагинальная микрофлора помимо защитной функции выполняет и ряд других важных функций – ферментативную, витаминообразующую, иммуностимулирующую и др., ее обычно рассматривают как индикатор состояния влагалища [25,26].
При определении видового состава микрофлоры влагалища, по данным Е.Ф. Киры [27], среди анаэробных грамположительных бактерий нередко выявляются коагулазонегативные стафилококки, что составляет 34-92%. Особое значение, как возбудителям заболеваний, принадлежит S. еpidermidis и S. haemolyticus. Во влагалище здоровых женщин эпидермальный стафилококк можно обнаружить в 90% случаев [28]. Этот микроорганизм активно участвует в обеспечении колонизационной резистентности.
Гемолитический стафилококк (S. haemolyticus) может быть выделен из влагалища здоровых женщин при отсутствии признаков инфекции. В определенных условиях эти микроорганизмы могут стать возбудителями инфекционных процессов урогенитального тракта. Возможно носительство данных бактерий на коже перианальной области (источник развития вагинитов) [29].
Золотистый стафилококк (S. aureus) не входит в состав нормальной микрофлоры генитального тракта, но нередко в небольшом количестве выделяется из влагалища клинически здоровых женщин. По данным ряда авторов, он колонизирует влагалище транзиторно и обнаруживается лишь в 5% случаев. Поэтому наличие золотистого стафилококка в вагинальной микрофлоре не является признаком патологии [30]. Его этиологическая значимость определяется количественными исследованиями [29].
Клостридии (Clostridium spр.) встречаются у 10-25% женщин. При бактерильных вагинозах их частота увеличивается [31].
Нередко в генитальном тракте женщин встречаются стрептококки (гемолитические и негемолитические). Эти микроорганизмы также являются обитателями слизистых оболочек дыхательных путей, пищеварительного и в определенных условиях способствуют развитию инфекционных процессов [32]. Наибольшее клиническое значение имеют стрептококки групп A (S. рyogenes), B (S. аgalactiae) и D (S. bovis). В вагинальном секрете содержится стрептококк группы B (S. agalactiae).
По данным Г.В. Ершова, Д.Н. Бочкарева, И.В. Смоленова [33] при воспалительных заболеваниях органов малого таза (ВЗОМТ) у женщин были выявлены культуры S. pyogenes (10,5% случаев), S. viridans (7,9%) и S. pneumoniae (1,8%).
Среди аэробных микроорганизмов наиболее часто встречаются энтерококки (Enterococcus). Из них на долю E. faecalis приходится 80-90%, E. faecium – 5-10%. В генитальном тракте здоровых женщин они встречаются в 10% случаях. Энтерококки входят в состав нормальной микрофлоры кишечника, где их концентрация достигает 106 КОЕ/мл [34]. В последнее время возросла роль энтерококков при инфекциях мочевыводящих путей [35,36]. По мнению Г.В. Ершова, Д.Н. Бочкарева, И.В. Смоленова [33] E. faecalis имеет этиологическое значение в развитии ВЗОМТ.
Среди грамотрицательных условно-патогенных бактерий наиболее часто выделяют эшерихии [37]. Распространенность Escherichia coli, по данным Л.И. Кафарской, О.В. Коршунова, Б.А. Ефимова [38], составляет 10-30%, а количественный показатель – 10-104 КОЕ/мл. Нередко они обнаруживаются в структуре микрофлоры, выделенной из мочи женщин с пиелонефритом (50-58,3%), а также из цервикального канала при сальпингоофорите (11,2-19,9%).
Прочие энтеробактерии встречаются менее, чем у 10% здоровых женщин (бактерии рода Klebsiella). Клебсиеллы – факультативные анаэробы [39]. Они могут быть причиной урогенитальных инфекционных заболеваний [40].
Таким образом, бактерии – представители нормальной микрофлоры влагалища, тесно взаимодействуя между собой и с клетками вагинального эпителия, создают и поддерживают высокую колонизационную резистентность влагалищного биотопа, но иногда могут стать причиной воспалительных процессов урогенитального тракта. Ввиду того, что вагинальная микрофлора помимо защитной функции выполняет и ряд других важных функций — ферментативную, витаминообразующую, иммуностимулирующую и др., ее обычно рассматривают как индикатор состояния влагалища[41, 42].
Литература:
Добротина В.Т. Основы иммунологии / В.Т. Добротина. – М. – 2003. – 225 с
Савченко Т.Н. Определение видового состава и чувствительности к антибактериальным препаратам беременных с кандидозным вульвовагинитом на ранних сроках беременности / Т.Н. Савченко, М.Х. Точиева, Е.И. Гиммельфарб и др. // I Международный конгресс по репродукции. – М. – 2006. – С.221-222.
Соколовский Е.В., Савичева А.М., Домейка М. и др. Инфекции, передаваемые половым путём. Руководство для врачей. – М.: МЕДпресс-информ, 2006. – 123 с
Ковтун О.Г. Современные аспекты послеродового эндометрита (ретроспективный анализ) / О.Г. Ковтун // Материалы 7 Всероссийского научного форума «Мать и дитя», 2005. – С.98-99.
Порсохонова Д.Ф., Курбанов Д.Д., Арифов С.С. и др. Клинико-иммунологическая характеристика урогенитальных и экстрагенитальных поражений при хламидийной и уреаплазменной инфекции у женщин // Цитокины и воспаление. – 2005. – Т.4, №4. – С.4-6.
Шабашова Н.В., Мирзабалаева А.К., Долго-Сабурова Ю.В. и др. Роль про- и противовоспалительных цитокинов в патогенезе хронического рецидивирующего кандидозного вульвовагинита у женщин // Материалы Международного Конгресса «Практическая гинекология: от новых возможностей к новой стратегии». – Москва, 2006. – С.212-213.
Кулаков В.И. Актуальные проблемы антимикробной терапии и профилактики в акушерстве, гинекологии и неонатологии / В.И. Кулаков, Б.Л. Гуртовой, А.С. Анкирская, А.Г. Антонов // Акушерство и гинекология. – 2004. – №1. – С.3-6.
Eschenbach D.A., Davick P.R., Williams B.L. et al. Prevalence of hydrogen peroxide-producing Lactobacillus species in normal women and women with bacterial vaginosis // J. Clin. Microbiol. – 1999. – V.27, №2. – P.251-256.
Кудрина М.И. Вульво-вагинальный кандидоз. // Москва, 2005. – 18 с.
Вихляева Е.М. Руководство по эндокринной гинекологии / Е.М. Вихляева– Мед. информ. агентство. – 2006. – 784 с.
Brabin L. Interactions of the female hormonal environment, susceptibility to viral infections, and disease progression // AIDS Patient Care STDS. – 2002. – V.16, №5. – P.211-213.
Кира Е.Ф., Муслимова С.З. Современный взгляд на нетрансмиссионные инфекции влагалища и вульвы у женщин репродуктивного возраста // Акушерство и гинекология. – 2008. – №1. – С.3-6.
Eschenbach D.A. Bacterial vaginosis and anaerobes in obstetric-gynecologic infection // Clin. Infect. Dis. – 1993. – Vol.16, Suppl.4. – P.282-287.
Overmann B.A. The vaginal as an ecologyc system. Current understanding and clinical application // J. Nure Midwifery. – 2003. – V.38, №3. – P.146-151.
Кира Е.Ф. Инфекция и репродуктивное здоровье (часть 3). Клинические проявления инфекционных заболеваний влагалища, включая СТЗ // Журнал акушерства и женских болезней. – 2001. – №1. – С.50-55.
Adamson G.D., Brown D.Jr., Standard J.V., Sadoff J. et al. Tree day treatment with butaconazole vaginal cream for vulvovaginal candidiasis // J. Reprod. Med. – 1996. – Vol. 31. – P. 131-132.
Егорова Е.В., Минскер О.Б. Грибковые и некоторые паразитарные заболевания женских половых органов. — М.: Медицина, 1999.- С.219.
Погодин О.К. Хламидийная инфекция в акушерстве, гинекологии и перинатологии. – Петрозаводск, 2007. – 29 с.
Лебедев В.А., Давыдов А.И. Урогенитальный хламидиоз // Вопр. гинекол., акуш. и перинатол. – 2002. — №2. – С.25-31.
Хаитов Р.М., Пинегин Б.В. Основные представления об иммунотропных лекарственных средствах // Иммунология. –1996. – №6. – С.4-9.
Вульфович Ю.В., Раковская И.В., Гамова Н.А. и др. Лабораторная диагностика микоплазмоза и уреаплазмоза у урологических и гинекологических больных // Журн. микробиол., эпидемиол., иммунол. – 2005. – №5. – С.97-100.
Савичева А.М., Башмакова М.А. Микробиоценозы влагалища и их регуляция // Тез. докл. научн. конф. «Дисбактериозы и эубиотики». – М., 1996. – С. 33.
Назарова Е.К., Гиммельфарб Е.А., Созаева Л.Г. Микробиоценоз влагалища и его нарушения // Клинич. лаборат. диагн. – 2003. – №2. – С.25-32.
Воробьев А.А., Абрамов Н.А., Бондаренко В.М., Шендеров Б.А. Дисбактериозы – актуальная проблема медицины // Вестн. РАМН. – 2007. – №11. – С.12-18.
Глазкова Л.К., Акилов О.Е. Практические аспекты персистирующей хламидийной инфекции // ИППП. – 1999. – №4. – С.29-34.
Серов В.Н., Краснопольский В.И., Делекторский В.В. и др. Хламидиоз. Клиника, диагностика, лечение // Методические рекомендации. – М., 2006. – 18 с.
Кира Е.Ф. Инфекция и репродуктивное здоровье (часть 3). Клинические проявления инфекционных заболеваний влагалища, включая СТЗ // Журнал акушерства и женских болезней. – 2001. – №1. – С.50-55.
Анкирская А.Е. Бактериальный вагиноз // Акуш. и гинек. – 2005. – №6. – С.13-16.
Арутюнян К.Н. Клинико-микробиологические особенности современного течения пуэрперального эндомиометрита. Автореф. дис… канд. мед. наук – Самара, 2008. – 24 с.
Стрижаков А.Н. Эндометриоз: клинические и теоретические аспекты / А.Н. Стрижаков, А.И. Давыдов. – М.: Медицина. – 2006. – 330 с.
Кафарская Л.И., Коршунова О.В., Ефимов Б.А. Микробная экология влагалища // ЖМЖИ. – 2002. – №6. – С.91-99.
Оганян К.А. Течение и исход беременности при колонизации мочеполового тракта женщин стрептококками группы B и D: Автореф. дис… канд. мед. наук – Санкт-Петербург, 2008. – 24 с.
Ершов Г.В., Бочкарев Д.Н., Смоленов И.В. Этиологическая структура и резистентность возбудителей воспалительных заболеваний органов малого таза у женщин // Клиническая микробиология и антимикробная химиотерапия. – 2004. – Т.6. – №2. – С.193-199.
Сидоренко С.В., Резван С.П., Грудинина С.А., Кротова Л.А., Стерхова Г.В. Результаты многоцентрового исследования антибиотикочувствительности энтерококков // Антибиотики и химиотерапия. – 1998. – №9. – С.9-18.
Ковтун О.Г. Современные аспекты послеродового эндометрита (ретроспективный анализ) / О.Г. Ковтун // Материалы 7 Всероссийского научного форума «Мать и дитя», 2005. – С.98-99.
Анохова Л.И., Загородняя Э.Д., Дашкевич О.Ю. Профилактика эндометрита после кесарева сечения методом эндоваскулярного лазерного облучения // Мать и дитя: Материалы VII Российского форума, 11-14 окт. 2005 г. – М., 2005. – С.17-18.
Страчунский Л.С. Современная антимикробная химиотерапия /Л.С. Страчунский, С.Н. Козлов // Руководство для врачей. – Москва, 2002. – 436 с.
Кафарская Л.И., Коршунова О.В., Ефимов Б.А. Микробная экология влагалища // ЖМЖИ. – 2002. – №6. – С.91-99.
Воробьев А.А., Быков А.С. Атлас по медицинской микробиологии, вирусологии и иммунологии. – 2003. – 236 с.
Сидорова И.С., Боровкова Е.И. Микрофлора половых путей у женщин репродуктивного возраста. – М.: Практическая медицина, 2007. – 80 с.
Ларсен Б. Микрофлора половых путей в норме // Общие инфекции / Под ред. Л.Г.Кейта, Г.С. Бергера, Д.А. Эдельмана. – М.: Медицина, 1988. – Гл.1. – С.17-45.
McCormack W. M. The genital mycoplasmas // II. N. Engl. J. Med. – 1980. – Vol. 301. – P. 1063-1067.
Основные термины (генерируются автоматически): женщина, вагинальный эпителий, влагалище, бактерия, бактерия рода, нормальная микрофлора влагалища, репродуктивный возраст, вагинальная микрофлора, генитальный тракт, защитная функция.
Что означает результат моего теста?
Если вы только что прошли тест на носительство стрептококка группы B, независимо от результата, не беспокойтесь.
Ношение GBS совершенно нормально и естественно и не представляет опасности для здоровья и не вызывает симптомов у человека, являющегося носителем бактерий. Если вы знаете, что являетесь носителем СГБ, вы можете предпринять шаги, чтобы свести к минимуму относительно небольшую вероятность того, что у вашего ребенка разовьется инфекция СГБ.
Если вы делали частный тест, важно сообщить врачу / акушерке результат, положительный он или отрицательный.
Если стрептококк группы B был обнаружен во время беременности из вагинального или ректального мазка , лечение НЕ рекомендуется до начала родов, когда вам следует незамедлительно предложить внутривенные антибиотики *.
Если в образце мочи во время беременности был обнаружен стрептококк группы B , возможно, у вас инфекция мочевыводящих путей. Если да, то для лечения вам должны назначить антибиотики. Вам также следует предложить внутривенные антибиотики, когда начнутся роды *.
Нет никаких доказательств того, что прием антибиотиков для носительства GBS до родов снижает инфицирование GBS у новорожденных. Доказано, что антибиотики очень эффективны в предотвращении инфекции GBS у новорожденных, когда их вводят как можно скорее после начала родов, а затем через регулярные промежутки времени до рождения ребенка. Это резко снижает риск заражения СГБ у новорожденного.
* Все национальные руководства Великобритании рекомендуют предлагать маме внутривенные антибиотики во время родов, если СГБ был обнаружен во время текущей беременности.
Послушайте, как Фиона Гибсон узнала о стрептококке группы B, прошла тестирование, принимала антибиотики в родах и как ребенок Нейт родился здоровым и здоровым.
Если вы не беременны и носительство СГБ было обнаружено, вам не нужно ничего делать. Стрептококк группы B является нормальным.
Мои вагинальные симптомы вызваны стрептококком группы B?
Нам не известны убедительные доказательства того, что ношение СГБ вызывает вагинальные симптомы.Ношение СГБ протекает бессимптомно. СГБ, обнаруженный во влагалищном мазке, означает, что во влагалище было колонизировано СГБ на момент взятия мазка — это не означает, что СГБ является причиной каких-либо исследуемых симптомов.
Насколько надежны результаты моих тестов?
Статус носительства стрептококка группы B может меняться в течение более длительных периодов времени. В странах, где все беременные регулярно проверяются на стрептококк группы B, это обычно проводится на сроке от 35 до 37 недель беременности.
Положительный результат тестаПоложительный результат теста очень надежен. Любой положительный результат теста (NHS или частный) является очень сильным показателем того, что GBS присутствовал при взятии образцов. Очень маловероятно, что тест даст ложноположительный результат (т. Е. Обнаружит стрептококк группы B, когда его нет).
Отрицательный результат тестаНадежность отрицательного результата теста на носительство стрептококка группы B зависит как от того, откуда были взяты образцы, так и от того, какой метод использовался для обработки этих образцов.
Если вы принимали или недавно закончили принимать антибиотики во время взятия образцов, это может повлиять на результаты ваших анализов — поговорите об этом со своей акушеркой или врачом.
Если результат «стандартного» теста NHS отрицательный
Отрицательный результат теста на стрептококк группы B стандартного мазка NHS не является надежным — этот тест дает высокую долю ложноотрицательных результатов. Этот тест обнаруживает стрептококк группы B только примерно в половине случаев, когда он присутствует, поэтому около половины (50%) носителей стрептококка группы B получат неверный ответ.
Если результат теста ЕСМ (частного или NHS) отрицательный.
Отрицательный результат теста на стрептококк группы В в результате теста ЕСМ является очень надежным. Исследования показали, что при правильном выполнении теста ECM (обогащенная питательная среда) в течение 5 недель после родов матери, отрицательный результат на 96% означает, что она , а не будет иметь стрептококк группы B, когда она родит ( Таким образом, только 4% женщин приобрели носительство GBS между тестом и родами).
Подробнее о различных тестах, используемых для обнаружения стрептококка группы B, можно узнать здесь.
Какие у меня есть варианты, где я рожу ребенка?Вы можете составить план родов, который поможет вам сообщить вашей медицинской бригаде, какие роды вы хотели бы иметь, и чего бы вы хотели, и чего вы хотели бы избежать.Стрептококк группы B не всегда означает, что вам нужно изменить план родов.
Вам следует обсудить запланированное место рождения со своим врачом или акушеркой во время беременности, чтобы убедиться, что вы можете принимать антибиотики во время родов для защиты от инфекции GBS у вашего новорожденного ребенка.
Пенициллин G — это обычно назначаемый антибиотик (альтернативы доступны для женщин с аллергией на пенициллин). Пенициллин G вводится внутривенно (в / в) в течение 15-30 минут каждые четыре часа, и это может оказаться невозможным в домашних условиях или в некоторых акушерских отделениях (особенно автономных).Очень важно, чтобы вы сообщили своим врачам, если у вас когда-либо была аллергическая реакция на пенициллин или любой другой антибиотик.
Вы должны сообщить своему врачу или акушерке, если у вас ранее был ребенок с инфекцией стрептококка группы B, или если у вас был положительный результат теста на стрептококк группы B во время этой или предыдущей беременности.
Как только у вас начнутся схватки или у вас отойдет вода, обратитесь к врачу, поскольку, если вы носите СГБ и решили принимать антибиотики, важно, чтобы вы получили первую дозу как можно скорее.
Если вы решите использовать антибиотики во время родов, вы все равно сможете свободно передвигаться.
Щелкните ниже, чтобы узнать больше о: —
Мне предложили мембранную развертку. Безопасно ли это для женщин-носителей стрептококка группы B?
Нет убедительных доказательств того, что протирание мембраны вредно для женщин с СГБ. Результаты испытаний мембранных очистителей не показывают какого-либо увеличения проблем, вызванных СГБ, у женщин, подвергшихся очистке, и весьма вероятно, что в эти испытания было включено много женщин с СГБ.
Теоретически остается риск того, что очистка мембраны может иногда вводить GBS в матку. Поэтому наша медицинская консультативная группа рекомендует с осторожностью использовать мембранную очистку для женщин с СГБ, когда есть другие приемлемые альтернативы (например, индукция родов с помощью геля простагландина, введенного во влагалище).
Каковы признаки того, что стрептококк группы B влияет на моего будущего ребенка?
Хотя СГБ встречается редко, он может вызвать инфицирование ребенка в утробе матери, что может привести к преждевременным родам, мертворождению и позднему выкидышу.К счастью, это встречается нечасто, поскольку и мать, и ее ребенок обладают естественной защитой от заражения ребенка СГБ до начала родов или отхождения воды. Если ваша беременность протекает нормально, нет оснований подозревать, что стрептококк группы B заражает вашего ребенка.
В том маловероятном случае, если инфекция GBS действительно разовьется, обычно начинаются роды или происходит разрыв плодных оболочек. Пришло время как можно скорее попасть в больницу, чтобы ввести внутривенные антибиотики, чтобы обеспечить вашему ребенку наилучшую защиту.
Если вас что-то беспокоит во время беременности (в том числе, если у вас уменьшились шевеления плода, что может быть признаком дистресса ребенка), вам в первую очередь следует посоветоваться с акушеркой. Если ее нет, обратитесь в родильный дом — вам помогут.
Если обнаружен стрептококк группы B, когда мне следует принимать антибиотики?Если стрептококк группы B был обнаружен в вагинальном или ректальном мазке , антибиотики не будут вводиться до начала родов — лечение носительства антибиотиками до начала родов не снижает вероятность развития у вашего ребенка стрептококковой инфекции группы B.
Когда начнутся роды, вам предложат внутривенные (IV) антибиотики. Эти антибиотики снижают риск развития СГБ-инфекции у вашего ребенка в первую неделю жизни на 85-90%, от примерно 1 из 400 рожденных до примерно 1 из 4000.
Если в вашем организме был обнаружен стрептококк группы B моча , вам могут потребоваться таблетки антибиотика, так как у вас может быть инфекция мочевыводящих путей (ИМП). Вам также предложат внутривенные антибиотики, как только начнутся роды, чтобы защитить вашего новорожденного ребенка от стрептококковой инфекции группы B.
Если у вас был предыдущий ребенок, у которого развилась стрептококковая инфекция группы B , вам всегда следует предлагать внутривенные антибиотики во время родов при будущих беременностях, поскольку существует повышенный риск заражения будущего ребенка.
Рекомендуемая страница
Стрептококк группы B в моей моче
Стрептококк группы B, обнаруженный в моче, не всегда означает наличие инфекции, особенно при низком уровне обнаруженных бактерий. Иногда бывает так, что…
Подробнее
Существуют и другие ситуации, когда вам будут предложены антибиотики, но они не имеют прямого отношения к стрептококковой инфекции группы B:
- Если у вас преждевременные выделения воды (до 37 недель) и вы не рожая, вам могут предложить антибиотики.См. Информационную брошюру Королевского колледжа акушеров и гинекологов: https://www.rcog.org.uk/en/patients/patient-leaflets/when-your-waters-break-prematurely/. Возможно, вас заинтересует руководство NG25 Национального института здравоохранения и повышения квалификации (NICE) по преждевременным родам и родам: https://www.nice.org.uk/guidance/ng25/chapter/Recommendations
- Если у вас Если вы планируете кесарево сечение и у вас стрептококк группы B, вам не нужны внутривенные антибиотики, специфичные для стрептококка группы B, за исключением случаев, когда роды уже начались или у вас отошли воды.Всем женщинам, перенесшим кесарево сечение, во время операции будут предложены антибиотики, чтобы снизить риск широкого спектра инфекций, в том числе стрептококка группы B.
Если стрептококк группы B был обнаружен во время предыдущей беременности, и у вашего ребенка не развилась инфекция стрептококка группы B , существует 1 из 2 (50%) шансов, что вы снова будете переносить стрептококк группы B во время этой беременности.Чтобы помочь вам выбрать, хотите ли вы вводить антибиотики внутривенно во время родов, вы можете пройти специальный мазок (известный как обогащенная культуральная среда или тест ECM), чтобы узнать, есть ли у вас GBS на 35–37 неделе беременности.
Клинические руководства рекомендуют вам предлагать этот тест ECM от NHS, но мы знаем, что некоторые больницы NHS еще не предлагают тесты ECM. Если ваша больница не может предложить тестирование ECM, вы можете приобрести тест ECM в частном порядке.
Если результат показывает, что:
- вы носите Strep группы B, то риск развития у вашего ребенка стрептококковой инфекции группы B с ранним началом увеличивается примерно до 1 из 400, и вам будут предложены антибиотики внутривенно во время родов. .
- , если вы не являетесь носителем стрептококка группы B , то риск развития у вашего ребенка стрептококковой инфекции группы B с ранним началом намного ниже (1 из 5000), и вы можете отказаться от внутривенного введения антибиотиков в родах.
Если вам предложили внутривенно антибиотики для предотвращения инфицирования стрептококками группы B у вашего новорожденного ребенка, их следует начать как можно скорее после начала родов или отхождения воды.Их вводят внутривенно с помощью канюли, обычно на тыльной стороне ладони, и через регулярные промежутки времени (каждые 4 часа, если вам вводят пенициллин G, с разными интервалами для приема антибиотиков, рекомендованных женщинам с аллергией на пенициллин) до тех пор, пока ваш ребенок родился.
Вы по-прежнему можете двигаться во время родов, а внутривенные антибиотики не должны мешать вам рожать в воде.
Если вода выйдет за пределы до , когда у вас начнутся схватки, ваш врач или акушерка обсудят с вами, когда вам понадобятся антибиотики внутривенно, и о том, когда лучше всего родиться.Это будет зависеть от ваших индивидуальных обстоятельств и от того, сколько недель вы беременны.
Рекомендуемая страница
Внутривенные антибиотики во время родов
Если вы согласились на внутривенное (в / в) введение антибиотиков во время родов против ранней инфекции СГБ, их следует ввести как можно скорее, как только роды начались, и …
Подробнее
Могут ли в / в антибиотики во время родов причинить вред?Некоторые женщины могут испытывать временные побочные эффекты, например, плохое самочувствие или диарею.У женщин может быть аллергия на определенные антибиотики, и в редких случаях реакция может быть серьезной или даже опасной для жизни (анафилаксия). Сообщите своему врачу или акушерке, если вы знаете, что у вас аллергия на пенициллин или другие лекарства.
Ваш врач или акушерка должны обсудить с вами как преимущества, так и риски внутривенного введения антибиотиков во время родов, чтобы предотвратить раннее начало инфекции GBS у вашего ребенка.
Если вы решите не вводить внутривенные антибиотики во время родов, ваш ребенок будет находиться под тщательным наблюдением в течение 12 часов после рождения, поскольку он подвержен повышенному риску развития стрептококковой инфекции группы B с ранним началом.
Я не хочу принимать антибиотики при родах — есть ли естественные альтернативы?
Члены нашей медицинской консультативной группы изучили альтернативы, но не убеждены в том, что любая терапия, кроме антибиотиков во время родов, эффективна для предотвращения раннего начала инфекции GBS.
Один вопрос, который нам часто задают в последнее время, заключается в том, снижает ли сырой чеснок, введенный вагинально, вероятность заражения СГБ у новорожденного ребенка. Нет убедительных доказательств того, что чеснок предотвратит колонизацию GBS, и, поскольку резервуаром для колонизации GBS является кишечник, чеснок вагинально не повлияет на колонизацию там.Точно так же нет убедительных доказательств того, что чеснок предотвратит заражение СГБ у ребенка.
Несмотря на то, что это является предметом многочисленных дискуссий, не существует натуральных, гомеопатических или альтернативных лекарств, для которых есть хорошие исследования, показывающие, что они эффективны для предотвращения инфицирования стрептококками группы B у новорожденных. Если это изменится, мы выпустим обновление.
Если у вас есть какие-либо вопросы о стрептококках группы B, позвоните в нашу службу поддержки
пн-пт 9.00-17.00
0330120 0796
Или напишите нам по адресу info @ gbss.org.uk
Подробнее о профилактике GBS-инфекции у вашего ребенка во время родов
Быстрые роды
Индукция родов
Домашние роды
Водные роды
Кесарево сечение
Стрептококк группы B в моче
Внутривенные антибиотики во время родов
Доказательства инфекции у бессимптомных женщин?
Справочная информация .Значение возможного наличия инфекции в мазке Папаниколау бессимптомных женщин по цитологическим критериям практически неизвестно. Материалы и методы . В общей сложности 1117 бессимптомных небеременных женщин прошли мазок Папаниколау и были выполнены посевы из влагалища и шейки матки (622 с воспалением и 495 без воспаления в мазке Папаниколау). Результатов . Из 622 женщин с воспалением по Пап-тесту у 251 (40,4%) были отрицательные посевы (присутствует нормальная флора), а у 371 (59.6%) у женщин были положительные культуры с разными возбудителями. Напротив, группа женщин без воспаления на мазке Папаниколау показала значительно увеличенный процент отрицательных культур (67,1%,) и уменьшенный процент положительных культур (32,9%,). Бактериальный вагиноз диагностировался чаще в обеих группах и значительно чаще в группе с воспалением на мазке Папаниколау по сравнению с группой без воспаления (). Выводы . Отчет о воспалительных изменениях в мазке Папаниколау шейки матки не может быть использован для надежного прогнозирования наличия инфекции половых путей, особенно у бессимптомных женщин.Тем не менее, выделение различных патогенов примерно у 60% женщин с воспалением на мазке Папаниколау нельзя упускать из виду и к нему следует относиться с беспокойством.
1. Введение
Инфекции половых путей часто встречаются у женщин репродуктивного возраста, и связанные с этим расходы являются значительными. Было отмечено, что многие женщины остаются бессимптомными при вагините или цервиците [1, 2]. Папаниколау (Пап-тест) — это простая, быстрая и безболезненная процедура, выполняемая на клетках шейки матки и используемая в качестве скринингового теста для профилактики рака шейки матки [3, 4].При сообщении результатов мазка Папаниколау шейки матки обычно делается замечание о возможном наличии инфекции на основании цитологических критериев [5]. Клиническое значение воспаления в мазке по Папаниколау у бессимптомных женщин практически неизвестно, так как не существует руководств по соответствующему лечению. Таким образом, клиницисты часто сталкиваются с дилеммой, следует ли рекомендовать этим женщинам делать посевы из влагалища / шейки матки, чтобы изолировать возможные патогены [6, 7]. В этом исследовании оценивалась возможная связь между воспалением в мазках Папаниколау и наличием цервикальных / вагинальных патогенов, определяемая посевом.
2. Материалы и методы
Исследуемая популяция состояла из бессимптомных небеременных женщин репродуктивного возраста, поступивших в амбулаторную клинику акушерства и гинекологии университетской больницы Аретайо для рутинного анализа мазка Папаниколау в период с января 2008 года по май 2012 года и которые дали согласие на обследование. включены в это исследование. Комитет по этике больницы Aretaieio одобрил исследование, и от всех субъектов были получены формы информированного согласия.
Женщин посоветовали явиться в больницу через 10–20 дней после первого дня менструального цикла без использования вагинального душа или лекарств в течение как минимум месяца.Мазки, показывающие воспалительные изменения или отсутствие воспаления, были включены в это исследование, в то время как неадекватные мазки и мазки, показывающие любую атипичную морфологию, были исключены. Воспалительные изменения, обнаруженные в мазке, окрашенном по Папаниколау, включали присутствие клеток с увеличенными ядрами, пикноз или кариорексис, перинуклеарные ореолы и вакуоли. Часто регистрировали повышенное количество полиморфноядерных лейкоцитов или нейтрофилов и парабазальных клеток с генерализованной эозинофилией клеток. Кроме того, присутствие эпителиальных клеток, покрытых окрашенными в синий цвет кокковыми бактериями, на окрашенном мазке из шейки матки вместе с уменьшенным количеством или отсутствием лактобацилл свидетельствует о бактериальном вагинозе.
Бессимптомных женщин с воспалительными изменениями в мазке Папаниколау или без них вызывали для посева. Образцы половых путей (вагинальные и шейные) были доступны для анализа. Влажный образец, а также мазок, окрашенный по Граму, исследовали под микроскопом для выявления Trichomonas vaginalis и для получения ценной информации о присутствующих микроорганизмах (дрожжах и бактериях), а также для диагностики бактериального вагиноза с использованием методов Амселя и Нугента. критерии [8, 9].Женщин проверяли на наличие различных аэробных бактерий, то есть видов Candida , стрептококков группы B, Gardnerella vaginalis и Neisseria gonorrhoeae , а также анаэробных бактерий. Таким образом, клинические образцы, собранные у пациентов, высевали на соответствующие чашки для стандартных аэробных и анаэробных культур и инкубировали при 37 ° C в течение 24 и 48 часов соответственно. Выделенные патогены идентифицировали с помощью автоматизированной системы VITEK 2 (BioMerieux, Marcy l’Etoile, Франция).Кроме того, присутствие Chlamydia trachomatis , а также Ureaplasma urealyticum и Mycoplasma hominis в исследованных образцах было определено с помощью тестов COBAS AMPLICOR Chlamydia trachomatis (США) и диагностики Rocheplasma Mycoplasma (Rocheplasma , США) BioMerieux, Marcy l’Etoile, Франция) соответственно.
Статистический анализ проводился с использованием критерия хи-квадрат, и значения ≤0,05 считались значимыми.
3.Результаты
Всего у 1117 женщин были сданы анализы мазков и посевы из влагалища и шейки матки (622 с воспалением и 495 без воспаления на мазке Папаниколау). Результаты посева в исследуемой популяции представлены в таблице 1. У женщин с воспалением на Пап-тесте процент отрицательных посевов значительно снизился (), а процент положительных посевов увеличился (). Среди женщин с выявленными возбудителями половых путей бактериальный вагиноз диагностировался чаще в обеих группах.Интересно, что в группе с воспалением на мазке Папаниколау женщин с диагнозом бактериальный вагиноз было значительно больше по сравнению с группой без воспаления (). Выделение других патогенов, таких как видов Candida , Chlamydia trachomatis и T. vaginalis , а также случаи, диагностированные как аэробный вагинит (характеризуемые выделением Streptococcus agalactiae , грамотрицательных стержней и метицилл-резистентных палочек). Staphylococcus aureus ) не различались между двумя группами.
| ||||||||||||||||||||||||||||||||||||||||||||||
4. Обсуждение
В нашем исследовании мы провели посевы из влагалища и шейки матки на широкий спектр микроорганизмов без воспаления у женщин с Пап-тест для определения прогностической ценности этого вывода на предмет наличия патогенов у бессимптомных женщин.Мы установили, что почти 60% женщин с воспалительными изменениями в мазках из шейки матки имели положительные культуры на различные патогены. Характеристика цервиковагинальной микробной флоры необходима, и, таким образом, было бы целесообразно для всех пациентов с воспалением на Пап-тесте пройти микробиологическое обследование шейки матки и влагалища для выявления потенциальных патогенов для правильной диагностики и лечения. Келли и Блэк обнаружили, что 47% женщин с воспалительными изменениями при исследовании мазка из шейки матки имели микробиологически подтвержденную инфекцию [10].Wilson et al. также сообщили, что воспаление при цитологическом исследовании часто связано с инфекцией половых путей [11]. Подобные результаты и сопоставимые с нашими результатами были опубликованы в литературе [2, 12, 13]. Однако примерно у одной трети женщин без воспалительных изменений при мазке мазка посевы были положительными. Предыдущие исследования показали, что женщины без воспалительных изменений в мазках из шейки матки могут содержать патогены половых путей. Бертолино и др. отметили, что воспаление на мазке Папаниколау имеет относительно низкую прогностическую ценность для наличия вагинальных патогенов у бессимптомных женщин [5], в то время как Parsons et al.обнаружили высокий уровень положительных культур как у женщин с воспалительными изменениями, так и у женщин без воспалительных изменений при мазке мазка, что позволяет предположить, что воспаление на мазке Папаниколау является плохим индикатором цервикальной инфекции [6]. С другой стороны, Берк и Хики продемонстрировали, что распространенность инфекции была выше в группе мазка воспаления, таким образом подтверждая, что женщины с мазком воспаления более склонны к заражению половых путей, чем женщины, мазок которых не показывает признаков воспаления [7]. .
Бактериальный вагиноз — это состояние, при котором происходят впечатляющие микроэкологические изменения влагалищной флоры, характеризующиеся снижением количества Lactobacillus spp. и чрезмерный рост Gardnerella vaginalis вместе с анаэробами и потенциально патогенными бактериями, включая Ureaplasma urealyticum и Mycoplasma hominis . Воспаление на мазке Папаниколау было связано с 30–50% случаев бактериального вагиноза [14, 15], что согласуется с нашими данными.Более того, другие сообщают, что большинство мазков с воспалительными изменениями содержали ключевые клетки, что указывает на бактериальный вагиноз и делает вывод, что мазок Папаниколау хорошо подходит для диагностики цервикальных инфекций, связанных с бактериальным вагинозом [2, 7, 12].
Флора влагалища представляет собой сложную микросреду, которая состоит из различных видов бактерий в постоянно изменяющихся количествах и пропорциях. Хотя некоторые патологические состояния и клинические проявления четко определены, присутствие некоторых аэробных микроорганизмов можно рассматривать как колонизацию.В 2002 году Donders et al. предложили термин «аэробный вагинит», чтобы лучше определить патологическое состояние, которое коррелирует с присутствием аэробных бактерий, в основном стрептококков группы B, Escherichia coli и Staphylococcus aureus [16]. Интересно, что уже сообщалось, что Streptococcus agalactiae подавляет рост лактобацилл, а Gardnerella vaginalis , но не S. aureus [17, 18]. В нашей исследуемой популяции распространенность S.agalactiae и грамотрицательных палочек (в основном E. coli ) было ниже, чем в недавнем сообщении [19], но было аналогично сообщению Donders et al. [16] и Лукич и др. [20].
Staphylococcus aureus Влагалищная колонизация широко изучалась с момента возникновения синдрома токсического шока несколько десятилетий назад. Однако вагинальное носительство метициллин-устойчивого S. aureus (MRSA) не было хорошо документировано. Распространенность MRSA была низкой в нашей популяции и аналогична предыдущим отчетам в амбулаторной, негоспитализированной и бессимптомной выборке [16, 21].
Сорок три женщины (11,6%) с воспалением на мазке Папаниколау были положительными на инфекцию Candida , при этом большинство из них были диабетиками. Эти результаты согласуются с предыдущими результатами, представленными в литературе [16], но не согласуются с недавним отчетом, в котором в другой популяции частота инфицирования Candida у пациентов с воспалительными изменениями была очень высокой, 73,8% [13] . С другой стороны, наши результаты высоки по сравнению с другими сообщениями в литературе [2, 6, 22].
В некоторых исследованиях сообщается о корреляции между признаками воспаления при тестировании мазка и положительными образцами на Chlamydia trachomatis [5, 7, 12]. В нашей выборке распространенность положительных результатов тестирования C. trachomatis составила 0,8%, что соответствует предыдущим отчетам [6, 13, 15]. Скрининг инфекции нижних отделов половых путей с использованием интрацервикального или вагинального мазка на инфекцию Chlamydia следует проводить, даже если в некоторых группах населения заявленная распространенность является низкой, поскольку инфекция хламидиоза, в частности, имеет долгосрочные последствия для фертильности из-за ее потенциальной возможности. вызвать бессимптомное повреждение маточных труб.
Trichomonas vaginalis — паразит, вызывающий симптоматическую и бессимптомную инфекцию женской мочеполовой системы. Доказано, что выздоровление T. vaginalis чаще происходило у женщин с воспалением на мазке Папаниколау, чем у женщин без воспаления [5, 12]. В нашем исследовании только два образца были положительными на T. vaginalis у женщин с воспалением, что согласуется с другими данными о низкой распространенности [16, 22, 23] и отличается от исследований, в которых была обнаружена повышенная частота этого паразита [2, 13].
5. Выводы
Результаты нашего исследования показывают, что отчет о воспалительных изменениях в мазке Папаниколау шейки матки не может быть использован для надежного прогнозирования наличия инфекции половых путей, особенно у бессимптомных женщин. Необходимы дальнейшие исследования с продольным характером для изучения возможного наличия инфекции на основе цитологических критериев. Тем не менее, выделение различных патогенов примерно у 60% женщин с воспалительными изменениями в мазке Папаниколау шейки матки в отсутствие видов Lactobacillus нельзя игнорировать и к этому следует относиться с беспокойством.
Рекомендации по отбору и культивированию клинических образцов от беременных женщин на Streptococcus группы B
Редакция от 8 января 2003 г.
Скачать PDF-версию, отформатированную для печати:
Рекомендации по сбору и культивированию клинических образцов от беременных женщин на стрептококки группы B (PDF)
Обоснование
Стрептококковая инфекция группы B (GBS) является ведущей бактериальной инфекцией, связанной с болезнями и смертью среди новорожденных в Соединенных Штатах.GBS ( Streptococcus agalactiae ) передается вертикально от колонизированных женщин их младенцам до или во время родов. Раннее начало инфекции GBS (инфекция, возникающая менее чем за 7 дней жизни) может привести к тяжелой, потенциально смертельной инфекции у новорожденных, которая может включать сепсис, менингит и пневмонию.
Инфицированные младенцы могут страдать от неврологических осложнений и нуждаться в длительном лечении. госпитализация. Основные факторы риска раннего неонатального заболевания включают колонизацию GBS у матери, длительный разрыв плодных оболочек, внутриутробную лихорадку, роды на сроке менее 37 недель гестации, бактериурию GBS во время беременности и предыдущие роды ребенка с заболеванием GBS.СГБ также может вызывать заболевание у беременных. Инфекции, вызываемые СГБ у матери, включают бессимптомную бактериурию, эндометрит, амнионит, преждевременные роды, мертворождение и, в редких случаях, эндокардит. В 1996 году Центры по контролю и профилактике заболеваний (CDC) в сотрудничестве с Американским колледжем акушеров и гинекологов (ACOG) и Американской академией педиатрии (AAP) разработали рекомендации по профилактике перинатального заболевания GBS. Руководящие принципы включали выбор подхода на основе скрининга или без него.В 2002 году CDC разработал пересмотренные инструкции. Опубликованные 16 августа 2002 г. рекомендации рекомендуют универсальный скрининговый подход к профилактике перинатального СГБ. Используя метод скрининга, беременные женщины проходят скрининг на СГБ на сроке от 35 до 37 недель беременности. Поскольку желудочно-кишечный тракт является основным источником этого микроорганизма, подходящими образцами для посева являются вагинальный мазок и ректальный мазок. Образцы следует культивировать с использованием селективного обогащающего бульона. Значительное количество инфекций СГБ можно предотвратить с помощью скрининга преждевременных родов и последующей антимикробной профилактики во время родов (введение антибиотиков после начала родов или разрыва мембран, но до родов).В целом, пенициллин G является предпочтительным средством профилактики, специфичным для колонизации GBS, из-за его эмпирической эффективности против GBS и узкого спектра действия (вероятность выбора устойчивых к антибиотикам организмов меньше, чем у других агентов).
Коллекция образцов
Вискозные или дакроновые тампоны с непитательной транспортной средой сохраняют жизнеспособность организма, обеспечивая увлажнение и буферизацию для поддержания pH. Предлагаемый пример:
- Транспортная система мазков для культивирования R (Liquid Amies или Liquid Stuarts) Becton Dickinson, Sparks, MD 800-638-8663
Самый чувствительный метод обнаружения пренатальной колонизации GBS требует использования двух тампонов.Один тампон используется для получения образца из влагалища. Второй тампон используется для взятия образца из аноректума. Может быть предпочтительнее использовать отдельные мазки для каждого участка, чтобы исключить возможность ятрогенного переноса инфекционных агентов, таких как вирус папилломы человека (ВПЧ).
Посев из шейки матки и использование расширителя приводит к минимальной чувствительности и не рекомендуются.
Сразу после взятия пробы тампоны вставляются в транспортер. СМИ.Если собираются отдельные тампоны, оба тампона можно поместить в те же транспортные средства массовой информации. Когда используется соответствующий транспортный носитель, GBS из ректовагинальных мазков может оставаться жизнеспособным до 96 часов в комнате или холодильнике температура, позволяющая транспортировать в центральную микробиологическую лабораторию для обработки. Все образцы должны быть помечены явным источником (вагинально или ректально).
Образцы должны быть идентифицированы для лаборатории как специфические для стрептококка группы B.Неспособность указать образец в качестве экрана для GBS может привести к альтернативной обработке мазка, что снизит чувствительность обнаружения стрептококка группы B. Если для женщин с аллергией на пенициллин назначен тест на чувствительность, на этикетках образцов должно быть указано, что пациент страдает аллергией на пенициллин, и указаны тесты на чувствительность к антибиотикам для клиндамицина и эритромицина, если GBS изолирован.
Бульоны для селективного обогащения
Обширные исследования показали, что достигается оптимальное восстановление GBS. использование бульонов селективного обогащения в качестве метода первичного обнаружения.Эти бульоны могут состоять из бульона Тодда Хьюитта, который обеспечивает отличное питательное основа для стрептококков и специфические комбинации антибиотиков для подавления рост сапрофитных грамотрицательных организмов.
Примеры этих бульонов селективного обогащения включают:
- Бульон LIM (бульон Тодда Хьюитта с 10 мкг / мл колистина и 15 мкг / мл налидиксовой кислоты)
- Trans-Vag Broth (бульон Тодда Хьюитта с 8 мкг / мл гентамицина и 15 мкг / мл налидиксовой кислоты) (требуется добавление 5% дефибринированной овечьей крови для увеличения выделения GBS)
Вышеупомянутые бульоны для селективного обогащения доступны по адресу:
- Remel Microbiology Products, Lenexa, KS 800-255-6730
- Бектон Дикинсон, Спаркс, Мэриленд 800-638-8663.
Процедура культивирования
Всегда консультируйтесь с вкладышем производителя для обновления процедуры.
- При поступлении образца в лабораторию подготовьте селективный пробирка с обогащенным бульоном, промаркировав ее соответствующим образом. При использовании Транс-Ваг бульона добавьте 0,25 мл стерильной дефибринированной овечьей крови в каждую пробирку. Овечья кровь в бульон LIM не добавляется.
- Можно засеять первичные твердые среды с селективными агентами и / или без них. перед бульоном.Это нужно делать в дополнение, а не вместо посева в селективный бульон. Удалите тампон (и) из транспортного средства. систему и засеять чашки. Полоса для изоляции и инкубации при температуре 35-37 ° C в окружающем воздухе или CO2 в течение 18-24 часов.
- Вставьте тампон (и) в бульон для селективного обогащения в асептических условиях. техника. Если и вагинальный, и ректальный мазки взяты из одного пациенту, оба тампона могут быть помещены в один обогащенный бульон.Агитировать тампоном (-ами) и выдавите лишнюю жидкость на стенку пробирки. Тампон (-а) можно отломить в пробирку или вернуть в транспорт. систему сохранить в соответствии с индивидуальным лабораторным протоколом. Слабо винт колпачок на пробирку с посевом.
- Инкубируйте бульон и чашки в аэробных условиях при 35 ° C с CO2 или без него. на 24 часа. Через 24 часа осмотрите бульон на предмет наличия бактерий. рост (помутнение).Если нет помутнения, повторно инкубируйте бульон на дополнительные 24 часа. Даже если при 48 ° С нет видимого помутнения. ч., отвар может содержать небольшое количество организмов. Перейти к шагу
- Если рост присутствует в течение 24 часов или бульон был инкубирован в течение 48 часов пересейте бульон на одной или двух неселективных 5% овцах. чашки с кровяным агаром. Инкубируйте чашки для субкультур при 35 ° C в аэробных условиях.
- Наблюдайте за ростом субкультуры после полных 24 часов инкубации, чтобы наличие бета- или негемолитических стрептококков.Если отрицательный на 24 часов, повторно инкубируйте еще 24 часа, прежде чем сообщать об отрицательном результат.
Лабораторная идентификация бета-стрептококка группы B
В настоящее время наиболее надежным методом определения наличия GBS является идентификация от колониального роста. На агаре с овечьей кровью стрептококк группы В дает от полупрозрачных до непрозрачных, беловато-серых, мягких, гладких колоний. Большинство, но не все штаммы образуют относительно узкую зону бета-гемолиза.Случайные штаммы не вызывают бета-гемолиза.
Подозрительные колонии (каталаза-отрицательные, грамположительные кокки) должны быть идентифицированы. с помощью стандартных стандартных методов идентификации стрептококков группы B в том числе:
- Серологические группы стрептококков, такие как агглютинация на предметном стекле, точная и надежная методика выявления GBS. Если рост недостаточное или сильно перемешанное, пересейте в новую чашку.
- GBS можно идентифицировать с помощью алгоритма общепринятого биохимического анализа. тесты, такие как положительный тест CAMP, положительный гидролиз гиппурата, отрицательный желчный эскулин, отрицательный PYR, отрицательный VP и чувствительность к 30 ? g ванкомициновый диск. Предполагаемая идентификация GBS является удовлетворительной. метод идентификации, но не такой точный, как серологическая группировка.
- Флуоресцентное антитело или генетический зонд являются полезными вариантами и могут использоваться для идентификации бета-гемолитических колоний.
- Автоматизированные методы и наборы, включая микросканирование грамположительных панелей, Карты Vitek и полоски API могут идентифицировать GBS с высокой степенью точности, хотя по большей стоимости.
В настоящее время прямые (по мазку) методы обнаружения антигенов, такие как оптические
иммуноферментный анализ и иммуноферментный анализ высокоспецифичны, но недостаточно
чувствителен к обнаружению умеренного или низкого уровня СГБ.Поэтому использование прямого
методы обнаружения для скрининга СГБ НЕ рекомендуются, за исключением
необычные обстоятельства.
Предлагаемая отчетность
- При восстановлении GBS указать: Изолированный стрептококк группы B
- Если GBS не обнаружен, укажите в отчете: Стрептококк группы B не выделен
- Все результаты, положительные или отрицательные, должны быть сообщены заказывающий клиницист или отделение.
- Если посев из неподходящего источника (любого источника, кроме вагинального и ректально) получен, поставщик должен быть уведомлен.
- Любое количество GBS, выделенного в посеве мочи беременной женщины, должно быть сообщенным.
- Непрерывный доступ для врачей (24 часа в сутки, 7 дней в неделю) оптимален.
Контроль качества
Должны выполняться рекомендации производителей по пользовательскому контролю качества. на каждую партию бульона селективного обогащения.См. Документ NCCLS M22-A2, Декабрь 1996 г. Обеспечение качества коммерчески приготовленных микробиологических препаратов Культура СМИ — второе издание ; Утвержденный стандарт, для комплексного методические рекомендации.
Если в среде обнаружен недостаток, это должно быть задокументировано лабораторией. и производитель должен быть уведомлен. Соответствующее корректирующее действие должны быть установлены и отмечены в лабораторных записях. Качество медиа отказ управления должен привести к дополнительному тестированию среды до тех пор, пока причину недостатка можно выявить и устранить.
* Примечание: Не используйте носители, которые выглядят взломанными.
Всегда обращайтесь к вкладышу производителя по поводу обновлений процедуры
Предлагаемые меры контроля качества включают:
- А. Визуальный осмотр
(Изучите каждую партию каждой партии на предмет физического дефекты или износ)- 1. Треснувшие или сломанные пробирки или крышки
- 2.Доказательства замерзания
- 3. Загрязнение
- 4. Утечка
- B. Процедура испытания бульона
- Streptococcus agalactiae ATCC 12386 (рост от умеренного до сильного)
- Escherichia coli ATCC 25922 (частичное или полное ингибирование)
- 1.При использовании Trans-Vag Broth добавьте 0,25 мл стерильного дефибринированного раствора в асептических условиях. овечья кровь в каждую пробирку.
- 2. Засейте отдельные бульоны вышеуказанными микроорганизмами QC:
- a. Засейте стерильными пипетками пробирки с разведением 1,0 мл. 18-24ч культур триптиказо-соевого бульона. Используемое разведение должно содержат 1000 или менее КОЕ / мл. Для S. agalactiae и 1.0×105 КОЕ / мл для E. coli .
- г. Инкубируйте пробирки с открытыми крышками при температуре 35 + 2 ° C в аэробной атмосфере.
- 3. Проверяйте пробирки на предмет роста в течение 3 дней.
Предлагаемые микроорганизмы для контроля качества и ожидаемые результаты включают:
Тест на чувствительность к антибиотикам
- С помощью ватного тампона приготовьте суспензию после 18-24-часового роста организм в физиологическом растворе или бульоне Мюллера-Хинтона, чтобы соответствовать 0,5 Макфарланда стандарт мутности.
- В течение 15 минут после регулировки мутности окуните стерильную вату. тампон в отрегулированную подвеску.Тампон следует повернуть несколько раз. раз и плотно прижать к внутренней стенке трубки над уровень жидкости. Используйте тампон для инокуляции всей поверхности Мюллера-Хинтона. пластина с агаром с овечьей кровью. После высыхания пластины используйте стерильные щипцы. поместить диск клиндамицина (2 мкг) на половину планшета и диск с эритромицином (15 мкг) на другую половину.
- Инкубируйте при 35 ° C в 5% CO2 в течение 20-24 часов.
- Измерьте диаметр зоны подавления с помощью линейки или штангенциркуля. Интерпретировать в соответствии с руководящими принципами NCCLS для видов Streptococcus кроме S. pneumoniae .
2002 Точки останова *
Клиндамицин:
- ≥ 19 мм = восприимчивый
- 16-18 = средний
- ≤ 15 = стойкий
Эритромицин:
- ≥ 21 мм = восприимчивый
- 16-20 = средний
- ≤ 15 = стойкий
* Источник: NCCLS.Стандарт эффективности по чувствительности к противомикробным препаратам
тестирование, M100-S12, Таблица 2H, Уэйн, Па .:
NCCLS, 2002. NCCLS рекомендует дисковую диффузию (M-2) или микроразбавление в бульоне.
тестирование (М-7) для определения чувствительности к СГБ. Коммерческие системы, которые
были одобрены или одобрены для тестирования на стрептококки, отличные от S.
pneumoniae также можно использовать. Тест на чувствительность к пенициллину
обычно не рекомендуется для лечения GBS, поскольку изоляты, устойчивые к пенициллину
на сегодняшний день не подтверждены.
Лаборатория общественного здравоохранения
Джон Бессер, M.S., Сью Джонсон, M.T. (ASCP)
Отдел по расследованию и контролю острых заболеваний
Рут Линфилд, доктор медицины, Крейг Морин, магистр медицины, Карен Уайт, магистр медицины, Ричард
Данила, к.э.н., магистр.
Авторы выражают признательность Синтии Г. Уитни, Ричарду Р.Facklam, Анне Шухат, Шарон Л. Хиллиер и Патриции Ферриери за их вклад к этому документу.
Список литературы- Руководство по клинической микробиологии ASM. Издание седьмое. 1999. с. 285.
- Комитет по акушерской практике, Американский колледж акушеров и Гинекологи. Профилактика стрептококковой инфекции группы B с ранним началом у новорожденных.Вашингтон; Американский колледж акушеров и гинекологов. 1996.
- Комитет по инфекционным болезням / Комитет по плодам и новорожденным, Американский Академия педиатрии. Пересмотренные рекомендации по профилактике раннего начала стрептококковая инфекция группы B. Педиатрия 1997; 99: 489-96.
- Справочник по процедурам клинической микробиологии. 1992. Vol 2: 1.20.12-23.
- Руководство по клинической микробиологии ASM.Издание шестое. 1995. стр. 300-305.
- Диагностическая микробиология Бейли и Скотта. 1994. Издание девятое. С. 340-342.
- Профилактика перинатального стрептококкового заболевания группы B: общественное здравоохранение Перспектива. CDC MMWR. 31 мая 1996 г. Т. 45. № РР-7.
- Профилактика перинатальной стрептококковой болезни группы B: пересмотренные рекомендации из CDC. CDC MMWR.16 августа 2002 г. Т. 51.
- Хиллер, С.Л., А. Шучат, 1997. Профилактика стрептококков группы B у новорожденных болезнь: роль лаборатории клинической микробиологии. Клиническая микробиология Информационный бюллетень Том 19: 113-16.
- Whitney, C.G., B. Schwartz, K. Deaver, W. Gozansky, J. Wenger, A. Schuchat. 1995. Институционализация профилактики перинатальных стрептококков группы B. (GBS) Инфекции.ICAAC Abstract K192: p. 322.
- Рекомендации по сбору и культивированию клинических образцов беременных Женщины для стрептококков группы B. Ноябрь 1997 г. Департамент Коннектикута Здравоохранение.
- Бейкер, С.Дж. 1996. Неадекватность быстрых иммуноанализов для выявления во время родов. носителей стрептококков группы B. Акушерство и гинекология. Том 33. № 1.
- NCCLS.1996. Гарантия качества для коммерчески подготовленных СМИ — второй Издание: Утвержденный стандарт. M22-A2. Том 16.
- Philipson, E.H., D.A. Палермино, А. Робинсон. 1995. Усиленная антенатальная обнаружение колонизации стрептококками группы B. Акушерство и гинекология. 85: 437-9.
- Платт, М.В., Дж. К. Маклафлин, Дж. Дж. Гилсон, М.Ф. Wellhoner, L.J. Nims. 1996. Повышенное выздоровление стрептококков группы B за счет включения ректальное культивирование и обогащение.Диагностическая микробиология инфекционных болезней. 21: 65-8.
- Бульон Тодда Хьюитта с гентамицином и налидиксовой кислотой (Trans-Vag Broth) Технический Информация. 1993. Remel Microbiology Products.
- LIM Broth Контроль качества / Информация о продукте. 2001. Контроль качества BBL и Руководство по информации о продукте для трубчатых носителей.
Написано 28.05.98
Редакция 03.03.2000, 01.08.2003
Бактериальный вагиноз, микрофлора влагалища и правила гигиены влагалища у пациентов с синдромом выделений из влагалища в Гамбии, Западная Африка | BMC Инфекционные болезни
Hillier SL, Holmes KK: Бактериальный вагиноз. Заболевания, передающиеся половым путем. Под редакцией: Holmes KK, Sparling PF, Mardh PA, Lemon SM, Stamm WA, Piot P и Wasserheit JN. 1999, Нью-Йорк, Макгроу-Хилл, 563-586. 3-й
Google Scholar
Hillier SL, Nugent RP, Eschenbach DA, Krohn MA, Gibbs RS, Martin DH, Cotch MF, Edelman R, Pastorek 2nd JG, Rao AV, McNellis D, Regan JA, Carey JC, Klebanoff MA, и Группа изучения вагинальных инфекций и недоношенности.: Связь между бактериальным вагинозом и преждевременными родами ребенка с низкой массой тела при рождении. N Engl J Med. 1995, 333: 1737-1742. 10.1056 / NEJM199512283332604.
CAS Статья PubMed Google Scholar
Севанкамбо Н., Грей Р.Х., Вавер М.Дж., Пакстон Л., Макнейм Д., Вабвайр-Манген Ф., Сервадда Д., Ли С., Киванука Н., Хиллиер С.Л., Рабе Л., Гайдос, Калифорния, Куинн Т.К., Конде-Луле J: ВИЧ-1 инфекция, связанная с аномальной морфологией вагинальной флоры и бактериальным вагинозом.Ланцет. 1997, 350: 546-550. 10.1016 / S0140-6736 (97) 01063-5.
CAS Статья PubMed Google Scholar
Taha TE, Hoover DR, Dallabetta GA, Kumwenda NI, Mtimavalye LA, Yang LP, Liomba GN, Broadhead RL, Chiphangwi JD, Miotti PG: Бактериальный вагиноз и нарушения влагалищной флоры: связь с увеличением заражения ВИЧ . СПИД. 1998, 12: 1699-1706. 10.1097 / 00002030-199813000-00019.
CAS Статья PubMed Google Scholar
Шмид Г., Марковиц Л., Джозеф Р., Куманс Е.: Бактериальный вагиноз и ВИЧ-инфекция. Половая трансмиссия. 2000, 76: 3-4. 10.1136 / sti.76.1.3.
CAS Статья PubMed PubMed Central Google Scholar
Фонк К., Кидула Н., Яоко В., Эстамбале Б., Клэйс П., Ндинья-Ахола Дж., Кируи П., Буэйо Дж., Теммерман М.: Действительность алгоритма вагинальных выделений среди беременных и небеременных женщин в Найроби , Кения. Половая трансмиссия.2000, 76: 33-38. 10.1136 / sti.76.1.33.
CAS Статья PubMed PubMed Central Google Scholar
Ледру С., Меда Н., Фофана М., Соула Дж., Бази А.Дж., Хирон Дж. П.: Этиологическое исследование мочеполовых инфекций у женщин детородного возраста в Бобо-Диуласо, Буркина-Фасо, 1992. Sex Transm Dis. 1996, 23: 151-156.
CAS Статья PubMed Google Scholar
Mayaud P, ka-Gina G, Cornelissen J, Todd J, Kaatano G, West B, Uledi E, Rwakatare M, Kopwe L, Manoko D, Laga M, Grosskurth H, Hayes R, Mabey D: валидация алгоритма ВОЗ с оценкой риска для клинического лечения выделений из влагалища в Мванзе, Танзания. Половая трансмиссия. 1998, 74: S77-84.
PubMed Google Scholar
Govender L, Hoosen AA, Moodley J, Moodley P, Sturm AW: Бактериальный вагиноз и связанные с ним инфекции во время беременности.Int J Gynaecol Obstet. 1996, 55: 23-28. 10.1016 / 0020-7292 (96) 02744-0.
CAS Статья PubMed Google Scholar
Mayaud P, Uledi E, Cornelissen J, ka-Gina G, Todd J, Rwakatare M, West B, Kopwe L, Manoko D, Grosskurth H, Hayes R, Mabey D: оценка риска для выявления цервикальных инфекций в городских женских консультациях в Мванзе, Танзания. Половая трансмиссия. 1998, 74: S139-46.
PubMed Google Scholar
Томас Т., Чоудри С., Кариуки С., Моисей С.: Выявление инфекции шейки матки среди беременных женщин в Найроби, Кения: ограничения подходов, основанных на оценке риска и симптомах. Genitourin Med. 1996, 72: 334-338.
CAS PubMed PubMed Central Google Scholar
Валравен Г., Шерф С., Вест Б., Экпо Г., Пейн К., Коулман Р., Бейли Р., Морисон Л.: Бремя болезней репродуктивных органов у сельских женщин в Гамбии, Западная Африка.Ланцет. 2001, 357: 1161-1167. 10.1016 / S0140-6736 (00) 04333-6.
CAS Статья PubMed Google Scholar
Моррис М.К., Роджерс П.А., Кингхорн Г.Р .: Бактериальный вагиноз — это инфекция, передающаяся половым путем ?. Половая трансмиссия. 2001, 77: 63-68. 10.1136 / sti.77.1.63.
CAS Статья PubMed PubMed Central Google Scholar
Hay PE, Taylor-Robinson D, Lamont RF: Диагностика бактериального вагиноза в гинекологической клинике.Br J Obstet Gynaecol. 1992, 99: 63-66.
CAS Статья PubMed Google Scholar
Holzman C, Leventhal JM, Qiu H, Jones NM, Wang J: Факторы, связанные с бактериальным вагинозом у небеременных женщин. Am J Public Health. 2001, 91: 1664-1670.
CAS Статья PubMed PubMed Central Google Scholar
Амсель Р., Тоттен П.А., Шпигель КА, Чен К.С., Эшенбах Д., Холмс К.К.: Неспецифический вагинит.Диагностические критерии и микробно-эпидемиологические ассоциации. Am J Med. 1983, 74: 14-22. 10.1016 / 0002-9343 (83)
-9.
CAS Статья PubMed Google Scholar
Ньюджент Р.П., Крон М.А., Хиллиер С.Л.: Надежность диагностики бактериального вагиноза повышается за счет стандартизированного метода интерпретации окраски по Граму. J Clin Microbiol. 1991, 29: 297-301.
CAS PubMed PubMed Central Google Scholar
Martino JL, Vermund SH: Спринцевание: доказательства рисков или пользы для здоровья женщины. Epidemiol Rev.2002, 24: 109-124. 10.1093 / эпирев / mxf004.
Артикул PubMed PubMed Central Google Scholar
Фонк К., Каул Р., Кели Ф, Бвайо Дж. Дж., Нгуги Э. Н., Мозес С., Теммерман М.: Инфекции, передаваемые половым путем, и вагинальные спринцевания среди женщин-секс-работников в Найроби, Кения. Половая трансмиссия. 2001, 77: 271-275.10.1136 / sti.77.4.271.
CAS Статья PubMed PubMed Central Google Scholar
Gresenguet G, Kreiss JK, Chapko MK, Hillier SL, Weiss NS: ВИЧ-инфекция и спринцевание в центральной Африке. СПИД. 1997, 11: 101-106. 10.1097 / 00002030-199701000-00015.
CAS Статья PubMed Google Scholar
West B, Morison L, van der Loeff MS, Gooding E, Awasana AA, Demba E, Mayaud P: Оценка нового набора для быстрой диагностики (FemExam) бактериального вагиноза у пациентов с синдромом выделений из влагалища в Гамбия.Sex Transm Dis. 2003, 30: 483-489.
Артикул PubMed Google Scholar
Бейли Р.Л., Хэмптон Т.Дж., Хейс Л.Дж., Уорд М.Э., Уиттл Х.С., Мейби Д.К.: Полимеразная цепная реакция для обнаружения глазной хламидийной инфекции в эндемичных по трахоме сообществах. J Infect Dis. 1994, 170: 709-712.
CAS Статья PubMed Google Scholar
Schim van der Loeff MF, Jaffar S, Aveika AA, Sabally S, Corrah T., Harding E, Alabi A, Bayang A, Ariyoshi K, Whittle HC: Смертность от ВИЧ-1, ВИЧ-2 и ВИЧ -1 / ВИЧ-2 пациенты с двойной инфекцией в клинике в Гамбии.СПИД. 2002, 16: 1775-1783. 10.1097 / 00002030-200209060-00010.
Артикул PubMed Google Scholar
Eschenbach DA, Davick PR, Williams BL, Klebanoff SJ, Young-Smith K, Critchlow CM, Holmes KK: Распространенность видов Lactobacillus, продуцирующих перекись водорода, у здоровых женщин и женщин с бактериальным вагинозом. J Clin Microbiol. 1989, 27: 251-256.
CAS PubMed PubMed Central Google Scholar
Конеман Э. У., Аллен С. Д., Янда В. М., Шрекенбергер П. К., Винн-младший В. К.: Атлас цветов и учебник по диагностической микробиологии. 1992, Филадельфия, Дж. Б. Липпинкотт, 4-я
Google Scholar
Морисон Л., Шерф С., Экпо Дж., Пейн К., Вест Б., Коулман Р., Валравен Г.: Долгосрочные последствия обрезания женских гениталий для репродуктивного здоровья в сельских районах Гамбии: обследование на уровне общины. Тропическая медицина и международное здоровье. 2001, 6: 643-653.10.1046 / j.1365-3156.2001.00749.x.
CAS Статья PubMed Google Scholar
Costello Daly C, Wangel AM, Hoffman IF, Canner JK, Lule GS, Lema VM, Liomba NG, Dallabetta GA: проверка диагностического алгоритма ВОЗ и разработка альтернативной системы оценки для ведения женщин с выделениями из влагалища в Малави. Половая трансмиссия. 1998, 74: S50-8.
Артикул PubMed Google Scholar
Schneider H, Coetzee DJ, Fehler HG, Bellingan A, Dangor Y, Radebe F, Ballard RC: Скрининг на заболевания, передаваемые половым путем, у сельских женщин Южной Африки. Половая трансмиссия. 1998, 74: S147-52.
PubMed Google Scholar
Ройс Р.А., Джексон Т.П., Торп Дж.Дж.М., Хиллиер С.Л., Рабе Л.К., Пасторе Л.М., Савиц Д.А.: расовая / этническая принадлежность, структура вагинальной флоры и pH во время беременности. Sex Transm Dis. 1999, 26: 96-102.
CAS Статья PubMed Google Scholar
Ройс Р.А., Торп Дж., Гранадос Дж. Л., Савиц Д.А.: Бактериальный вагиноз, связанный с ВИЧ-инфекцией, у беременных женщин из Северной Каролины. J Acquir Immune Defic Syndr Hum Retrovirol. 1999, 20: 382-386.
CAS Статья PubMed Google Scholar
La Ruche G, Messou N, Ali-Napo L, Noba V, Faye-Kette H, Combe P, Bonard D, Sylla-Koko F, Dheha D, Welffens-Ekra C, Dosso M, Msellati P : Спринцевание: связь с инфекциями нижних половых путей у беременных африканских женщин.Sex Transm Dis. 1999, 26: 191-196.
CAS Статья PubMed Google Scholar
Хилл ГБ: Микробиология бактериального вагиноза. Am J Obstet Gynecol. 1993, 169: 450-454.
CAS Статья PubMed Google Scholar
Spiegel CA: Бактериальный вагиноз. Clin Microbiol Rev.1991, 4: 485-502.
CAS Статья PubMed PubMed Central Google Scholar
Hawes SE, Hillier SL, Benedetti J, Stevens CE, Koutsky LA, Wolner-Hanssen P, Holmes KK: лактобациллы, продуцирующие перекись водорода, и приобретение вагинальных инфекций. J Infect Dis. 1996, 174: 1058-1063.
CAS Статья PubMed Google Scholar
Hillier SL, Krohn MA, Klebanoff SJ, Eschenbach DA: Связь лактобацилл, продуцирующих перекись водорода, с бактериальным вагинозом и генитальной микрофлорой у беременных женщин.Obstet Gynecol. 1992, 79: 369-373.
CAS Статья PubMed Google Scholar
Klebanoff SJ, Coombs RW: Вирицидный эффект Lactobacillus acidophilus на вирус иммунодефицита человека типа 1: возможная роль в гетеросексуальной передаче. J Exp Med. 1991, 174: 289-292. 10.1084 / jem.174.1.289.
CAS Статья PubMed Google Scholar
Boskey ER, Telsch KM, Whaley KJ, Moench TR, Cone RA: Продукция кислоты вагинальной флорой in vitro согласуется со скоростью и степенью закисления влагалища.Заражение иммунной. 1999, 67: 5170-5175.
CAS PubMed PubMed Central Google Scholar
Reid G: Пробиотические агенты для защиты урогенитального тракта от инфекций. Am J Clin Nutr. 2001, 73: 437С-443С.
CAS PubMed Google Scholar
Mardh PA, Elshibly S, Kalling I., Hellberg D: Изменения флоры влагалища, связанные с Mycoplasma hominis.Am J Obstet Gynecol. 1997, 176: 173-178.
CAS Статья PubMed Google Scholar
Thorsen P, Jensen IP, Jeune B, Ebbesen N, Arpi M, Bremmelgaard A, Moller BR: Несколько микроорганизмов, связанных с бактериальным вагинозом, могут составлять патологическое ядро: популяционное микробиологическое исследование среди 3596 беременных женщин. Am J Obstet Gynecol. 1998, 178: 580-587.
CAS Статья PubMed Google Scholar
Arya OP, Tong CY, Hart CA, Pratt BC, Hughes S, Roberts P, Kirby P, Howel J, McCormick A, Goddard AD: Является ли Mycoplasma hominis вагинальным патогеном ?. Половая трансмиссия. 2001, 77: 58-62. 10.1136 / sti.77.1.58.
CAS Статья PubMed PubMed Central Google Scholar
Regan JA, Klebanoff MA, Nugent RP, Eschenbach DA, Blackwelder WC, Lou Y, Gibbs RS, Rettig PJ, Martin DH, Edelman R: Колонизация стрептококками группы B во время беременности и неблагоприятный исход: VIP Study Group .Am J Obstet Gynecol. 1996, 174: 1354-1360.
CAS Статья PubMed Google Scholar
Suara RO, Adegbola RA, Barker CJ, Secka O, Mulholland EK, Greenwood BM: Носительство стрептококков группы B у беременных гамбийских матерей и их младенцев. J Infect Dis. 1994, 170: 1316-1319.
CAS Статья PubMed Google Scholar
Основы практики, обзор, Streptococcus группы B
Автор
Дарвин Скотт Смит, MD, MSc, DTM & H Адъюнкт-доцент кафедры микробиологии и иммунологии Медицинской школы Стэнфордского университета; Заведующий отделением инфекционных болезней и географической медицины, Отделение внутренней медицины, Kaiser Permanente Medical Group
Дарвин Скотт Смит, доктор медицинских наук, магистр наук, DTM & H является членом следующих медицинских обществ: Американской медицинской ассоциации, Американского общества тропической медицины и гигиены, инфекционных заболеваний. Американское общество болезней, Международное общество медицины путешествий
Раскрытие информации: нечего раскрывать.
Соавтор (ы)
Маниш Басистха, магистр здравоохранения, CIC, CWS, CASP, FACCWS, HACP Старший менеджер программы профилактики и контроля инфекций, больница Kaiser Foundation в Редвуд-Сити
Маниш Басистха, магистр здравоохранения, CIC, CWS, CASP, FACCWS, член HACP следующих медицинских обществ: Академия общего образования, Американский колледж специалистов по клиническим ранам, Американский колледж эпидемиологии, Ассоциация профессионалов в области инфекционного контроля и эпидемиологии, Международная федерация инфекционного контроля, Общество эпидемиологии здравоохранения Америки
Раскрытие информации: ничего не раскрыть.
Специальная редакционная коллегия
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Получил зарплату от Medscape за работу. для: Medscape.
Карл В. Смит, доктор медицины Выдающиеся Крис Дж. И Мари А. Олсон, заведующий кафедрой акушерства и гинекологии, профессор кафедры акушерства и гинекологии, старший заместитель декана по клиническим вопросам, Медицинский центр Университета Небраски
Карл В. Смит, доктор медицинских наук, член следующих медицинских обществ: Американского колледжа акушеров и гинекологов, Американского института ультразвука в медицине, Ассоциации профессоров гинекологии и акушерства, Центральной ассоциации акушеров и гинекологов, Общества материнско-фетальной медицины, Совета кафедр акушерства при университетах. и гинекологии, Медицинская ассоциация Небраски
Раскрытие: Ничего не раскрывать.
Главный редактор
Карл В. Смит, доктор медицины Выдающиеся Крис Дж. И Мари А. Олсон, заведующий кафедрой акушерства и гинекологии, профессор кафедры акушерства и гинекологии, старший заместитель декана по клиническим вопросам, Медицинский центр Университета Небраски
Карл В. Смит, доктор медицинских наук, член следующих медицинских обществ: Американского колледжа акушеров и гинекологов, Американского института ультразвука в медицине, Ассоциации профессоров гинекологии и акушерства, Центральной ассоциации акушеров и гинекологов, Общества материнско-фетальной медицины, Совета кафедр акушерства при университетах. и гинекологии, Медицинская ассоциация Небраски
Раскрытие: Ничего не раскрывать.
Дополнительные участники
Стефани А. Невинс Научный сотрудник, Отдел генетики, Лаборатория Снайдера, Медицинский факультет Стэнфордского университета
Раскрытие: Ничего не разглашать.
Благодарности
Леонард Б. Берковиц, доктор медицины Начальник отдела инфекционных заболеваний и служб ВИЧ / СПИДа, Бруклинский госпитальный центр; Доцент кафедры медицины Государственного университета Нью-Йорка в Бруклине
Леонард Б. Берковиц, доктор медицинских наук, является членом следующих медицинских обществ: Американского колледжа врачей, Американского общества микробиологов, Американского общества инфекционных болезней и Phi Beta Kappa
.Раскрытие информации: нечего раскрывать.
Хайзал Хамза, MD Старший врач отделения внутренней медицины, клиника Fairview Ridges
Раскрытие информации: нечего раскрывать.
Фаузия Хаттак, MD Врач-резидент, отделение внутренней медицины, Бруклинский больничный центр, Медицинский колледж Вейл Корнелл
Раскрытие информации: нечего раскрывать.
Хизер Комер Юн, директор программы MD , Сообщество по инфекционным заболеваниям, Консорциум санитарного просвещения военнослужащих силовых структур Сан-Антонио (SAUSHEC)
Хизер Комер Юн, доктор медицинских наук, является членом следующих медицинских обществ: Alpha Omega Alpha, Американский колледж врачей — Американское общество внутренней медицины, Общество инфекционных болезней вооруженных сил и Общество инфекционных болезней Америки
Раскрытие информации: нечего раскрывать.
Аномальная микрофлора влагалища у небеременных и беременных женщин с симптомами в греческой больнице: проспективное исследование
Дондерс Г.Г. (1999) Микроскопия бактериальной флоры на свежих мазках из влагалища. Infect Dis Obstet Gynecol 7: 177–179
CAS Статья PubMed PubMed Central Google Scholar
Donders GG, Bosmans E, Dekeersmaecker A et al (2000) Патогенез аномальной бактериальной флоры влагалища.Am J Obstet Gynecol 182: 872–878
CAS Статья PubMed Google Scholar
Geng N, Wu W, Fan A et al (2015) Анализ факторов риска аэробного вагинита: исследование случай – контроль. Gynecol Obstet Invest 81: 148–154
Статья Google Scholar
Donders GG, Vereecken A, Bosmans E et al (2002) Определение типа аномальной микрофлоры влагалища, которая отличается от бактериального вагиноза: аэробный вагинит.BJOG 109: 34–43
Статья PubMed Google Scholar
Донати Л., Ди Вико А., Нуччи М. и др. (2010) Микробная флора влагалища и исход беременности. Arch Gynecol Obstet 281: 589–600
Артикул PubMed Google Scholar
Donders GG, Van Calsteren C, Bellen G et al (2010) Связь между аномальной флорой влагалища и длиной шейки матки как факторами риска преждевременных родов.Ультразвуковой акушерский гинекол [Epub перед печатью]
Donders GG, Van Calsteren K, Bellen G et al (2009) Прогностическое значение аномальной флоры влагалища, бактериального вагиноза и аэробного вагинита в отношении преждевременных родов в первом триместре беременности . BJOG 116: 1315–1324
CAS Статья PubMed Google Scholar
Han C, Wu W, Fan A et al (2015) Достижения в диагностике и лечении аэробного вагинита.Arch Gynecol Obstet 291: 251–257
Артикул PubMed Google Scholar
Виейра-Баптиста П., Лима-Силва Дж., Пинто С. и др. (2016) Бактериальный вагиноз, аэробный вагинит, воспаление влагалища и серьезные аномалии мазка Папаниколау. Eur J Clin Microbiol Infect Dis 35: 657–664
CAS Статья PubMed Google Scholar
Iavazzo C, Vogiatzi C, Falagas ME (2008) Ретроспективный анализ изолятов от пациентов с вагинитом в частной греческой акушерско-гинекологической больнице (2003-2006).Med Sci Monit 14: CR228 – CR231
PubMed Google Scholar
Тансарли Г.С., Костарас Е.К., Атанасиу С. и др. (2013) Распространенность и лечение аэробного вагинита среди небеременных женщин: оценка доказательств для недооцененной клинической сущности. Eur J Clin Microbiol Infect Dis 32: 977–984
CAS Статья PubMed Google Scholar
CLSI
Amsel R, Totten PA, Spiegel CA et al (1983) Неспецифический вагинит. Диагностические критерии и микробно-эпидемиологические ассоциации. Am J Med 74: 14–22
CAS Статья PubMed Google Scholar
Maniatis AN, Palermos J, Kantzanou M et al (1996) Streptococcus agalactiae: вагинальный патоген? J Med Microbiol 44: 199–202
CAS Статья PubMed Google Scholar
Donders G, Bellen G, Rezeberga D (2011) Аэробный вагинит во время беременности. BJOG 118: 1163–1170
Статья PubMed Google Scholar
Frobenius W, Bogdan C (2015) Диагностическая ценность выделений из влагалища, Влажное соединение и влагалищный pH — обновленная информация по основам гинекологической инфекционности. Geburtshilfe Frauenheilkd 75: 355–366
CAS Статья PubMed PubMed Central Google Scholar
Fan A, Yue Y, Geng N et al (2013) Аэробный вагинит и смешанные инфекции: сравнение клинических и лабораторных данных. Arch Gynecol Obstet 287: 329–335
Артикул PubMed Google Scholar
Wang C, Han C, Geng N et al (2016) Эффективность перорального моксифлоксацина при аэробном вагините. Eur J Clin Microbiol Infect Dis 35: 95–101
CAS Статья PubMed Google Scholar
Heczko PB, Tomusiak A, Adamski P et al (2015) Дополнение стандартной антибиотикотерапии пероральными пробиотиками для бактериального вагиноза и аэробного вагинита: рандомизированное двойное слепое плацебо-контролируемое исследование. BMC Womens Health 15: 115
Статья PubMed PubMed Central Google Scholar
Дондерс Г.Г., Рубан К., Беллен Г. (2015) Выбор антимикробного лечения аэробного вагинита. Curr Infect Dis Rep 17: 477
Статья PubMed Google Scholar
Пептострептококк — обзор | Темы ScienceDirect
2.7 Другие болезни
Микробный баланс в мочеполовых путях и влагалище может быть нарушен Gardnerella , Peptostreptococcus , Prevotella или аэробными кокками, а многие организмы могут вызывать инфекции мочевыводящих путей и бактериальный вагиноз (Kirjavainen et al. , 2009; Nelson et al., 2010; Lamont et al., 2011). Кроме того, сообщалось о различиях микробного состава у ВИЧ-инфицированных субъектов по сравнению с ВИЧ-серонегативными группами (Spear et al., 2011).
Новые данные о возрастных заболеваниях указывают на микробный дисбиоз как потенциальный фактор риска (Tiihonen et al., 2010). Ослабленная иммунная система также связана с повышенным риском хронических заболеваний, таких как аутоиммунные заболевания, атеросклероз, диабет 2 типа и даже болезнь Альцгеймера. С другой стороны, общие генетические и иммунологические механизмы лежат в основе совпадения воспаления в кишечнике и суставах. В недавнем исследовании сообщается о связи между бактериальным гастроэнтеритом и риском развития симптомов артрита (Garg et al., 2008), а отклонения в микробиоте были выявлены при артрите (Toivanen, 2003) и спондилите (Stebbings et al., 2009).
Способность микробиоты взаимодействовать с мозгом и модулировать поведение становится концепцией здоровья и болезней (Heijtz et al., 2011). Эпидемиологические исследования показали связь между нарушениями развития нервной системы, такими как аутизм и шизофрения, и микробными инфекциями в перинатальном периоде, но дисбактериоз в микробиоме кишечника также может приводить к нарушению регуляции иммунных ответов как в кишечнике, так и в дистальных эффекторных участках иммунной системы, таких как центральная нервная система.Недавние открытия предполагают, что изменение определенных бактериальных популяций, присутствующих в кишечнике, может привести к провоспалительному состоянию, которое может привести к развитию рассеянного склероза у человека (Ochoa-Repáraz et al., 2011). Кроме того, изменения в микробиоме были связаны с синдромом аутизма вместе с другими генетическими факторами и факторами окружающей среды (Ochoa-Repáraz et al., 2011; Sekirov et al., 2010). Кроме того, психические проблемы, включая шизофрению, беспокойство, стресс или депрессию, часто связаны с другими расстройствами, в которых могут играть роль нарушения микробиоты (Neufeld and Foster, 2009).Изменения микробиома кишечника также были связаны с большим депрессивным расстройством, демонстрируя снижение относительного процента конкретных комменсальных популяций, таких как Lactobacilli и Bifidobacterium (Dowlati et al., 2010). Изменения кишечной микробиоты также, по-видимому, играют важную роль в индукции и стимулировании прогрессирования поражения печени (Cesaro et al.
 , Eubacterium spp., Bifidobacterium spp., Propionibacterium spp., Clostridium spp.;
, Eubacterium spp., Bifidobacterium spp., Propionibacterium spp., Clostridium spp.;
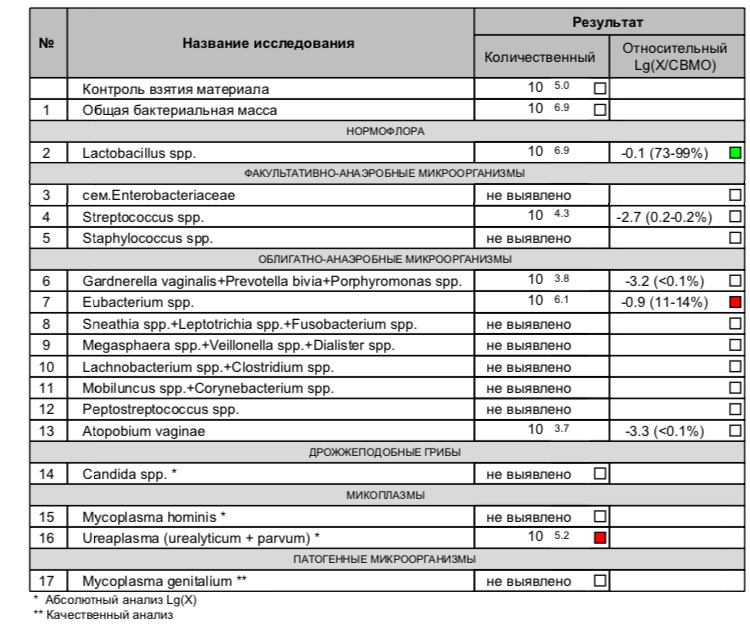 ,
,

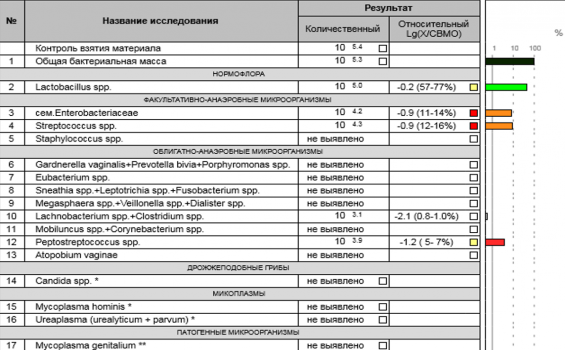
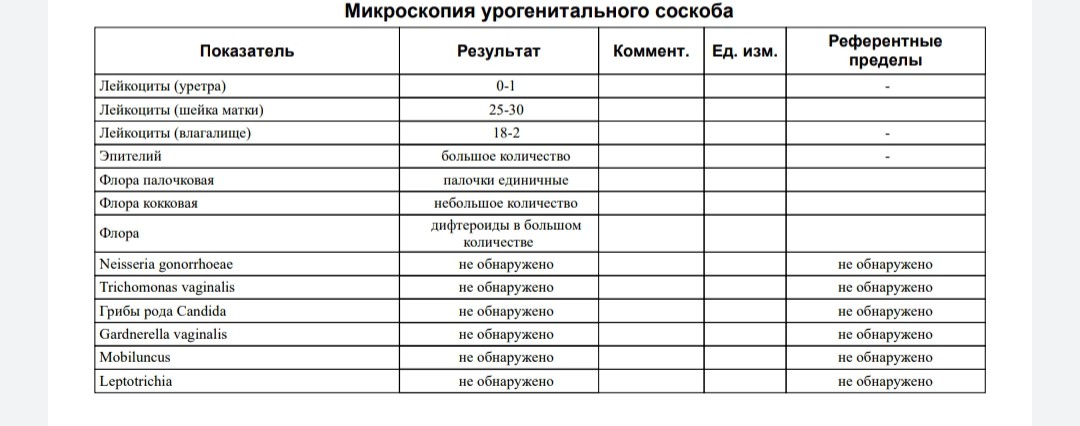
 Селится в половых органах и кишечнике. Особенно опасен для беременных, потому что в процессе родов способен заразить малыша.
Селится в половых органах и кишечнике. Особенно опасен для беременных, потому что в процессе родов способен заразить малыша.
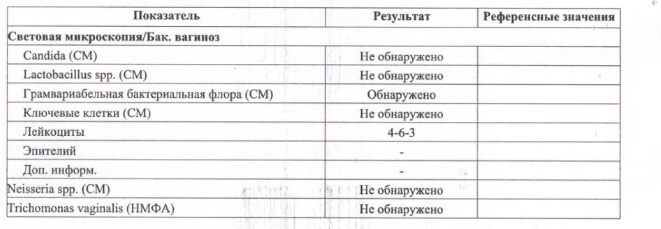 Так как энтерококк фекалис невосприимчив к антибиотикам тетрациклиновой группы, назначается длительный срок применения препаратов-бактериофагов. Препараты подбираются на основе данных о штамме бактерий и их восприимчивости к тем или иным средствам.
Так как энтерококк фекалис невосприимчив к антибиотикам тетрациклиновой группы, назначается длительный срок применения препаратов-бактериофагов. Препараты подбираются на основе данных о штамме бактерий и их восприимчивости к тем или иным средствам.